2018年10月23日
JO25567試験とNEJ026試験・・・エルロチニブ+ベバシズマブの位置づけは・・・?
ずっと棚上げにしてきた話題だが、今日は思い切って取り上げる。
以前もちょっとだけ触れた。
http://oitahaiganpractice.junglekouen.com/e935118.html
EGFR遺伝子変異陽性の進行非小細胞肺がん患者さんに対して、エルロチニブ単剤療法とエルロチニブ+ベバシズマブ併用療法の効果を検証する臨床試験。
ランダム化第II相試験のJO25567試験は、4年前には論文化されていて、エルロチニブ+ベバシズマブ療法が有意に無増悪生存期間を延長し、ベバシズマブの新たな可能性を示すepoch makingな結果を残した。
http://oitahaiganpractice.junglekouen.com/e751839.html
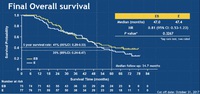
一方、この当時から全生存期間に大きな差がついていないことが意識されていた。
今年2018年の米国臨床腫瘍学会では、追跡調査の結果、無増悪生存期間には差がつくものの、全生存期間には差がつかないことが改めて報告された。
無増悪生存期間は延長するものの、全生存期間には寄与しないというベバシズマブの特性が、分子標的薬との併用でも追認されるという結果に終わった。
もちろん、無増悪生存期間の延長には意味がある。
医療従事者は全生存期間が金科玉条であり、無増悪生存期間はあくまでも副次的な目標、ととらえがちだが、患者さんやご家族の話を伺っていると、仮に全生存期間が延長しなかったとしても、無増悪生存期間が延長するなら治療の意義は十分にあるようだ。
問題は、無増悪生存期間の延長と引き換えに、ベバシズマブ特有の有害事象リスクを受け入れられるかどうかということだろう。
なお、サブグループ解析を見ると、術後再発患者では(対象患者数が少なく信頼性は落ちるものの)エルロチニブ+ベバシズマブ併用療法の方が優位に生存期間を延長したようだ。
病勢進行後の後治療については、オシメルチニブを含めて、両群に差異はなかった。



さて、一方のNEJ026試験。
JO25567試験の結果が公表されたときは、このデータなら第II相試験の段階で実地臨床に応用しても差し支えないだろうという議論が大勢だった。
実際に、欧州ではJO25567試験とBELIEF試験のデータを背景として、エルロチニブ+ベバシズマブ併用療法を規制当局が承認した。
http://oitahaiganpractice.junglekouen.com/e851167.html
http://oitahaiganpractice.junglekouen.com/e906132.html
http://oitahaiganpractice.junglekouen.com/e914142.html
しかし、(私を含め)第III相臨床試験原理主義者が多い我が国では、第III相試験できちんと検証すべきだろうということになり、NEJグループがNEJ026試験を立ち上げた。
基本的には第II相試験であるJO25567試験の内容を第III相ランダム化比較試験へ拡大したという位置づけだが、病勢増悪後の後治療も規定されている。
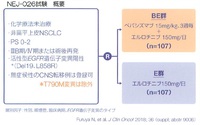
エルロチニブ単剤療法(E)群では、後治療はプラチナ製剤+ペメトレキセド併用療法からペメトレキセド維持療法、エルロチニブ+ベバシズマブ併用療法(BE)群では、後治療はプラチナ製剤+ペメトレキセド+ベバシズマブ併用療法からペメトレキセド+ベバシズマブ併用維持療法、というように、併用群ではbeyond PDでのベバシズマブ継続使用が規定されていた。
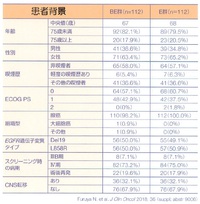
結果として、E群およびBE群の無増悪生存期間中央値はそれぞれ13.3ヶ月、16.9ヶ月でハザード比は0.65(95%信頼区間は0.417-0.877)、p値は0.01573と有意にBE群で優れていた。

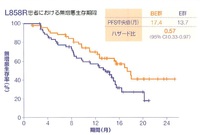
さらに、EGFR遺伝子変異型別のサブグループ解析では、Exon 19欠失変異では両群に有意差は認められず、Exon21点突然変異ではBE群が有意に優れる結果だった。

有害事象は、予想通り高血圧・タンパク尿・出血がBE群で高頻度となっており、無増悪生存期間延長のためにこれを許容できるかが焦点である。
なんにせよ、JO25567試験で認められた無増悪生存期間延長効果がNEJ026試験でも認められたわけで、Exon 21変異でより効果が高かったことを考えると、若い患者でExon 19変異の人はアファチニブ、Exon 21変異の人はエルロチニブ+ベバシズマブといった使い分けもできるのではないだろうか。
まだ先の話だが、おそらく全生存期間はJO25567試験の結果を追認することになるだろう。
しかし、JO25567試験で確認された、両群とも生存期間中央値が47ヶ月以上という事実、従来のエルロチニブの臨床効果と比較すると、やや長すぎるような違和感を覚えるのは私だけだろうか。
要は生存期間中央値が4年ということであり、これはLUX-Lung 3試験から得られた日本人に対するアファチニブの生存期間延長効果に匹敵する。
http://oitahaiganpractice.junglekouen.com/e821581.html
以前もちょっとだけ触れた。
http://oitahaiganpractice.junglekouen.com/e935118.html
EGFR遺伝子変異陽性の進行非小細胞肺がん患者さんに対して、エルロチニブ単剤療法とエルロチニブ+ベバシズマブ併用療法の効果を検証する臨床試験。
ランダム化第II相試験のJO25567試験は、4年前には論文化されていて、エルロチニブ+ベバシズマブ療法が有意に無増悪生存期間を延長し、ベバシズマブの新たな可能性を示すepoch makingな結果を残した。
http://oitahaiganpractice.junglekouen.com/e751839.html
一方、この当時から全生存期間に大きな差がついていないことが意識されていた。
今年2018年の米国臨床腫瘍学会では、追跡調査の結果、無増悪生存期間には差がつくものの、全生存期間には差がつかないことが改めて報告された。
無増悪生存期間は延長するものの、全生存期間には寄与しないというベバシズマブの特性が、分子標的薬との併用でも追認されるという結果に終わった。
もちろん、無増悪生存期間の延長には意味がある。
医療従事者は全生存期間が金科玉条であり、無増悪生存期間はあくまでも副次的な目標、ととらえがちだが、患者さんやご家族の話を伺っていると、仮に全生存期間が延長しなかったとしても、無増悪生存期間が延長するなら治療の意義は十分にあるようだ。
問題は、無増悪生存期間の延長と引き換えに、ベバシズマブ特有の有害事象リスクを受け入れられるかどうかということだろう。
なお、サブグループ解析を見ると、術後再発患者では(対象患者数が少なく信頼性は落ちるものの)エルロチニブ+ベバシズマブ併用療法の方が優位に生存期間を延長したようだ。
病勢進行後の後治療については、オシメルチニブを含めて、両群に差異はなかった。




さて、一方のNEJ026試験。
JO25567試験の結果が公表されたときは、このデータなら第II相試験の段階で実地臨床に応用しても差し支えないだろうという議論が大勢だった。
実際に、欧州ではJO25567試験とBELIEF試験のデータを背景として、エルロチニブ+ベバシズマブ併用療法を規制当局が承認した。
http://oitahaiganpractice.junglekouen.com/e851167.html
http://oitahaiganpractice.junglekouen.com/e906132.html
http://oitahaiganpractice.junglekouen.com/e914142.html
しかし、(私を含め)第III相臨床試験原理主義者が多い我が国では、第III相試験できちんと検証すべきだろうということになり、NEJグループがNEJ026試験を立ち上げた。
基本的には第II相試験であるJO25567試験の内容を第III相ランダム化比較試験へ拡大したという位置づけだが、病勢増悪後の後治療も規定されている。
エルロチニブ単剤療法(E)群では、後治療はプラチナ製剤+ペメトレキセド併用療法からペメトレキセド維持療法、エルロチニブ+ベバシズマブ併用療法(BE)群では、後治療はプラチナ製剤+ペメトレキセド+ベバシズマブ併用療法からペメトレキセド+ベバシズマブ併用維持療法、というように、併用群ではbeyond PDでのベバシズマブ継続使用が規定されていた。


結果として、E群およびBE群の無増悪生存期間中央値はそれぞれ13.3ヶ月、16.9ヶ月でハザード比は0.65(95%信頼区間は0.417-0.877)、p値は0.01573と有意にBE群で優れていた。

さらに、EGFR遺伝子変異型別のサブグループ解析では、Exon 19欠失変異では両群に有意差は認められず、Exon21点突然変異ではBE群が有意に優れる結果だった。


有害事象は、予想通り高血圧・タンパク尿・出血がBE群で高頻度となっており、無増悪生存期間延長のためにこれを許容できるかが焦点である。
なんにせよ、JO25567試験で認められた無増悪生存期間延長効果がNEJ026試験でも認められたわけで、Exon 21変異でより効果が高かったことを考えると、若い患者でExon 19変異の人はアファチニブ、Exon 21変異の人はエルロチニブ+ベバシズマブといった使い分けもできるのではないだろうか。
まだ先の話だが、おそらく全生存期間はJO25567試験の結果を追認することになるだろう。
しかし、JO25567試験で確認された、両群とも生存期間中央値が47ヶ月以上という事実、従来のエルロチニブの臨床効果と比較すると、やや長すぎるような違和感を覚えるのは私だけだろうか。
要は生存期間中央値が4年ということであり、これはLUX-Lung 3試験から得られた日本人に対するアファチニブの生存期間延長効果に匹敵する。
http://oitahaiganpractice.junglekouen.com/e821581.html
セルペルカチニブ、上市
CLIP1-LTK融合遺伝子の発見・・・LC-SCRUM Asiaから
セルペルカチニブ、2021年12月13日発売予定
セルペルカチニブと過敏症
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
脳転移を有する患者集団に対しても、免疫チェックポイント阻害薬は有効なのか
第4世代ALK阻害薬・・・TPX-0131とNVL-655
セルペルカチニブ、製造販売承認
ドライバー遺伝子変異陽性患者におけるPACIFICレジメンの有効性
HER2遺伝子変異陽性肺がんに対するtrastuzumab deruxtecan
オシメルチニブ耐性化後は、耐性機序同定や分子標的治療は意味がないのか
EGFR/ALK陽性非小細胞肺がんに対するカルボプラチン+ペメトレキセド+ペンブロリズマブ併用療法
ドライバー遺伝子異常検出におけるジレンマとmultiplex PCR
中国人患者におけるRET阻害薬(Selpercatinib, Pralsetinib)の有効性
オシメルチニブによる術前療法・・・NeoADAURAの前哨戦
BRAF遺伝子変異と縁がない
RET阻害薬、セルペルカチニブがやってくる
進行が速い進行肺腺がんに遭遇したらどう振る舞うか
ARROW試験のupdated data...RET肺がんとpralsetinib
EGFRエクソン20挿入変異に対するAmivantamab
CLIP1-LTK融合遺伝子の発見・・・LC-SCRUM Asiaから
セルペルカチニブ、2021年12月13日発売予定
セルペルカチニブと過敏症
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
脳転移を有する患者集団に対しても、免疫チェックポイント阻害薬は有効なのか
第4世代ALK阻害薬・・・TPX-0131とNVL-655
セルペルカチニブ、製造販売承認
ドライバー遺伝子変異陽性患者におけるPACIFICレジメンの有効性
HER2遺伝子変異陽性肺がんに対するtrastuzumab deruxtecan
オシメルチニブ耐性化後は、耐性機序同定や分子標的治療は意味がないのか
EGFR/ALK陽性非小細胞肺がんに対するカルボプラチン+ペメトレキセド+ペンブロリズマブ併用療法
ドライバー遺伝子異常検出におけるジレンマとmultiplex PCR
中国人患者におけるRET阻害薬(Selpercatinib, Pralsetinib)の有効性
オシメルチニブによる術前療法・・・NeoADAURAの前哨戦
BRAF遺伝子変異と縁がない
RET阻害薬、セルペルカチニブがやってくる
進行が速い進行肺腺がんに遭遇したらどう振る舞うか
ARROW試験のupdated data...RET肺がんとpralsetinib
EGFRエクソン20挿入変異に対するAmivantamab
この記事へのコメント
いつもブログを拝見しております。突然のコメント失礼致します。
NEJ026のプロトコルに関してですが、おそらくTKI単剤群の後治療にBevが含まれていたかと存じます。
どこかでBevの可能性を見つけたいということでしょうか。
NEJ026のプロトコルに関してですが、おそらくTKI単剤群の後治療にBevが含まれていたかと存じます。
どこかでBevの可能性を見つけたいということでしょうか。
Posted by 九州人 at 2018年10月28日 23:29








