2015年03月27日
抗腫瘍治療と肝機能障害
肝機能障害は、抗腫瘍治療をやっているとしばしばお目にかかります。
治療経過中に自然に軽快することもあれば、薬の減量や変更を余儀なくされることもあります。
EGFR阻害薬では、タルセバよりイレッサの方が肝機能障害が出やすい傾向にあるようです。
以下のような質問を頂きまして、いつものように歯切れ悪く回答しました。
誰かいい案をご存知でしたら教えてください。
**********************************************************************************
私の場合、肝臓値がすぐに悪化します(遺伝的に酒に弱く飲まない肝臓です)。
抗がん剤2サイクル目の直前の血液検査の結果は
GOT 68 (基準5-30)
GPT 89 (基準3-35)
αーGTP 42 (基準1-28)
でした。
主治医はこれでゴーサインを出したのですが、2回目、3回目と積み重なるにつれ当然悪化し、延期or中断するのではないかと、私は冷や冷やです。主治医に聞いても予防薬はないとのこと。一方で患者さんのブログを読んでいると中には「グリチロン」を予防的に飲んでいる方もいらっしゃるようです。
先生のブログを読んでも、吐き気の予防については、随分と学会で議論もあり、標準があるようですが、同じ副作用の肝臓値の悪化予防については特に議論はなく、標準のようなものはないのでしょうか。また、同じように骨髄抑制を予防するための標準のようなものはないのでしょうか。ノイトロジン、グランなどを飲んで(点滴して?)いらっしゃる方がいるようです。
効果がなくなって治療を変更するのはどうもしようがありませんが、予防できる手段のあるにもかかわらず、それをせずに副作用がために延期や中断、挙句の果て終了となるのは避けたいと思っています。もし、ご存じでしたら教えていただけますと幸いです。
**********************************************************************************
おっしゃる通り、抗腫瘍薬による肝機能障害が出現した際の対応に、予防的なものはなさそうです。
今日の外来に来られた私の患者さんも、治療中に軽度の肝機能障害が出たり消えたりしています。
一般的な考え方として、Grade2以上の肝機能障害が出現したら休薬し、Grade1以下になるのを待って再開、2週間以上Grade2以上の肝機能障害が続けば、治療休止もしくは治療変更を考えます。
肝機能障害出現後にウルソデオキシコール酸やグリチルリチン酸を服用するのも一案ですが、一般的な対応ではないと思います。
GOT、GPTは正常上限の3倍まで、GGTPは正常上限の2.5倍までがGrade1、Grade1以上5倍までがGrade2の有害事象とされていますから、担当の先生がゴーサインを出されたのは納得がいきます。
化学療法全体に言えることですが、そして、ある意味あなたを失望させる話かもしれませんが、「治癒を目指す」薬物療法を行う場合には、多少の困難や有害事象があっても、予定されたスケジュールで、予定された治療量の薬を使うこと、一方「延命や症状緩和を目指す」薬物療法を行う場合には、有害事象に遭遇した場合には休薬、投与量減量、ときには治療変更をすることが基本です。前者は、治療のために命を危険にさらしてでも、そこを凌いだ時には「治癒」が得られるかも知れない、その為なら命を危険にさらす価値がある、と考えます。後者では、一定期間の延命のための治療で命を危険にさらしたり、QoLを落とすわけにはいかない、と考えます。
話はかわります。
ノイトロジンやグラン、ノイアップといった白血球を増やす薬は、いわば「細胞増殖薬」ですよね。
白血球もがん細胞も、根元を辿っていくと起源は同じです。白血球を増やす薬は、がん細胞も増やしてしまいそうだなと思いませんか?
ですから、これらの薬の使い方はガイドラインで厳密に定義されています。
かつて、化学療法による貧血を是正するために赤血球の増殖因子を使うか使わないかの比較試験が行われましたが、使った方が予後不良でした。
ちょっと脱線してしまいましたが、肝機能障害を予防できる手段、私は残念ながら存じません。
ようやくB型肝炎ウイルスキャリアーの対策が整ったくらいです。
お役に立てなくて申し訳ありません。
ウルソデオキシコール酸やグリチルリチン酸に使用の可否について、担当の先生に相談してみられてはいかがでしょうか。
また、抗腫瘍薬の減量も、規定に従って考慮されるとよろしいかと思います。
治療経過中に自然に軽快することもあれば、薬の減量や変更を余儀なくされることもあります。
EGFR阻害薬では、タルセバよりイレッサの方が肝機能障害が出やすい傾向にあるようです。
以下のような質問を頂きまして、いつものように歯切れ悪く回答しました。
誰かいい案をご存知でしたら教えてください。
**********************************************************************************
私の場合、肝臓値がすぐに悪化します(遺伝的に酒に弱く飲まない肝臓です)。
抗がん剤2サイクル目の直前の血液検査の結果は
GOT 68 (基準5-30)
GPT 89 (基準3-35)
αーGTP 42 (基準1-28)
でした。
主治医はこれでゴーサインを出したのですが、2回目、3回目と積み重なるにつれ当然悪化し、延期or中断するのではないかと、私は冷や冷やです。主治医に聞いても予防薬はないとのこと。一方で患者さんのブログを読んでいると中には「グリチロン」を予防的に飲んでいる方もいらっしゃるようです。
先生のブログを読んでも、吐き気の予防については、随分と学会で議論もあり、標準があるようですが、同じ副作用の肝臓値の悪化予防については特に議論はなく、標準のようなものはないのでしょうか。また、同じように骨髄抑制を予防するための標準のようなものはないのでしょうか。ノイトロジン、グランなどを飲んで(点滴して?)いらっしゃる方がいるようです。
効果がなくなって治療を変更するのはどうもしようがありませんが、予防できる手段のあるにもかかわらず、それをせずに副作用がために延期や中断、挙句の果て終了となるのは避けたいと思っています。もし、ご存じでしたら教えていただけますと幸いです。
**********************************************************************************
おっしゃる通り、抗腫瘍薬による肝機能障害が出現した際の対応に、予防的なものはなさそうです。
今日の外来に来られた私の患者さんも、治療中に軽度の肝機能障害が出たり消えたりしています。
一般的な考え方として、Grade2以上の肝機能障害が出現したら休薬し、Grade1以下になるのを待って再開、2週間以上Grade2以上の肝機能障害が続けば、治療休止もしくは治療変更を考えます。
肝機能障害出現後にウルソデオキシコール酸やグリチルリチン酸を服用するのも一案ですが、一般的な対応ではないと思います。
GOT、GPTは正常上限の3倍まで、GGTPは正常上限の2.5倍までがGrade1、Grade1以上5倍までがGrade2の有害事象とされていますから、担当の先生がゴーサインを出されたのは納得がいきます。
化学療法全体に言えることですが、そして、ある意味あなたを失望させる話かもしれませんが、「治癒を目指す」薬物療法を行う場合には、多少の困難や有害事象があっても、予定されたスケジュールで、予定された治療量の薬を使うこと、一方「延命や症状緩和を目指す」薬物療法を行う場合には、有害事象に遭遇した場合には休薬、投与量減量、ときには治療変更をすることが基本です。前者は、治療のために命を危険にさらしてでも、そこを凌いだ時には「治癒」が得られるかも知れない、その為なら命を危険にさらす価値がある、と考えます。後者では、一定期間の延命のための治療で命を危険にさらしたり、QoLを落とすわけにはいかない、と考えます。
話はかわります。
ノイトロジンやグラン、ノイアップといった白血球を増やす薬は、いわば「細胞増殖薬」ですよね。
白血球もがん細胞も、根元を辿っていくと起源は同じです。白血球を増やす薬は、がん細胞も増やしてしまいそうだなと思いませんか?
ですから、これらの薬の使い方はガイドラインで厳密に定義されています。
かつて、化学療法による貧血を是正するために赤血球の増殖因子を使うか使わないかの比較試験が行われましたが、使った方が予後不良でした。
ちょっと脱線してしまいましたが、肝機能障害を予防できる手段、私は残念ながら存じません。
ようやくB型肝炎ウイルスキャリアーの対策が整ったくらいです。
お役に立てなくて申し訳ありません。
ウルソデオキシコール酸やグリチルリチン酸に使用の可否について、担当の先生に相談してみられてはいかがでしょうか。
また、抗腫瘍薬の減量も、規定に従って考慮されるとよろしいかと思います。
2015年03月24日
たばこの経済
2015年3月21日の日本経済新聞朝刊に、以下のような記事が載っていました。

これを見て少し思うところがあり、大学で学生講義に使っているスライドも一部織り交ぜながら記事を書きます。
よく知られているように、日本人の死亡数へもっとも高く寄与しているのは喫煙です。

喫煙は、心血管疾患、悪性新生物、糖尿病のいずれの発症にも寄与しています。
日本人の死因の一位が悪性新生物、二位が心血管疾患であることを思えば、喫煙がいかに大きな公衆衛生上の問題であるかわかります。

そんなわけで、喫煙に関する問題は社会でよく取り上げられます。
たばこ教育の浸透やたばこ値上げの効果のためか、我が国の成人喫煙割合、たばこ消費量は年々減少しています。

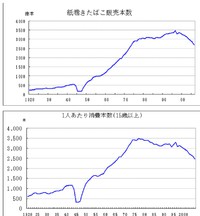
そのためか、主要先進国では、少なくとも男性の肺癌年齢調整死亡割合は年々減少の一途を辿っています。

ところで、我が国のたばこ消費量が減少する一方で、輸入たばこのシェアは年々上昇しています。

我が国同様、たばこ消費量が年々減少している欧米諸国から輸出されるたばこが我が国で消費され、欧米の外貨獲得に一役買い、日本国民の健康が蝕まれていることに、ずっと歯噛みする思いで過ごしてきました。
そこに持ってきて、今回の記事です。
日本たばこ産業も、欧米諸国のたばこ企業と同じことを、諸外国に対して行おうとしています。
記事の円グラフを見ると、日本国内でのJTのたばこの販売量は20%そこそこで、残り80%は海外に輸出されています。
それぞれの国の国民の健康を考えるとき、JTのこの姿勢が、諸外国からの攻撃対象にならないか心配です。

これを見て少し思うところがあり、大学で学生講義に使っているスライドも一部織り交ぜながら記事を書きます。
よく知られているように、日本人の死亡数へもっとも高く寄与しているのは喫煙です。

喫煙は、心血管疾患、悪性新生物、糖尿病のいずれの発症にも寄与しています。
日本人の死因の一位が悪性新生物、二位が心血管疾患であることを思えば、喫煙がいかに大きな公衆衛生上の問題であるかわかります。

そんなわけで、喫煙に関する問題は社会でよく取り上げられます。
たばこ教育の浸透やたばこ値上げの効果のためか、我が国の成人喫煙割合、たばこ消費量は年々減少しています。


そのためか、主要先進国では、少なくとも男性の肺癌年齢調整死亡割合は年々減少の一途を辿っています。

ところで、我が国のたばこ消費量が減少する一方で、輸入たばこのシェアは年々上昇しています。

我が国同様、たばこ消費量が年々減少している欧米諸国から輸出されるたばこが我が国で消費され、欧米の外貨獲得に一役買い、日本国民の健康が蝕まれていることに、ずっと歯噛みする思いで過ごしてきました。
そこに持ってきて、今回の記事です。
日本たばこ産業も、欧米諸国のたばこ企業と同じことを、諸外国に対して行おうとしています。
記事の円グラフを見ると、日本国内でのJTのたばこの販売量は20%そこそこで、残り80%は海外に輸出されています。
それぞれの国の国民の健康を考えるとき、JTのこの姿勢が、諸外国からの攻撃対象にならないか心配です。
2015年03月24日
間質性肺炎を合併した高齢者進行扁平上皮癌
間質性肺炎合併肺癌の抗がん薬治療。
大部分の間質性肺炎自体が難治なので、肺癌まで合併してしまうとどうもこうも行きません。
しばしば質問を受けて頭を抱えてしまいますが、今日も若手の先生から以下のような質問が舞い込みました。
*************************************************************************************
メールで失礼いたします。大変お久しぶりです。
ひとつ質問です。
76歳男性(PSは0)、COPD、塵肺(間質性肺炎あり)の扁平上皮癌cT2aN3M0 StageⅢB(右S6原発、N3は鎖骨下リンパ節)。
かかりつけ医からの紹介で大分市内の呼吸器内科、呼吸器外科へ行き、検査、治療しないほうがよいと言われてました。
今回たまたま肺炎で当院へ紹介となり、肺炎(肺炎球菌性肺炎)が改善したのち、気管支鏡を施行し、診断がつきました。
間質性肺炎があり化学療法は勧めなかったのですが、今後期待できる生存期間などを説明した後にどうしても治療してくれと言われました。
肺癌学会ガイドライン上では75歳以上、PS0、扁平上皮癌となると、ビノレルビン、ジェムシタビン、ドセタキセルとあります。
間質性肺炎合併なので、やるならビノレルビンといったところでしょうか。
製薬会社の方に相談したところ、タキサン系は間質性肺炎合併例にはすすめませんと言われました。
先生であれば、その他の薬剤も含めて、何を選択しますか。
ガイドライン上はカルボプラチン併用も考慮してよい(C1)ともあります。
しかし、自分の判断でプラチナは入れたくないなという感があります。
*************************************************************************************
というわけで、以下のごとく回答しました。
正しいかどうかは別として、あくまでも私なりの見解です。
*************************************************************************************
細かいことを考えずにEvidence Based Medicine(EBM)で判断すれば、75歳以上高齢者進行扁平上皮癌の1st line治療はドセタキセル単剤です。
我が国で行われたドセタキセルvsシスプラチン+ドセタキセル併用の第III相試験で、後者の優越性が証明されなかったからです。
2nd line以降はエビデンスがありませんので、勧める根拠自体がありません。
以上、終了。
・・・これじゃあ、先生も怒りますよね。
そんなわけで、少し過去の学会抄録等を調べてみました。
エビデンスレベルは低いかも知れませんが、この領域ではそんなこと言ってちゃ話が進みません。
1)2014年度 第55回日本肺癌学会総会 S4-5
・厚生労働省「びまん性肺疾患に関する調査研究班」実態調査。
・全国19施設より396症例の化学療法レジメンと急性増悪の有無について回答を得た。
・治療関連急性増悪と診断されたのが52例(13.1%)
・ビノレルビン、ドセタキセル使用時の急性増悪の頻度は比較的高め、イリノテカンやジェムシタビンはほとんど使われていない。
・使用実績、急性増悪の発症頻度および肺癌に対する有効性を考慮すると、カルボプラチン+パクリタキセル(急性増悪頻度12/146=8.6%)、プラチナ製剤+エトポシド併用療法(急性増悪頻度7/124=5.6%)が間質性肺炎合併肺癌の初回化学療法の有力な候補レジメンであ
る。
2)2014年度 第54回日本呼吸器学会総会 S6-4
・間質性肺炎に合併した肺癌の内科的治療と問題点
・日本医科大学呼吸器内科学分野では、特発性間質性肺炎合併の非小細胞肺癌ではカルボプラチン+パクリタキセル併用療法を、小細
胞癌ではカルボプラチン+エトポシド併用療法を施行。
・治療関連急性増悪の頻度は約6%で、全国平均の13.1%より低かった。
3)2014年度 第55回日本肺癌学会総会 O-50
・「抗がん剤レジメン毎の薬剤性肺障害頻度についてのレトロスペクティブスタディ」
・ドセタキセル、ペメトレキセド、ジェムシタビン、ビノレルビン、エルロチニブ、ゲフィチニブについて、倉敷中央病院呼吸器内科での薬剤性肺障害発症頻度を検討。
・ドセタキセル271人、ペメトレキセド249人、ジェムシタビン183人、ビノレルビン179人、エルロチニブ375人、ゲフィチニブ246人
・薬剤性肺障害発症頻度はドセタキセル7.0%、ペメトレキセド8.8%、ジェムシタビン4.3%、ビノレルビン1.6%、エルロチニブ1.5%、ゲフィチニブ2.8%だった。
・間質性肺炎合併は有意な薬剤性肺障害発症のリスクファクターで、治療ラインが進むほどに薬剤性肺障害発症リスクは有意に下がる傾向にあった。
・早期の治療ラインで使用されるドセタキセルやペメトレキセドでは、薬剤性肺障害発症頻度が高かった。
2012年ごろまで遡ってみましたが、これ以上役に立ちそうな内容は出てきませんでした。
僕なりにまとめると、
① とりあえず、間質性肺炎合併肺癌のレジメンとしては、カルボプラチン+パクリタキセル、カルボプラチン+エトポシドが無難と考えられている。
② イリノテカンやジェムシタビンは、初回治療としては避けた方がいい。
③ どの薬を使おうが、急性増悪は起こるときには起こる。
④ 様々なバイアスが割り込んでくるので、レトロスペクティブスタディにおける急性増悪の頻度を見ても、どの薬剤が本当にリスクが高いのかは判断できない。
ですから、リスクはどの薬もほぼ同じとみて、より効果が期待できる治療を選択するのが妥当ではないでしょうか。
僕ならキードラッグをドセタキセル、アブラキサン、S-1にします。
ドセタキセルなら単剤のみ、アブラキサンやS-1については、初回治療で用いるならカルボプラチンとの併用を考慮します。
繰り返すようですが、EBMとして推奨できるのはドセタキセル単剤療法のみです。
我が国の患者さんも参加したカルボプラチン+アブラキサンの臨床試験では年齢制限はなかったので、これも可でしょうか。
我が国で行われたカルボプラチン+S-1のLETS studyは、74歳以下が対象だったので、厳密に言えば今回の患者さんには適応できません。
ジェムシタビン単剤、ビノレルビン単剤は欧州で行われたELVIS, MILES studyを経て、欧州では高齢者の標準治療のひとつと考えられていますが、国内ではビノレルビンはドセタキセル単剤に劣ると結論されています。
以上、参考になれば幸いです。
最後にひとつ。
検査、治療はしない方がいいと説明した病院について、みなさんはどんな印象を持たれましたか。
治療はおろか、検査すらしないなんてひどい、という印象をお持ちになった方も少なからずいらっしゃるかもしれません。
しかし、診断がついたところで放射線治療も抗がん薬治療もできない、となれば、無用なリスクを患者さんに背負わせる検査すら勧められない、という医師の判断は、ちゃんとした説明をしているのなら、間違ってはいないのではないでしょうか。
このように、手術不能の間質性肺炎合併肺癌、もしくはハイリスク基礎疾患合併肺癌は、患者さん・ご家族と担当医の間にすれ違いや誤解を生じやすい、厄介な病態だと言えます。
大部分の間質性肺炎自体が難治なので、肺癌まで合併してしまうとどうもこうも行きません。
しばしば質問を受けて頭を抱えてしまいますが、今日も若手の先生から以下のような質問が舞い込みました。
*************************************************************************************
メールで失礼いたします。大変お久しぶりです。
ひとつ質問です。
76歳男性(PSは0)、COPD、塵肺(間質性肺炎あり)の扁平上皮癌cT2aN3M0 StageⅢB(右S6原発、N3は鎖骨下リンパ節)。
かかりつけ医からの紹介で大分市内の呼吸器内科、呼吸器外科へ行き、検査、治療しないほうがよいと言われてました。
今回たまたま肺炎で当院へ紹介となり、肺炎(肺炎球菌性肺炎)が改善したのち、気管支鏡を施行し、診断がつきました。
間質性肺炎があり化学療法は勧めなかったのですが、今後期待できる生存期間などを説明した後にどうしても治療してくれと言われました。
肺癌学会ガイドライン上では75歳以上、PS0、扁平上皮癌となると、ビノレルビン、ジェムシタビン、ドセタキセルとあります。
間質性肺炎合併なので、やるならビノレルビンといったところでしょうか。
製薬会社の方に相談したところ、タキサン系は間質性肺炎合併例にはすすめませんと言われました。
先生であれば、その他の薬剤も含めて、何を選択しますか。
ガイドライン上はカルボプラチン併用も考慮してよい(C1)ともあります。
しかし、自分の判断でプラチナは入れたくないなという感があります。
*************************************************************************************
というわけで、以下のごとく回答しました。
正しいかどうかは別として、あくまでも私なりの見解です。
*************************************************************************************
細かいことを考えずにEvidence Based Medicine(EBM)で判断すれば、75歳以上高齢者進行扁平上皮癌の1st line治療はドセタキセル単剤です。
我が国で行われたドセタキセルvsシスプラチン+ドセタキセル併用の第III相試験で、後者の優越性が証明されなかったからです。
2nd line以降はエビデンスがありませんので、勧める根拠自体がありません。
以上、終了。
・・・これじゃあ、先生も怒りますよね。
そんなわけで、少し過去の学会抄録等を調べてみました。
エビデンスレベルは低いかも知れませんが、この領域ではそんなこと言ってちゃ話が進みません。
1)2014年度 第55回日本肺癌学会総会 S4-5
・厚生労働省「びまん性肺疾患に関する調査研究班」実態調査。
・全国19施設より396症例の化学療法レジメンと急性増悪の有無について回答を得た。
・治療関連急性増悪と診断されたのが52例(13.1%)
・ビノレルビン、ドセタキセル使用時の急性増悪の頻度は比較的高め、イリノテカンやジェムシタビンはほとんど使われていない。
・使用実績、急性増悪の発症頻度および肺癌に対する有効性を考慮すると、カルボプラチン+パクリタキセル(急性増悪頻度12/146=8.6%)、プラチナ製剤+エトポシド併用療法(急性増悪頻度7/124=5.6%)が間質性肺炎合併肺癌の初回化学療法の有力な候補レジメンであ
る。
2)2014年度 第54回日本呼吸器学会総会 S6-4
・間質性肺炎に合併した肺癌の内科的治療と問題点
・日本医科大学呼吸器内科学分野では、特発性間質性肺炎合併の非小細胞肺癌ではカルボプラチン+パクリタキセル併用療法を、小細
胞癌ではカルボプラチン+エトポシド併用療法を施行。
・治療関連急性増悪の頻度は約6%で、全国平均の13.1%より低かった。
3)2014年度 第55回日本肺癌学会総会 O-50
・「抗がん剤レジメン毎の薬剤性肺障害頻度についてのレトロスペクティブスタディ」
・ドセタキセル、ペメトレキセド、ジェムシタビン、ビノレルビン、エルロチニブ、ゲフィチニブについて、倉敷中央病院呼吸器内科での薬剤性肺障害発症頻度を検討。
・ドセタキセル271人、ペメトレキセド249人、ジェムシタビン183人、ビノレルビン179人、エルロチニブ375人、ゲフィチニブ246人
・薬剤性肺障害発症頻度はドセタキセル7.0%、ペメトレキセド8.8%、ジェムシタビン4.3%、ビノレルビン1.6%、エルロチニブ1.5%、ゲフィチニブ2.8%だった。
・間質性肺炎合併は有意な薬剤性肺障害発症のリスクファクターで、治療ラインが進むほどに薬剤性肺障害発症リスクは有意に下がる傾向にあった。
・早期の治療ラインで使用されるドセタキセルやペメトレキセドでは、薬剤性肺障害発症頻度が高かった。
2012年ごろまで遡ってみましたが、これ以上役に立ちそうな内容は出てきませんでした。
僕なりにまとめると、
① とりあえず、間質性肺炎合併肺癌のレジメンとしては、カルボプラチン+パクリタキセル、カルボプラチン+エトポシドが無難と考えられている。
② イリノテカンやジェムシタビンは、初回治療としては避けた方がいい。
③ どの薬を使おうが、急性増悪は起こるときには起こる。
④ 様々なバイアスが割り込んでくるので、レトロスペクティブスタディにおける急性増悪の頻度を見ても、どの薬剤が本当にリスクが高いのかは判断できない。
ですから、リスクはどの薬もほぼ同じとみて、より効果が期待できる治療を選択するのが妥当ではないでしょうか。
僕ならキードラッグをドセタキセル、アブラキサン、S-1にします。
ドセタキセルなら単剤のみ、アブラキサンやS-1については、初回治療で用いるならカルボプラチンとの併用を考慮します。
繰り返すようですが、EBMとして推奨できるのはドセタキセル単剤療法のみです。
我が国の患者さんも参加したカルボプラチン+アブラキサンの臨床試験では年齢制限はなかったので、これも可でしょうか。
我が国で行われたカルボプラチン+S-1のLETS studyは、74歳以下が対象だったので、厳密に言えば今回の患者さんには適応できません。
ジェムシタビン単剤、ビノレルビン単剤は欧州で行われたELVIS, MILES studyを経て、欧州では高齢者の標準治療のひとつと考えられていますが、国内ではビノレルビンはドセタキセル単剤に劣ると結論されています。
以上、参考になれば幸いです。
最後にひとつ。
検査、治療はしない方がいいと説明した病院について、みなさんはどんな印象を持たれましたか。
治療はおろか、検査すらしないなんてひどい、という印象をお持ちになった方も少なからずいらっしゃるかもしれません。
しかし、診断がついたところで放射線治療も抗がん薬治療もできない、となれば、無用なリスクを患者さんに背負わせる検査すら勧められない、という医師の判断は、ちゃんとした説明をしているのなら、間違ってはいないのではないでしょうか。
このように、手術不能の間質性肺炎合併肺癌、もしくはハイリスク基礎疾患合併肺癌は、患者さん・ご家族と担当医の間にすれ違いや誤解を生じやすい、厄介な病態だと言えます。
2015年03月05日
来ました、ニボルマブ!
話題の免疫チェックポイント阻害薬のニボルマブ、ついに肺癌治療としても2015/3/4付でFDAに承認されました。
以下、米国臨床腫瘍学会の記事から引用します。
FDA Approves Nivolumab to Treat Squamous Non–Small Cell Lung Cancer
By The ASCO Post
Posted: 3/4/2015 3:50:05 PM
Last Updated: 3/4/2015 4:07:38 PM
米国食品医薬品局(FDA)は本日、PD-1阻害薬であるニボルマブ(商品名Opdivo)を、プラチナ併用化学療法後の進行肺扁平上皮癌患者の治療薬として承認した。ニボルマブはPD-1受容体に結合してPD-L1/PD-L2との相互作用を阻害するモノクローナル抗体で、これによりPD-1経路により阻害される免疫応答-これには抗腫瘍免疫応答が含まれるが-を促進させる。
今回の承認は、プラチナ併用化学療法中もしくはその後に病勢進行した、進行肺扁平上皮癌の患者272人を対象に、複数国および施設にまたがり行われた、オープンラベル無作為化臨床試験の結果に基づいている。ニボルマブ群(n=135人)は3mg/kgのニボルマブを2週間ごとに静脈内投与、ドセタキセル群(n=137人)は75mg/㎡のドセタキセルを3週間ごとに静脈内投与された。主要評価項目は全生存期間だった
。
予定されていた中間解析の段階で、ニボルマブはドセタキセルに対し、統計学的に有意に全生存期間を延長した。生存期間中央値はニボルマブ群で9.2ヶ月(95%信頼区間は7.3-13.3ヶ月)、ドセタキセル群で6ヶ月(95%信頼区間は5.1-7.3ヶ月)で、ハザード比は0.59、その95%信頼区間は0.44-0.79、p値=0.00025だった。
今回の承認はまた、プラチナ併用化学療法と、さらに少なくともあと1レジメンの化学療法を施行したのちに病勢進行した進行肺扁平上皮癌の患者を対象に、複数国および施設にまたがって行われたシングルアームの臨床試験結果にも基づいている。117人の患者が3mg/kgのニボルマブを2週間ごとに静脈内投与された。主要評価項目は奏効割合で、効果判定は独立した判定委員会でRESICT v1.1により行われた。奏効割合は15%(95%信頼区間は9%-22%)で、これらは全て部分奏効であった。解析時点で、部分奏効した17人中10人(59%)は6ヶ月以上にわたり部分奏効を維持していた。
ニボルマブの主要な有害事象は疲労、呼吸困難、筋肉痛、食欲不振、咳、嘔気、便秘だった。ほとんどの重篤な有害事象は肺・大腸・肝臓・腎臓・ホルモン産生器官等の健常臓器に対する強い免疫応答によるものだった。
8年前、私が修行先でまとめた論文の序文は、「腺癌と異なり、扁平上皮癌の領域では有効な分子標的薬や抗体医薬は皆無である」というくだりから始めました。
既にシスプラチン+ジェムシタビン+ネシツムマブ併用療法が肺扁平上皮癌の全生存期間をわずかながら延長することが報告されていますが、今回のニボルマブの報告は、有効性の差が出にくい二次治療以降で、しかも併用ではなく単剤療法で、肺扁平上皮癌にとっては唯一といってもいい標準治療のドセタキセルに対して圧倒的な優位性を示しています。
扁平上皮癌に対する個人的な思い入れもあり、興奮のあまり病院の仕事を後回しにして記事を書いてしまいました。
早く我が国でも承認されて、患者さんの手元に届きますように。
免疫チェックポイントの領域は非常に注目されており、昨年の肺癌学会総会に続き、この4月の内科学会総会でもこの領域の先駆者である本庶佑先生が特別講演をされる予定です。
前回のご講演は、基礎研究者の矜持と本懐を感じる味わい深いものでしたが、もう一度改めて拝聴しようと思っています。
以下、米国臨床腫瘍学会の記事から引用します。
FDA Approves Nivolumab to Treat Squamous Non–Small Cell Lung Cancer
By The ASCO Post
Posted: 3/4/2015 3:50:05 PM
Last Updated: 3/4/2015 4:07:38 PM
米国食品医薬品局(FDA)は本日、PD-1阻害薬であるニボルマブ(商品名Opdivo)を、プラチナ併用化学療法後の進行肺扁平上皮癌患者の治療薬として承認した。ニボルマブはPD-1受容体に結合してPD-L1/PD-L2との相互作用を阻害するモノクローナル抗体で、これによりPD-1経路により阻害される免疫応答-これには抗腫瘍免疫応答が含まれるが-を促進させる。
今回の承認は、プラチナ併用化学療法中もしくはその後に病勢進行した、進行肺扁平上皮癌の患者272人を対象に、複数国および施設にまたがり行われた、オープンラベル無作為化臨床試験の結果に基づいている。ニボルマブ群(n=135人)は3mg/kgのニボルマブを2週間ごとに静脈内投与、ドセタキセル群(n=137人)は75mg/㎡のドセタキセルを3週間ごとに静脈内投与された。主要評価項目は全生存期間だった
。
予定されていた中間解析の段階で、ニボルマブはドセタキセルに対し、統計学的に有意に全生存期間を延長した。生存期間中央値はニボルマブ群で9.2ヶ月(95%信頼区間は7.3-13.3ヶ月)、ドセタキセル群で6ヶ月(95%信頼区間は5.1-7.3ヶ月)で、ハザード比は0.59、その95%信頼区間は0.44-0.79、p値=0.00025だった。
今回の承認はまた、プラチナ併用化学療法と、さらに少なくともあと1レジメンの化学療法を施行したのちに病勢進行した進行肺扁平上皮癌の患者を対象に、複数国および施設にまたがって行われたシングルアームの臨床試験結果にも基づいている。117人の患者が3mg/kgのニボルマブを2週間ごとに静脈内投与された。主要評価項目は奏効割合で、効果判定は独立した判定委員会でRESICT v1.1により行われた。奏効割合は15%(95%信頼区間は9%-22%)で、これらは全て部分奏効であった。解析時点で、部分奏効した17人中10人(59%)は6ヶ月以上にわたり部分奏効を維持していた。
ニボルマブの主要な有害事象は疲労、呼吸困難、筋肉痛、食欲不振、咳、嘔気、便秘だった。ほとんどの重篤な有害事象は肺・大腸・肝臓・腎臓・ホルモン産生器官等の健常臓器に対する強い免疫応答によるものだった。
8年前、私が修行先でまとめた論文の序文は、「腺癌と異なり、扁平上皮癌の領域では有効な分子標的薬や抗体医薬は皆無である」というくだりから始めました。
既にシスプラチン+ジェムシタビン+ネシツムマブ併用療法が肺扁平上皮癌の全生存期間をわずかながら延長することが報告されていますが、今回のニボルマブの報告は、有効性の差が出にくい二次治療以降で、しかも併用ではなく単剤療法で、肺扁平上皮癌にとっては唯一といってもいい標準治療のドセタキセルに対して圧倒的な優位性を示しています。
扁平上皮癌に対する個人的な思い入れもあり、興奮のあまり病院の仕事を後回しにして記事を書いてしまいました。
早く我が国でも承認されて、患者さんの手元に届きますように。
免疫チェックポイントの領域は非常に注目されており、昨年の肺癌学会総会に続き、この4月の内科学会総会でもこの領域の先駆者である本庶佑先生が特別講演をされる予定です。
前回のご講演は、基礎研究者の矜持と本懐を感じる味わい深いものでしたが、もう一度改めて拝聴しようと思っています。
2015年03月03日
ALK陽性肺癌クリゾチニブ内服後の体幹部定位照射
少し前の話ですが、表題の内容について扱った論文、宿題にしたままでした。
以下の記事の末尾に記載しています。
http://oitahaiganpractice.junglekouen.com/e776971.html
本日、改めて取り扱います。
Stereotactic radiation therapy can safely and durably control sites of extra-central nervous system oligoprogressive disease in anaplastic lymphoma kinasepositive lung cancer patients receiving crizotinib.
Gan GN, Weickhardt AJ, Scheier B, et al
Int J Radiat Oncol Biol Phys 88:892-898, 2014
目的:ALK陽性非小細胞肺癌患者において、中枢神経外病変による病勢進行を来した際の局所放射線焼灼療法(radiotherapeutic local ablation therapy:LAT)の継続性と毒性について検討すること。
方法:クリゾチニブ内服中のALK陽性非小細胞肺癌患者で、4ヶ所以下の中枢神経外病変出現が明らかとなったものを少数転移進行(Oligoprogressive disease:OPD)と分類した。中枢神経外病変の進行がOPDの定義を超えるもの、もしくはその他の理由でLATの継続ができなくなるまではクリゾチニブ内服を継続した。
結果:38人の対象患者中、33人がクリゾチニブ内服中に病勢進行した。この中で、14人が中枢神経外病巣により進行し、LATに適するOPDと判定された。中枢神経外病変によるOPD患者は、1-3コースのLATを受けた。6ヶ月および12ヶ月の局所制御割合はそれぞれ100%、86%だった。単回照射等量が25Gy以上の群と25Gy未満の群では、12ヶ月の局所制御割合がそれぞれ100%、60%であった(p=0.01)。Grade 2以上の急性もしくは遅発性放射線毒性は認められなかった。LATが行えた患者群とLATの対象とならなかった患者群でクリゾチニブ内服継続期間を比較すると、前者が28ヶ月、後者が10.1ヶ月だった。12ヶ月以上クリゾチニブを服用できた群と12ヶ月以下しか服用できなかった群では、2年生存割合がそれぞれ72%と12%だった(p<.0001)。
結論:クリゾチニブ内服中のALK陽性非小細胞肺癌患者において、LATは個別の進行病巣を安全に、継続的に根絶させる。照射線量と照射局所の治療反応性には正の相関がみられた。クリゾチニブ服用中の患者において、LATによりOPDを制御することでクリゾチニブの服用期間を延長することができ、生存期間延長も関連して認められた。

beyond PD、メンテナンス療法の考え方にしてもそうですが、今回扱われた治療も、一旦治療効果が得られた薬をいかにして長く続けるか、という戦略のひとつのようです。
少数転移により病勢進行したのであれば、そこだけを放射線照射で叩いて、それ以外の部分は多分クリゾチニブで制御されているだろうから服薬を続けよう、と。
しかし、今回の解析は「たまたま少数転移により進行し、LATを受けられた患者さんたち」の生存期間が、「たまたま何らかの理由によりLATが受けられなかった患者さんたち」より長かった、ということを示しただけであり、LATそのものの有効性が確認されたかどうかはわかりません。
以下の記事の末尾に記載しています。
http://oitahaiganpractice.junglekouen.com/e776971.html
本日、改めて取り扱います。
Stereotactic radiation therapy can safely and durably control sites of extra-central nervous system oligoprogressive disease in anaplastic lymphoma kinasepositive lung cancer patients receiving crizotinib.
Gan GN, Weickhardt AJ, Scheier B, et al
Int J Radiat Oncol Biol Phys 88:892-898, 2014
目的:ALK陽性非小細胞肺癌患者において、中枢神経外病変による病勢進行を来した際の局所放射線焼灼療法(radiotherapeutic local ablation therapy:LAT)の継続性と毒性について検討すること。
方法:クリゾチニブ内服中のALK陽性非小細胞肺癌患者で、4ヶ所以下の中枢神経外病変出現が明らかとなったものを少数転移進行(Oligoprogressive disease:OPD)と分類した。中枢神経外病変の進行がOPDの定義を超えるもの、もしくはその他の理由でLATの継続ができなくなるまではクリゾチニブ内服を継続した。
結果:38人の対象患者中、33人がクリゾチニブ内服中に病勢進行した。この中で、14人が中枢神経外病巣により進行し、LATに適するOPDと判定された。中枢神経外病変によるOPD患者は、1-3コースのLATを受けた。6ヶ月および12ヶ月の局所制御割合はそれぞれ100%、86%だった。単回照射等量が25Gy以上の群と25Gy未満の群では、12ヶ月の局所制御割合がそれぞれ100%、60%であった(p=0.01)。Grade 2以上の急性もしくは遅発性放射線毒性は認められなかった。LATが行えた患者群とLATの対象とならなかった患者群でクリゾチニブ内服継続期間を比較すると、前者が28ヶ月、後者が10.1ヶ月だった。12ヶ月以上クリゾチニブを服用できた群と12ヶ月以下しか服用できなかった群では、2年生存割合がそれぞれ72%と12%だった(p<.0001)。
結論:クリゾチニブ内服中のALK陽性非小細胞肺癌患者において、LATは個別の進行病巣を安全に、継続的に根絶させる。照射線量と照射局所の治療反応性には正の相関がみられた。クリゾチニブ服用中の患者において、LATによりOPDを制御することでクリゾチニブの服用期間を延長することができ、生存期間延長も関連して認められた。

beyond PD、メンテナンス療法の考え方にしてもそうですが、今回扱われた治療も、一旦治療効果が得られた薬をいかにして長く続けるか、という戦略のひとつのようです。
少数転移により病勢進行したのであれば、そこだけを放射線照射で叩いて、それ以外の部分は多分クリゾチニブで制御されているだろうから服薬を続けよう、と。
しかし、今回の解析は「たまたま少数転移により進行し、LATを受けられた患者さんたち」の生存期間が、「たまたま何らかの理由によりLATが受けられなかった患者さんたち」より長かった、ということを示しただけであり、LATそのものの有効性が確認されたかどうかはわかりません。



