2014年10月20日
B型肝炎ウイルス対策
10年前に比べると、抗がん薬治療を始めるにあたって、準備しておかなければならないことが増えたような気がします。
抗がん薬を調整する際の安全キャビネットの設置や防護服しかり。
塩酸イリノテカンを使用する際のUGT1A1遺伝子多型検査しかり。
胃がん、乳がんの治療をする際のHER2検索しかり。
大腸がんの治療をする際のK-ras遺伝子変異検査しかり。
肺がんの治療をする際のEGFR遺伝子変異検査、ALK遺伝子再構成検査しかり。
ペメトレキセドを投与するにあたっての、1週間先行してのビタミンB12、葉酸投与もしかり。
そして、今回取り上げる、B型肝炎ウイルス対策もまたしかり、です。
B型肝炎ウイルスのスクリーニング検査として頻用されるHBs抗原検索では、その陽性例でステロイドの投与や化学療法により、B型肝炎ウイルスの急激な増殖(再活性化)が起こり、致死的な重症肝炎に至ることが報告されています。
HBs抗原陰性であっても、HBc抗体やHBs抗体が陽性の場合、肝臓や末梢血単核球中でB型肝炎ウイルスの複製が持続する場合があることも知られています。
そのため、「免疫抑制・化学療法により発症するB型肝炎対策ガイドライン」が公開され、現在は2011年版が最新版とされています。

実際にB型重症肝炎に至った経験があるかと言われればないのですが、C型肝炎ウイルスキャリアーの原発性腹膜腫瘍の患者さんが化学療法中に肝硬変に陥り、治療継続不可能になったのを目の当たりにしたことがあり、忘れられません。
今回、他院から引き継いだ患者さんを調べてみると、HBc抗体、HBs抗体が陽性でした。
ガイドラインに従って、B型肝炎ウイルスDNA定量を行い、適切に対処します。
抗がん薬を調整する際の安全キャビネットの設置や防護服しかり。
塩酸イリノテカンを使用する際のUGT1A1遺伝子多型検査しかり。
胃がん、乳がんの治療をする際のHER2検索しかり。
大腸がんの治療をする際のK-ras遺伝子変異検査しかり。
肺がんの治療をする際のEGFR遺伝子変異検査、ALK遺伝子再構成検査しかり。
ペメトレキセドを投与するにあたっての、1週間先行してのビタミンB12、葉酸投与もしかり。
そして、今回取り上げる、B型肝炎ウイルス対策もまたしかり、です。
B型肝炎ウイルスのスクリーニング検査として頻用されるHBs抗原検索では、その陽性例でステロイドの投与や化学療法により、B型肝炎ウイルスの急激な増殖(再活性化)が起こり、致死的な重症肝炎に至ることが報告されています。
HBs抗原陰性であっても、HBc抗体やHBs抗体が陽性の場合、肝臓や末梢血単核球中でB型肝炎ウイルスの複製が持続する場合があることも知られています。
そのため、「免疫抑制・化学療法により発症するB型肝炎対策ガイドライン」が公開され、現在は2011年版が最新版とされています。

実際にB型重症肝炎に至った経験があるかと言われればないのですが、C型肝炎ウイルスキャリアーの原発性腹膜腫瘍の患者さんが化学療法中に肝硬変に陥り、治療継続不可能になったのを目の当たりにしたことがあり、忘れられません。
今回、他院から引き継いだ患者さんを調べてみると、HBc抗体、HBs抗体が陽性でした。
ガイドラインに従って、B型肝炎ウイルスDNA定量を行い、適切に対処します。
2014年10月15日
シスプラチン+ペメトレキセド+丸山ワクチン併用療法
他院からの紹介で、原発性肺腺癌、EGFR遺伝子変異陰性、ALK遺伝子再構成陰性の方に対し、シスプラチン+ペメトレキセド+丸山ワクチン併用療法を行うことになりました。
丸山ワクチン投与は保険外診療ですから(現在は「治験」として取り扱われているようですが)、公的医療機関ではなかなか行い難い治療のようです。
私自身、丸山ワクチンの投与依頼を受けるのは初めてですし、どちらかというとその効果には懐疑的ですが、ご本人もご家族も丸山ワクチンの使用を強く希望されており、丸山ワクチンを規定通り使うために、ということでわざわざ化学療法目的で入院していた紹介元を1日で退院して、私のもとに来られました。
おそらくお断りすると他に引き受けてくれる医療機関はなさそうだなと感じたので、お引き受けすることにしました。
賛否両論さまざまある治療だと思いますが、貴重な体験だと思って取り組んでみます。
折を見て、その後の経過を報告します。
丸山ワクチン投与は保険外診療ですから(現在は「治験」として取り扱われているようですが)、公的医療機関ではなかなか行い難い治療のようです。
私自身、丸山ワクチンの投与依頼を受けるのは初めてですし、どちらかというとその効果には懐疑的ですが、ご本人もご家族も丸山ワクチンの使用を強く希望されており、丸山ワクチンを規定通り使うために、ということでわざわざ化学療法目的で入院していた紹介元を1日で退院して、私のもとに来られました。
おそらくお断りすると他に引き受けてくれる医療機関はなさそうだなと感じたので、お引き受けすることにしました。
賛否両論さまざまある治療だと思いますが、貴重な体験だと思って取り組んでみます。
折を見て、その後の経過を報告します。
2014年10月15日
質疑応答
「ハイリスクな気管支鏡検査」の項に対して以下のコメントを頂きました。
ちょっと内容が長くなったので、項目を設けて記載することにしました。
ご参考になれば幸いです。
***********************************************************************************
不勉強なのですが、教えてください。
気管支鏡検査以外に、CTガイド針生検があると思います。
気胸リスクはあるとして、針生検のほうが患者に優しいように思います。
どのような使い分けになるのでしょうか?
AURA試験の適用判断の為の細胞採取は針生検で行いました(肺門付近の原発)。
因みに治験状況は今4クール目で、3クール後のCEAは治験前86→16です(そろそろ下げ止まりになりそうです)。
2クール後のCTでは、腫瘍縮小が認められました。脳転移は治験前でもタルセバが効いてくれて、ほとんど指摘できない位だったのを維持しています。
骨転移にも効いているようです。
長く付き合うことができるように祈る毎日です。
すいません、もう1つ
遺伝子検査の結果、分子標的薬が使え、奏効が期待できる場合、分子標的薬で転移巣を潰してから、放射線というシナリオも有りかと思います。
それよりも間質性肺炎リスクから分子標的薬→放射線は常識外れでしょうか?
素人故、おかしな考えかもしれませんが、よかったらご意見ください。
Posted by のぞみパパ
***********************************************************************************
ちょっと解説を加えますと、「AURA試験」というのは、EGFRチロシンキナーゼ阻害薬に耐性となった患者さんにも効果が期待できる第3世代のEGFRチロシンキナーゼ阻害薬、AZD9291に関する臨床試験のことです。
試験のプロトコールの詳細は存じませんが、腫瘍再生検のサンプルを治療開始前に採取することが求められているのでしょうね。
8月29日の記事で少し詳しく触れているので、興味のある方は以下をご参照ください。
http://oitahaiganpractice.junglekouen.com/e751093.html
さて、回答です。
のぞみパパさんへ
ご連絡ありがとうございます。
1)CTガイド下針生検について
私が修行に行った病院では本検査が盛んに行われていて、大分に帰ってきたらどんどんやろうと思っていましたが、以下の理由で第一選択としていません。
・合併症の頻度が高い。
検査手技自体は患者さんにやさしい(寝転んで、局所麻酔を受けて、針を刺されるだけ)ですが、医原性気胸の確率は約50%、その他にも出血、空気塞栓、肋間神経損傷、肋間動静脈損傷、そして医原性胸膜播種のリスクがあります。気胸はほとんどの場合経過観察で改善しますし、出血は軽度で収まることが多いし、空気塞栓や肋間神経・動静脈損傷は見たことがありません。しかし、胸膜播種に関しては周囲の医師からしばしば経験談を耳にしますし、私がお世話になっておる呼吸器外科の先生はことあるごとに本検査を忌避する発言をされています(本検査による胸膜播種を経験した苦い経験があられるそうです)。
・検査そのものへのアクセスが悪い
CTガイド下生検を担当するのは放射線科の医師であることが多いです。呼吸器科からCTガイド下針生検依頼ということでコンサルテーションを行い、放射線科医のスケジュール、検査室のスケジュールに合わせて予定が組まれ・・・ということで、往々にして結果が出るまでにかなりのタイムラグを要します。
・腫瘍の部位による
一般に、針生検の適応は末梢発生の腫瘍であり、肺門周囲は気管支鏡で到達可能ならば気管支鏡で行うのが一般的だと思います。誤って大血管を穿刺してしまうリスクは無視できません。
ちなみに、今回の患者さんは肺門とも末梢とも言えない、ちょうど中間領域あたりに原発巣がありました。
CTガイド下針生検の診断率は90%を超えるとされていますので、メリットとデメリットを担当医がどう見積もるか、各施設での気管支鏡実績と照らし合わせて、どちらがより妥当か、という判断になるでしょう。
分子標的薬の適応判断に関する遺伝子変異情報の重要性は、今後ますます高まるでしょう。
根治不能の患者さんでも、病理診断と遺伝子変異検索を確実に行うために、生検目的の手術を行うことが今後増えるかもしれません。
先日相談を受けた患者さんでは、そういった選択がされていました。
2)分子標的薬で遠隔転移巣のコントロールをしてから、原発巣ほかへの放射線治療を併用する
考え方としてはありかもしれません。
私の患者さんで、前医で局所進行原発性肺腺癌、cT3N3M0, stage IIIB、照射対象範囲が広く、根治的放射線照射適応なし、ということで紹介された方がいました。
当時盛んに行われていたシスプラチン+ジェムシタビン併用療法を2コース行うも、毒性は高度、効果は得られず、の状態でした。
紹介元から肺生検のサンプルを取り寄せ、EGFR遺伝子変異検索を行ったところ、Exon 19 deletionが認められました。
その後、gefitinib投与により腫瘍の縮小が得られ、照射対象範囲が狭まり、gefitinibを一旦休薬したうえで、残存病巣に対して根治的照射を行いました。
照射が終わり、放射線肺臓炎がひと段落してからgefitinibを再開しましたが、結果的にはがん性胸膜炎や多発肝転移、がん性腹膜炎で病巣が進行しました。
pemetrexed, erlotinib, docetaxel等である程度の病勢コントロールは得られましたが、最終的には第2世代や第3世代の薬の登場に間に合わずに息を引き取りました。
しかし、上記の治療により延命が得られたことは明らかで、診断から5年を超えて生存されました。
では、のぞみパパさんがおっしゃるように、遠隔転移の制御が得られた場合にはどうか、と言われると、悩みます。
最近、進展型小細胞がんでは、化学療法による効果が得られたのちに放射線照射を行うと予後が伸びる、という報告がありました。
非小細胞肺がんでも、分子標的薬で高い治療効果が得られた場合にはそんな現象が起こりうるかもしれません。
ただし、おそらく治癒というところまではいかないでしょうし、延命目的で行うにしてもまずは臨床試験の枠組みの中で取り組むべき課題です。
さらには、放射線照射ではなく、腫瘍量減量のために原発巣や粗大病巣を切除する、という方法も考えられます。
原発性腹膜腫瘍/卵巣腫瘍、睾丸発生の胚細胞腫瘍、腎細胞癌などは、遠隔転移があっても原発巣を切除するのが標準治療です。
また、大腸癌などでは、切除可能な限りは(肝転移をはじめとした)遠隔転移巣を切除するのがやはり標準治療とされています。
肺癌においても、こうした方法論はあっていいと思います。
gefitinib投与で病巣が縮小し、その後根治切除を行った局所進行肺がんの患者さんを2例知っていますが、2例ともに脳転移で再発されました。
局所進行の患者さんでもそんな感じですから、IV期の患者さんで行うにしても、あくまで根治ではなく、延命目的ということに留まるでしょう。
肺がんを含め、悪性新生物一般の新規治療の発展スピードは本当に目覚ましく、治癒が得られなくても、少しでも長生きするための努力をすると、新しい治療に出会えるチャンスが増えます。
ですから、たとえ進行期の患者さんであっても、手術や放射線の果たす役割は今後ますます大きくなっていくでしょうね。
ただし、これを臨床試験として行って、効果を証明するのは困難を極めるかもしれません。
長文失礼いたしました。
ちょっと内容が長くなったので、項目を設けて記載することにしました。
ご参考になれば幸いです。
***********************************************************************************
不勉強なのですが、教えてください。
気管支鏡検査以外に、CTガイド針生検があると思います。
気胸リスクはあるとして、針生検のほうが患者に優しいように思います。
どのような使い分けになるのでしょうか?
AURA試験の適用判断の為の細胞採取は針生検で行いました(肺門付近の原発)。
因みに治験状況は今4クール目で、3クール後のCEAは治験前86→16です(そろそろ下げ止まりになりそうです)。
2クール後のCTでは、腫瘍縮小が認められました。脳転移は治験前でもタルセバが効いてくれて、ほとんど指摘できない位だったのを維持しています。
骨転移にも効いているようです。
長く付き合うことができるように祈る毎日です。
すいません、もう1つ
遺伝子検査の結果、分子標的薬が使え、奏効が期待できる場合、分子標的薬で転移巣を潰してから、放射線というシナリオも有りかと思います。
それよりも間質性肺炎リスクから分子標的薬→放射線は常識外れでしょうか?
素人故、おかしな考えかもしれませんが、よかったらご意見ください。
Posted by のぞみパパ
***********************************************************************************
ちょっと解説を加えますと、「AURA試験」というのは、EGFRチロシンキナーゼ阻害薬に耐性となった患者さんにも効果が期待できる第3世代のEGFRチロシンキナーゼ阻害薬、AZD9291に関する臨床試験のことです。
試験のプロトコールの詳細は存じませんが、腫瘍再生検のサンプルを治療開始前に採取することが求められているのでしょうね。
8月29日の記事で少し詳しく触れているので、興味のある方は以下をご参照ください。
http://oitahaiganpractice.junglekouen.com/e751093.html
さて、回答です。
のぞみパパさんへ
ご連絡ありがとうございます。
1)CTガイド下針生検について
私が修行に行った病院では本検査が盛んに行われていて、大分に帰ってきたらどんどんやろうと思っていましたが、以下の理由で第一選択としていません。
・合併症の頻度が高い。
検査手技自体は患者さんにやさしい(寝転んで、局所麻酔を受けて、針を刺されるだけ)ですが、医原性気胸の確率は約50%、その他にも出血、空気塞栓、肋間神経損傷、肋間動静脈損傷、そして医原性胸膜播種のリスクがあります。気胸はほとんどの場合経過観察で改善しますし、出血は軽度で収まることが多いし、空気塞栓や肋間神経・動静脈損傷は見たことがありません。しかし、胸膜播種に関しては周囲の医師からしばしば経験談を耳にしますし、私がお世話になっておる呼吸器外科の先生はことあるごとに本検査を忌避する発言をされています(本検査による胸膜播種を経験した苦い経験があられるそうです)。
・検査そのものへのアクセスが悪い
CTガイド下生検を担当するのは放射線科の医師であることが多いです。呼吸器科からCTガイド下針生検依頼ということでコンサルテーションを行い、放射線科医のスケジュール、検査室のスケジュールに合わせて予定が組まれ・・・ということで、往々にして結果が出るまでにかなりのタイムラグを要します。
・腫瘍の部位による
一般に、針生検の適応は末梢発生の腫瘍であり、肺門周囲は気管支鏡で到達可能ならば気管支鏡で行うのが一般的だと思います。誤って大血管を穿刺してしまうリスクは無視できません。
ちなみに、今回の患者さんは肺門とも末梢とも言えない、ちょうど中間領域あたりに原発巣がありました。
CTガイド下針生検の診断率は90%を超えるとされていますので、メリットとデメリットを担当医がどう見積もるか、各施設での気管支鏡実績と照らし合わせて、どちらがより妥当か、という判断になるでしょう。
分子標的薬の適応判断に関する遺伝子変異情報の重要性は、今後ますます高まるでしょう。
根治不能の患者さんでも、病理診断と遺伝子変異検索を確実に行うために、生検目的の手術を行うことが今後増えるかもしれません。
先日相談を受けた患者さんでは、そういった選択がされていました。
2)分子標的薬で遠隔転移巣のコントロールをしてから、原発巣ほかへの放射線治療を併用する
考え方としてはありかもしれません。
私の患者さんで、前医で局所進行原発性肺腺癌、cT3N3M0, stage IIIB、照射対象範囲が広く、根治的放射線照射適応なし、ということで紹介された方がいました。
当時盛んに行われていたシスプラチン+ジェムシタビン併用療法を2コース行うも、毒性は高度、効果は得られず、の状態でした。
紹介元から肺生検のサンプルを取り寄せ、EGFR遺伝子変異検索を行ったところ、Exon 19 deletionが認められました。
その後、gefitinib投与により腫瘍の縮小が得られ、照射対象範囲が狭まり、gefitinibを一旦休薬したうえで、残存病巣に対して根治的照射を行いました。
照射が終わり、放射線肺臓炎がひと段落してからgefitinibを再開しましたが、結果的にはがん性胸膜炎や多発肝転移、がん性腹膜炎で病巣が進行しました。
pemetrexed, erlotinib, docetaxel等である程度の病勢コントロールは得られましたが、最終的には第2世代や第3世代の薬の登場に間に合わずに息を引き取りました。
しかし、上記の治療により延命が得られたことは明らかで、診断から5年を超えて生存されました。
では、のぞみパパさんがおっしゃるように、遠隔転移の制御が得られた場合にはどうか、と言われると、悩みます。
最近、進展型小細胞がんでは、化学療法による効果が得られたのちに放射線照射を行うと予後が伸びる、という報告がありました。
非小細胞肺がんでも、分子標的薬で高い治療効果が得られた場合にはそんな現象が起こりうるかもしれません。
ただし、おそらく治癒というところまではいかないでしょうし、延命目的で行うにしてもまずは臨床試験の枠組みの中で取り組むべき課題です。
さらには、放射線照射ではなく、腫瘍量減量のために原発巣や粗大病巣を切除する、という方法も考えられます。
原発性腹膜腫瘍/卵巣腫瘍、睾丸発生の胚細胞腫瘍、腎細胞癌などは、遠隔転移があっても原発巣を切除するのが標準治療です。
また、大腸癌などでは、切除可能な限りは(肝転移をはじめとした)遠隔転移巣を切除するのがやはり標準治療とされています。
肺癌においても、こうした方法論はあっていいと思います。
gefitinib投与で病巣が縮小し、その後根治切除を行った局所進行肺がんの患者さんを2例知っていますが、2例ともに脳転移で再発されました。
局所進行の患者さんでもそんな感じですから、IV期の患者さんで行うにしても、あくまで根治ではなく、延命目的ということに留まるでしょう。
肺がんを含め、悪性新生物一般の新規治療の発展スピードは本当に目覚ましく、治癒が得られなくても、少しでも長生きするための努力をすると、新しい治療に出会えるチャンスが増えます。
ですから、たとえ進行期の患者さんであっても、手術や放射線の果たす役割は今後ますます大きくなっていくでしょうね。
ただし、これを臨床試験として行って、効果を証明するのは困難を極めるかもしれません。
長文失礼いたしました。
2014年10月13日
ハイリスクな気管支鏡検査
みなさんは、村上龍さんの「13歳のハローワーク」という本を知っていますか?
子供たちが、大人になって就きたい仕事の道しるべにすることを目的に、こんなことが得意ならこんな職業をめざすといいんじゃないかな、という感じで様々な職業が紹介された本です。
結構厚い本で、紹介されている職業も多岐にわたり、ときどき開いて拾い読みしています。
医療系についても少なからずページが割かれていますが、その中に東京大学の上昌広先生の文章がありました。
我が国の医療は既に崩壊しているが、これは国の医療費削減政策による地方での医師不足や行き過ぎた医療訴訟による医師の萎縮が関わっている、等々が記載されています。
小松秀樹先生の著書、「医療崩壊-立ち去り型サボタージュとは何か」を思い出します。
実際のところ、我々も気管支鏡検査を行うにあたり、出血などの合併症で患者さんの命が危険にさらされる可能性を考えると、身がすくみます。
腫瘍内科という「文化」ができて、呼吸器内科医が肺がんの治療に携わらなくなり、ハイリスクな患者さんの肺がん診断のための気管支鏡検査については、いよいよ身の回りの呼吸器内科医も萎縮しつつあるような気がします。
最近、こんなことがありました。
80歳を超えた女性。
虚血性心疾患、慢性腎臓病があり、強力な抗血小板薬を心筋梗塞の予防のために常時服用しています。
かかりつけの先生から、レントゲンとCTを肺癌の疑いがあるといわれ、近くの基幹病院を受診しました。
CTを確認すると、大きさ25mm程度の主病巣のほかに、同側の他の肺葉にも数か所、数mm大の粒状影を認めます。
PET-CTで異常集積を認めた部位は、主病巣だけでした。
基幹病院で担当した医師は、原発性肺がんで、他の肺葉への肺内転移を伴うstage IIIBの可能性が高いけれど、気管支鏡検査を行うこと自体がハイリスクだと判断しました。
合併症のためにいわゆる抗がん薬治療は困難で、分子標的治療を行うにも遺伝子変異の検索もできず、無治療経過観察を勧めて、紹介元に送り返した模様です。
肺がんの可能性が高いのに経過観察を勧められて納得できないご家族は、隣県の重粒子線治療施設に相談に行きました。
肺内転移を有することから重粒子線治療は適応外で、もとの病院で気管支鏡検査をしてもらうといいでしょう、と返事をされたそうです。
おそらく重粒子線治療施設の放射線治療医の先生は、この患者さんに気管支鏡検査を行うことのリスク評価など全く考慮していないはずですが、その説明を受けたご家族が基幹病院の先生のところに結果を話しに行って、ややこしいことになります。
「先生は気管支鏡検査はハイリスクでできないとおっしゃいましたが、セカンドオピニオン目的で受診した重粒子線治療施設の先生は、このお返事にもあるように気管支鏡検査を受けることを勧めていますよ。」
となるわけです。
基幹病院の先生も熟慮の末に気管支鏡の適応なしと判断されており、その決定は覆らず、結果としてその後の対応は誰が責任を持つかを含めて、宙に浮いてしまいました。
このブログをご覧になったご家族が、本ブログ上で私に連絡を下さり、相談にお越しになりました。
幸い、もともとのかかりつけの先生、基幹病院で担当された先生、いずれにもなんとなくつながりがあり、諸々のいきさつを整理した上で、プランを提示しました。
本人、ご家族にも十分に検査のリスクをご理解いただいた上で、場合によっては検査によって命が危険にさらされることもご承知いただいた上で、最善の方法を選びましょう、ということになりました。
結局準備万端整えた上で気管支鏡検査を行いました。
検査中は心拍数が40-50回/分と徐脈になり、かなりひやひやしましたが、どうにか無事に検査を終えることができました。
私自身、過去に一度だけ、肺がん診断目的の気管支鏡検査で患者さんを亡くしたことがあります。
やはり80歳代の男性、直近1ヶ月の間に2回の脳梗塞を繰り返して前医入院中でしたが、胸部CTで肺結節影とリンパ節腫大を指摘され、私の勤務先を紹介受診されました。
今回の患者さんと同様に心臓の合併症もあり、一側総頚動脈の閉塞と対側の高度狭窄というとてもハイリスクな状況で、さらにはご本人があまり病状や検査の意義を理解されておらず、むしろ気管支鏡検査はお勧めしがたい状況でした。
しかし、息子さんがとても診断に熱意を持っていて、どうなってもいいから診断してやってほしい、分子標的薬の適応がないかどうか調べてやってほしいと懇願されました。
神経内科医に意見を求め、直近の脳梗塞発症から3週間以上経過していれば、気管支鏡検査もできないことはないだろうとの回答を得て、準備万端整えて検査に臨みました。
もちろん、検査中の脳梗塞再発その他の合併症リスクは十二分に説明したうえで臨みました。
その結果どうなったかといえば、肺腺癌・EGFR遺伝子変異陰性の診断がついたものの、患者さんは両側総頚動脈閉塞で重篤な脳梗塞の状態に陥り、検査中に意識を失ったまま2日後に息を引き取られました。
やむを得ない出来事だったと今でも後悔はしていませんが、検査や治療の適応判断をする上での大切な教訓にしており、ハイリスクな患者さんやご家族には悲しい反省すべき実例としてしばしばお話しています。
だからこそ、一度やると決めたからには、目的を達するために虎穴に入らねばなりません。
今回の検査中、幸いにも病巣を捉えることができました。
若手の医師は、
「ハイリスク患者ですし、ブラシ細胞診だけでいいですよね」
と考えを述べましたが、それを聞いた私は、
「診断後に診療するのは多分俺だから、何が何でも組織をとってEGFRもALKも検索する、君たちができるところまでやってくれたらあとはこっちで引き継ぐ。GS生検に加えて、通常鉗子でも生検するつもりだから、できるところまで検査したら教えて」
と答えました。
ブラシ細胞診だけでは、仮に肺がんの診断がついたとしても、組織型の特定に至らない場合もありますし、ブラシ洗浄液が細胞診陽性にならない限りはEGFR遺伝子変異検索ができません。
そもそもALK遺伝子再構成の検索はできません。
EBUS-GSで組織を得たとしても組織片のサイズが小さく、ALK検索に供せるかどうかが未知数です。
これも実際のところ、EBUS-GSで提出した組織は、微小なため組織診断不能、と判定されることがしばしばです。
診断がつかなかったのでもう一度気管支鏡をさせてください、とは言えない今回のケースだからこそ、通常鉗子で十分な大きさの組織片を採取することにこだわりました。
若手の医師は気を悪くしたかもしれませんが、肺がん治療医としての意気込みというか、覚悟みたいなものを、今回の検査で感じ取ってもらえればいいのですが。
実際に肺がんの診断がついたら、今回の患者さんは一度は根治的定位放射線照射の適応がないかどうか、放射線治療医に相談してみたいと思っています。
同側他葉に2-3か所しかない微小病変だけのために、根治療法の道を閉ざしてしまうのは、あまりにももったいない気がします。
薬物療法をするかしないかは、それから考えても遅くないはずです。
子供たちが、大人になって就きたい仕事の道しるべにすることを目的に、こんなことが得意ならこんな職業をめざすといいんじゃないかな、という感じで様々な職業が紹介された本です。
結構厚い本で、紹介されている職業も多岐にわたり、ときどき開いて拾い読みしています。
医療系についても少なからずページが割かれていますが、その中に東京大学の上昌広先生の文章がありました。
我が国の医療は既に崩壊しているが、これは国の医療費削減政策による地方での医師不足や行き過ぎた医療訴訟による医師の萎縮が関わっている、等々が記載されています。
小松秀樹先生の著書、「医療崩壊-立ち去り型サボタージュとは何か」を思い出します。
実際のところ、我々も気管支鏡検査を行うにあたり、出血などの合併症で患者さんの命が危険にさらされる可能性を考えると、身がすくみます。
腫瘍内科という「文化」ができて、呼吸器内科医が肺がんの治療に携わらなくなり、ハイリスクな患者さんの肺がん診断のための気管支鏡検査については、いよいよ身の回りの呼吸器内科医も萎縮しつつあるような気がします。
最近、こんなことがありました。
80歳を超えた女性。
虚血性心疾患、慢性腎臓病があり、強力な抗血小板薬を心筋梗塞の予防のために常時服用しています。
かかりつけの先生から、レントゲンとCTを肺癌の疑いがあるといわれ、近くの基幹病院を受診しました。
CTを確認すると、大きさ25mm程度の主病巣のほかに、同側の他の肺葉にも数か所、数mm大の粒状影を認めます。
PET-CTで異常集積を認めた部位は、主病巣だけでした。
基幹病院で担当した医師は、原発性肺がんで、他の肺葉への肺内転移を伴うstage IIIBの可能性が高いけれど、気管支鏡検査を行うこと自体がハイリスクだと判断しました。
合併症のためにいわゆる抗がん薬治療は困難で、分子標的治療を行うにも遺伝子変異の検索もできず、無治療経過観察を勧めて、紹介元に送り返した模様です。
肺がんの可能性が高いのに経過観察を勧められて納得できないご家族は、隣県の重粒子線治療施設に相談に行きました。
肺内転移を有することから重粒子線治療は適応外で、もとの病院で気管支鏡検査をしてもらうといいでしょう、と返事をされたそうです。
おそらく重粒子線治療施設の放射線治療医の先生は、この患者さんに気管支鏡検査を行うことのリスク評価など全く考慮していないはずですが、その説明を受けたご家族が基幹病院の先生のところに結果を話しに行って、ややこしいことになります。
「先生は気管支鏡検査はハイリスクでできないとおっしゃいましたが、セカンドオピニオン目的で受診した重粒子線治療施設の先生は、このお返事にもあるように気管支鏡検査を受けることを勧めていますよ。」
となるわけです。
基幹病院の先生も熟慮の末に気管支鏡の適応なしと判断されており、その決定は覆らず、結果としてその後の対応は誰が責任を持つかを含めて、宙に浮いてしまいました。
このブログをご覧になったご家族が、本ブログ上で私に連絡を下さり、相談にお越しになりました。
幸い、もともとのかかりつけの先生、基幹病院で担当された先生、いずれにもなんとなくつながりがあり、諸々のいきさつを整理した上で、プランを提示しました。
本人、ご家族にも十分に検査のリスクをご理解いただいた上で、場合によっては検査によって命が危険にさらされることもご承知いただいた上で、最善の方法を選びましょう、ということになりました。
結局準備万端整えた上で気管支鏡検査を行いました。
検査中は心拍数が40-50回/分と徐脈になり、かなりひやひやしましたが、どうにか無事に検査を終えることができました。
私自身、過去に一度だけ、肺がん診断目的の気管支鏡検査で患者さんを亡くしたことがあります。
やはり80歳代の男性、直近1ヶ月の間に2回の脳梗塞を繰り返して前医入院中でしたが、胸部CTで肺結節影とリンパ節腫大を指摘され、私の勤務先を紹介受診されました。
今回の患者さんと同様に心臓の合併症もあり、一側総頚動脈の閉塞と対側の高度狭窄というとてもハイリスクな状況で、さらにはご本人があまり病状や検査の意義を理解されておらず、むしろ気管支鏡検査はお勧めしがたい状況でした。
しかし、息子さんがとても診断に熱意を持っていて、どうなってもいいから診断してやってほしい、分子標的薬の適応がないかどうか調べてやってほしいと懇願されました。
神経内科医に意見を求め、直近の脳梗塞発症から3週間以上経過していれば、気管支鏡検査もできないことはないだろうとの回答を得て、準備万端整えて検査に臨みました。
もちろん、検査中の脳梗塞再発その他の合併症リスクは十二分に説明したうえで臨みました。
その結果どうなったかといえば、肺腺癌・EGFR遺伝子変異陰性の診断がついたものの、患者さんは両側総頚動脈閉塞で重篤な脳梗塞の状態に陥り、検査中に意識を失ったまま2日後に息を引き取られました。
やむを得ない出来事だったと今でも後悔はしていませんが、検査や治療の適応判断をする上での大切な教訓にしており、ハイリスクな患者さんやご家族には悲しい反省すべき実例としてしばしばお話しています。
だからこそ、一度やると決めたからには、目的を達するために虎穴に入らねばなりません。
今回の検査中、幸いにも病巣を捉えることができました。
若手の医師は、
「ハイリスク患者ですし、ブラシ細胞診だけでいいですよね」
と考えを述べましたが、それを聞いた私は、
「診断後に診療するのは多分俺だから、何が何でも組織をとってEGFRもALKも検索する、君たちができるところまでやってくれたらあとはこっちで引き継ぐ。GS生検に加えて、通常鉗子でも生検するつもりだから、できるところまで検査したら教えて」
と答えました。
ブラシ細胞診だけでは、仮に肺がんの診断がついたとしても、組織型の特定に至らない場合もありますし、ブラシ洗浄液が細胞診陽性にならない限りはEGFR遺伝子変異検索ができません。
そもそもALK遺伝子再構成の検索はできません。
EBUS-GSで組織を得たとしても組織片のサイズが小さく、ALK検索に供せるかどうかが未知数です。
これも実際のところ、EBUS-GSで提出した組織は、微小なため組織診断不能、と判定されることがしばしばです。
診断がつかなかったのでもう一度気管支鏡をさせてください、とは言えない今回のケースだからこそ、通常鉗子で十分な大きさの組織片を採取することにこだわりました。
若手の医師は気を悪くしたかもしれませんが、肺がん治療医としての意気込みというか、覚悟みたいなものを、今回の検査で感じ取ってもらえればいいのですが。
実際に肺がんの診断がついたら、今回の患者さんは一度は根治的定位放射線照射の適応がないかどうか、放射線治療医に相談してみたいと思っています。
同側他葉に2-3か所しかない微小病変だけのために、根治療法の道を閉ざしてしまうのは、あまりにももったいない気がします。
薬物療法をするかしないかは、それから考えても遅くないはずです。
2014年10月13日
進展型肺小細胞癌と予防的全脳照射
治療内容にも、「お国柄」というものがあります。
小細胞がんに関していえば、進展型小細胞癌の治療は、
・我が国:シスプラチン+イリノテカン
・米国:シスプラチン+エトポシド
・欧州:シクロフォスファミド+ドキソルビシン+ビンクリスチンとシスプラチン+エトポシドの交代療法
といったように、治療内容が国や地域によって異なるのは珍しくありません。
化学療法だけでもそうですが、このところ進展型小細胞癌に対する放射線治療の在り方についても、我が国と欧州でずれが生じつつあります。
肺小細胞癌に対して化学(放射線)療法を行い、CRもしくはgood PRが得られた場合には、予防的全脳照射を行うのが標準治療とされています。
よく引き合いに出されるのが、フランスのAuperin先生の以下の論文です。
Prophylactic cranial irradiation for patients with small-cell lung cancer in complete remission. Prophylactic Cranial Irradiation Overview Collaborative Group.
Aupérin A, Arriagada R, Pignon JP, Le Péchoux C, Gregor A, Stephens RJ, Kristjansen PE, Johnson BE, Ueoka H, Wagner H, Aisner J.
N Engl J Med. 1999 Aug 12;341(7):476-84
背景:肺小細胞がんの患者において、予防的全脳照射は脳転移の出現を減らす。治療後に完全奏効に至った際に予防的全脳照射を行うとどの程度予後が改善するのかよくわかっていない。今回我々は、予防的全脳照射が予後を改善するのか調べるため、メタアナルシスを行った。
方法:予防的全脳照射を行うか否かを比較した7つの臨床試験に参加し、治療後に完全奏効に至った987人の個別のデータを解析した。腫瘍評価項目は全生存期間とした。
結果:コントロール群に比べて、治療群の全死亡の相対リスクは0.84(95%信頼区間:0.73-0.97, p=0.01)であった。

これは、3年生存割合にして5.4%の増加(コントロール群15.3%に対して、治療群20.7%)に等しい。予防的全脳照射により無病生存期間も延長し(再発もしくは死亡の相対リスクは0.75,95%信頼区間:0.65-0.86,p<0.001)、脳転移の累積出現リスクも低下した(相対リスクは0.46,95%信頼区間:0.38-0.57,p<0.001)。

放射線照射量を4段階(8Gy,24-25Gy,30Gy,36-40Gy)に分けて検討したところ、照射量が増加するとともに脳転移のリスクは低下する傾向にあった(p=0.02)が、生存には寄与しなかった。 また、導入化学療法の開始後早期に全脳照射を開始すると脳転移のリスクが低下する傾向が見られた(p=0.01)。
結論:完全奏効に至った肺小細胞がんの患者に対する予防的全脳照射は全生存期間、無病生存期間のいずれも改善する。
我が国の肺がん診療ガイドラインでは、限局型肺小細胞がんの患者さんが初期治療で完全奏効に至った場合の予防的全脳照射は推奨グレード(A)として、進展型肺小細胞がんの患者さんが初期治療で完全奏効に至った場合の予防的全脳照射は推奨グレード(B)として記載しています。
これは、上記論文における総数987人の患者さんに対して進展型の患者さんが140人(14%)と少なかったことや、次の患者背景に示されているように、コントロール群と治療群における進展型の患者さんの割合に有意差があり、コントロール群により多くの進展型の患者さんが含まれていることも関わっているのだと思います。

それでは、進展型の患者さんに対する予防的全脳照射はどの程度意義があるのか。
そもそも、進展型の患者さんが完全奏効に至ることは稀です。
しかし、good PRと呼ばれる「この人はよく効いた!」と言える患者さんは相当数いらっしゃいます。
そんな患者さんへの予防的全脳照射はどうなのか、ということで、2007年の米国臨床腫瘍学会では、進展型小細胞癌においても予防的全脳照射は、脳転移再燃割合を改善するのみならず、全生存期間延長にも寄与するとオランダのSlotman先生が発表しました。この年のPlenary sessionに採択されており、8月にはNew England Journal of Medicine誌に掲載されています。
Prophylactic cranial irradiation in extensive small-cell lung cancer.
Slotman B, Faivre-Finn C, Kramer G, Rankin E, Snee M, Hatton M, Postmus P, Collette L, Musat E, Senan S; EORTC Radiation Oncology Group and Lung Cancer Group.
N Engl J Med. 2007 Aug 16;357(7):664-72
背景:化学療法に対する治療反応が得られた進展型肺小細胞がんの患者を対象に予防的全脳照射を行う無作為化比較試験を計画した。
方法:18歳から75歳までの進展型肺小細胞がんの患者を、予防的全脳照射を行う群(照射群)と行わない群(コントロール群)に無作為に割り付けた。主要評価項目は登録から症状を伴う脳転移が出現するまでの期間とした。脳転移を示唆する症状が出現した場合には脳のCTあるいはMRIを行った。
結果:各群均等に143人を割付けた。照射群では症状を伴う脳転移が出現するリスクが低かった(ハザード比0.27,95%信頼区間:0.16-0.44,p<0.001)。1年以内に脳転移が出現する累積リスクは照射群で14.6%(95%信頼区間:8.3-20.9)、コントロール群で40.4%(95%信頼区間:32.1-48.6)だった。

照射により無病生存期間中央値は12.0週から14.7週に延長し、割付後の生存期間中央値は5.4ヶ月から6.7ヶ月に延長した。


1年生存割合は照射群で27.1%(95%信頼区間:19.4-35.5)、コントロール群で13.3%(95%信頼区間:8.1-19.9)だった。照射には有害事象を伴ったが、global health statusに影響を与えるようなものはなかった。
結論:予防的全脳照射は症状を伴う脳転移を抑制し、無病生存期間および全生存期間を延長する。
これは非常にインパクトのある試験結果で、我が国のその後の小細胞がん関連の臨床試験に大きな影響を及ぼしました。
進展型肺小細胞がんに対する化学療法の第III相試験においても、その後に予防的全脳照射を加えるか否かで予後が変わるとなると、きっちりプロトコール治療として組み入れなければならないことになります。
施設によって予防的全脳照射をする、しないの見解が分かれ、それじゃああらかじめする施設、しない施設はその方針を決めておいて、治療施設も割付調整因子としましょうってなことになりました。
しかし、Slotman先生の報告にはいくつか問題点がありました。
ひとつは、試験登録前に画像診断により脳転移の有無が確認された患者がわずか29%であったこと。
我が国では(少なくとも全うな肺がん治療を行っている施設では)、治療開始前に脳転移の有無を画像診断で確認するのは常識です。
そもそも、脳転移に関わる臨床試験において、試験登録前に脳転移があるかないかを画像診断で確認していないなんて、我々の常識では考えられません。
もうひとつは、主要評価項目を「症状を伴う」脳転移が出現するまでの期間、としていることです。
脳転移の症状はADL、ひいてはPSに大きく影響を及ぼすため、その後の治療を継続できるかどうかに大きく影響します。
我が国では、症状がなくとも数か月ごとに画像診断で脳転移の有無を確認するのが一般的で、この点も我が国と実地臨床と乖離しています。
そのため、Slotman先生の報告内容を疑問視する先生は、我が国には少なからずいらっしゃったはずです。
そのため、我が国でも進展型肺小細胞癌に対する予防的全脳照射の追試が行われ、今年の米国臨床腫瘍学会で九州がんセンターの瀬戸先生が、Slotman先生とはまったく異なる見解を発表されました。
ASCO 2014 abstract #7503
Prophylactic crannial irradiation (PCI) has a detrimental effect on the overall survival (OS ) of patients (pts) with extensive disease small cell lung cancer (ED-SCLC) : Results of a Japanese randomized phase III trial.
Seto T, et al.
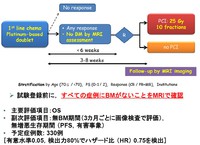
進展型肺小細胞がんに対してプラチナ併用化学療法を行い、なんらかの治療効果が得られた(CR,PR,SD with minor response)患者さんを対象に、前例MRIで脳転移のないことを確認した上で、予防的全脳照射群とコントロール群に無作為に割り付けます。
主要評価項目は全生存期間、副次評価項目は脳転移が出現するまでの期間(症状がなくても3か月ごとに画像診断で評価)、無増悪生存期間とし、有意水準0.05、検出力0.80でハザード比0.75を検出するために計330人の登録が必要でした。
しかし実際には、中間解析時点で無効中止になります。

各群約80人が登録された段階で、全生存期間において予防的全脳照射群の生存曲線がコントロール群を下回っており、これ以上試験を継続しても照射群の優越性が証明される見込みはないと結論されました。

無増悪生存期間も差がつかず。
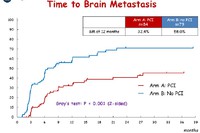
脳転移が出現するまでの期間については、照射群の方が優れていました。
予防的全脳照射が脳転移出現を抑制するのは、上記三報のいずれにも共通しています。
それが生存期間の延長につながったりつながらなかったりするのはなぜなのか。
個人的には、高齢の患者さんに予防的全脳照射を行った際にしばしば見られる認知機能の低下が、どの程度その後の治療に影響を及ぼしたのか、知りたいところです。
上記のSlotman先生は、進展型肺小細胞がんの初期治療後に治療反応性が得られた患者さんに対して、胸部放射線照射を行うと2年生存割合が伸びる、といった趣旨の報告も最近されています。主要評価項目の1年生存割合は改善しなかったので我が国の実地臨床へのインパクトは今のところないと思いますが、今後の臨床試験計画を考える上で新たな議論を呼びそうです。
http://www.ncbi.nlm.nih.gov/pubmed/25230595
小細胞がんに関していえば、進展型小細胞癌の治療は、
・我が国:シスプラチン+イリノテカン
・米国:シスプラチン+エトポシド
・欧州:シクロフォスファミド+ドキソルビシン+ビンクリスチンとシスプラチン+エトポシドの交代療法
といったように、治療内容が国や地域によって異なるのは珍しくありません。
化学療法だけでもそうですが、このところ進展型小細胞癌に対する放射線治療の在り方についても、我が国と欧州でずれが生じつつあります。
肺小細胞癌に対して化学(放射線)療法を行い、CRもしくはgood PRが得られた場合には、予防的全脳照射を行うのが標準治療とされています。
よく引き合いに出されるのが、フランスのAuperin先生の以下の論文です。
Prophylactic cranial irradiation for patients with small-cell lung cancer in complete remission. Prophylactic Cranial Irradiation Overview Collaborative Group.
Aupérin A, Arriagada R, Pignon JP, Le Péchoux C, Gregor A, Stephens RJ, Kristjansen PE, Johnson BE, Ueoka H, Wagner H, Aisner J.
N Engl J Med. 1999 Aug 12;341(7):476-84
背景:肺小細胞がんの患者において、予防的全脳照射は脳転移の出現を減らす。治療後に完全奏効に至った際に予防的全脳照射を行うとどの程度予後が改善するのかよくわかっていない。今回我々は、予防的全脳照射が予後を改善するのか調べるため、メタアナルシスを行った。
方法:予防的全脳照射を行うか否かを比較した7つの臨床試験に参加し、治療後に完全奏効に至った987人の個別のデータを解析した。腫瘍評価項目は全生存期間とした。
結果:コントロール群に比べて、治療群の全死亡の相対リスクは0.84(95%信頼区間:0.73-0.97, p=0.01)であった。

これは、3年生存割合にして5.4%の増加(コントロール群15.3%に対して、治療群20.7%)に等しい。予防的全脳照射により無病生存期間も延長し(再発もしくは死亡の相対リスクは0.75,95%信頼区間:0.65-0.86,p<0.001)、脳転移の累積出現リスクも低下した(相対リスクは0.46,95%信頼区間:0.38-0.57,p<0.001)。

放射線照射量を4段階(8Gy,24-25Gy,30Gy,36-40Gy)に分けて検討したところ、照射量が増加するとともに脳転移のリスクは低下する傾向にあった(p=0.02)が、生存には寄与しなかった。 また、導入化学療法の開始後早期に全脳照射を開始すると脳転移のリスクが低下する傾向が見られた(p=0.01)。
結論:完全奏効に至った肺小細胞がんの患者に対する予防的全脳照射は全生存期間、無病生存期間のいずれも改善する。
我が国の肺がん診療ガイドラインでは、限局型肺小細胞がんの患者さんが初期治療で完全奏効に至った場合の予防的全脳照射は推奨グレード(A)として、進展型肺小細胞がんの患者さんが初期治療で完全奏効に至った場合の予防的全脳照射は推奨グレード(B)として記載しています。
これは、上記論文における総数987人の患者さんに対して進展型の患者さんが140人(14%)と少なかったことや、次の患者背景に示されているように、コントロール群と治療群における進展型の患者さんの割合に有意差があり、コントロール群により多くの進展型の患者さんが含まれていることも関わっているのだと思います。

それでは、進展型の患者さんに対する予防的全脳照射はどの程度意義があるのか。
そもそも、進展型の患者さんが完全奏効に至ることは稀です。
しかし、good PRと呼ばれる「この人はよく効いた!」と言える患者さんは相当数いらっしゃいます。
そんな患者さんへの予防的全脳照射はどうなのか、ということで、2007年の米国臨床腫瘍学会では、進展型小細胞癌においても予防的全脳照射は、脳転移再燃割合を改善するのみならず、全生存期間延長にも寄与するとオランダのSlotman先生が発表しました。この年のPlenary sessionに採択されており、8月にはNew England Journal of Medicine誌に掲載されています。
Prophylactic cranial irradiation in extensive small-cell lung cancer.
Slotman B, Faivre-Finn C, Kramer G, Rankin E, Snee M, Hatton M, Postmus P, Collette L, Musat E, Senan S; EORTC Radiation Oncology Group and Lung Cancer Group.
N Engl J Med. 2007 Aug 16;357(7):664-72
背景:化学療法に対する治療反応が得られた進展型肺小細胞がんの患者を対象に予防的全脳照射を行う無作為化比較試験を計画した。
方法:18歳から75歳までの進展型肺小細胞がんの患者を、予防的全脳照射を行う群(照射群)と行わない群(コントロール群)に無作為に割り付けた。主要評価項目は登録から症状を伴う脳転移が出現するまでの期間とした。脳転移を示唆する症状が出現した場合には脳のCTあるいはMRIを行った。
結果:各群均等に143人を割付けた。照射群では症状を伴う脳転移が出現するリスクが低かった(ハザード比0.27,95%信頼区間:0.16-0.44,p<0.001)。1年以内に脳転移が出現する累積リスクは照射群で14.6%(95%信頼区間:8.3-20.9)、コントロール群で40.4%(95%信頼区間:32.1-48.6)だった。

照射により無病生存期間中央値は12.0週から14.7週に延長し、割付後の生存期間中央値は5.4ヶ月から6.7ヶ月に延長した。


1年生存割合は照射群で27.1%(95%信頼区間:19.4-35.5)、コントロール群で13.3%(95%信頼区間:8.1-19.9)だった。照射には有害事象を伴ったが、global health statusに影響を与えるようなものはなかった。
結論:予防的全脳照射は症状を伴う脳転移を抑制し、無病生存期間および全生存期間を延長する。
これは非常にインパクトのある試験結果で、我が国のその後の小細胞がん関連の臨床試験に大きな影響を及ぼしました。
進展型肺小細胞がんに対する化学療法の第III相試験においても、その後に予防的全脳照射を加えるか否かで予後が変わるとなると、きっちりプロトコール治療として組み入れなければならないことになります。
施設によって予防的全脳照射をする、しないの見解が分かれ、それじゃああらかじめする施設、しない施設はその方針を決めておいて、治療施設も割付調整因子としましょうってなことになりました。
しかし、Slotman先生の報告にはいくつか問題点がありました。
ひとつは、試験登録前に画像診断により脳転移の有無が確認された患者がわずか29%であったこと。
我が国では(少なくとも全うな肺がん治療を行っている施設では)、治療開始前に脳転移の有無を画像診断で確認するのは常識です。
そもそも、脳転移に関わる臨床試験において、試験登録前に脳転移があるかないかを画像診断で確認していないなんて、我々の常識では考えられません。
もうひとつは、主要評価項目を「症状を伴う」脳転移が出現するまでの期間、としていることです。
脳転移の症状はADL、ひいてはPSに大きく影響を及ぼすため、その後の治療を継続できるかどうかに大きく影響します。
我が国では、症状がなくとも数か月ごとに画像診断で脳転移の有無を確認するのが一般的で、この点も我が国と実地臨床と乖離しています。
そのため、Slotman先生の報告内容を疑問視する先生は、我が国には少なからずいらっしゃったはずです。
そのため、我が国でも進展型肺小細胞癌に対する予防的全脳照射の追試が行われ、今年の米国臨床腫瘍学会で九州がんセンターの瀬戸先生が、Slotman先生とはまったく異なる見解を発表されました。
ASCO 2014 abstract #7503
Prophylactic crannial irradiation (PCI) has a detrimental effect on the overall survival (OS ) of patients (pts) with extensive disease small cell lung cancer (ED-SCLC) : Results of a Japanese randomized phase III trial.
Seto T, et al.

進展型肺小細胞がんに対してプラチナ併用化学療法を行い、なんらかの治療効果が得られた(CR,PR,SD with minor response)患者さんを対象に、前例MRIで脳転移のないことを確認した上で、予防的全脳照射群とコントロール群に無作為に割り付けます。
主要評価項目は全生存期間、副次評価項目は脳転移が出現するまでの期間(症状がなくても3か月ごとに画像診断で評価)、無増悪生存期間とし、有意水準0.05、検出力0.80でハザード比0.75を検出するために計330人の登録が必要でした。
しかし実際には、中間解析時点で無効中止になります。

各群約80人が登録された段階で、全生存期間において予防的全脳照射群の生存曲線がコントロール群を下回っており、これ以上試験を継続しても照射群の優越性が証明される見込みはないと結論されました。

無増悪生存期間も差がつかず。

脳転移が出現するまでの期間については、照射群の方が優れていました。
予防的全脳照射が脳転移出現を抑制するのは、上記三報のいずれにも共通しています。
それが生存期間の延長につながったりつながらなかったりするのはなぜなのか。
個人的には、高齢の患者さんに予防的全脳照射を行った際にしばしば見られる認知機能の低下が、どの程度その後の治療に影響を及ぼしたのか、知りたいところです。
上記のSlotman先生は、進展型肺小細胞がんの初期治療後に治療反応性が得られた患者さんに対して、胸部放射線照射を行うと2年生存割合が伸びる、といった趣旨の報告も最近されています。主要評価項目の1年生存割合は改善しなかったので我が国の実地臨床へのインパクトは今のところないと思いますが、今後の臨床試験計画を考える上で新たな議論を呼びそうです。
http://www.ncbi.nlm.nih.gov/pubmed/25230595



