2020年04月29日
プラチナ併用化学療法後、次治療としてのペンブロリズマブ+ドセタキセル併用療法(EGFR遺伝子変異陽性者を含む)
免疫チェックポイント阻害薬がほぼ一次治療で使われるようになった今になって、二次治療での話かよ、と高を括っていた。
EGFR遺伝子変異陽性の患者からの相談に答えていて、ふと思いなおした。
EGFR遺伝子変異陽性で、EGFRチロシンキナーゼ阻害薬による治療を開始した患者では、耐性化後に免疫チェックポイント阻害薬を使用せずにプラチナ併用化学療法を行う患者の方が圧倒的に多いのだ。
EGFR遺伝子変異が認められた段階で、PD-L1を評価しない慣例があるのが一因。
薬剤性肺障害を恐れて、EGFRチロシンキナーゼ阻害薬を使い切るまでは免疫チェックポイント阻害薬を使いたくない、というのが一因。
そんなニッチなunmet needに、本試験は切り込んでいるように思う。
今回の結果を受けて、敢えてEGFR遺伝子変異陽性患者に絞って臨床試験を行ってみれば面白いのではないだろうか。
現時点で、間違いなくunmet needはある。
Addition of Pembrolizumab to Docetaxel for Previously Treated Immunotherapy-Naive Patients With Advanced NSCLC
Oscar Arrieta et al., JAMA Oncol 2020
doi:10.1001/jamaoncol.2020.0409
背景:
社会経済的な要因のため、進行非小細胞肺がん患者の多くは初回治療としての免疫チェックポイント阻害薬を使用できずにいる。前治療でプラチナ併用化学療法を行い、病勢進行に至った免疫チェックポイント阻害薬未使用の患者に対して、引き続く免疫チェックポイント阻害薬併用化学療法が臨床的に有用なのかどうか、今のところデータがない。
目的:
EGFR遺伝子変異状態、もしくはPD-L1発現状態によらず、プラチナ併用化学療法による前治療後の進行非小細胞肺がん患者に対してペンブロリズマブとドセタキセルの併用療法を行った際の効果と安全性を評価すること。
試験デザインと対象患者:
今回のPROLUNG試験では、組織学的に診断された進行非小細胞肺がん患者78人を、ペンブロリズマブ+ドセタキセル併用療法群(PD群)とドセタキセル単剤療法群(D群)に、1:1の割合で無作為に割り付けた。試験実施時期は2016年12月から2019年5月とした。本試験はメキシコシティーの国立がん研究所単施設で行われた。
治療内容:
PD群では、ドセタキセル75mg/㎡を1日目、ペンブロリズマブ200mg/回を8日目に投与し、これを3週間ごとに、最大6コースまで反復し、その後は病勢進行もしくは忍容不能の毒性発現に至るまで、ペンブロリズマブのみを維持療法として継続した。D群では、ドセタキセル単剤療法を病勢進行もしくは忍容不能の毒性発現に至るまで継続した。
評価項目:
主要評価項目は奏効割合とした。副次評価項目は無増悪生存期間、全生存期間、安全性とした。
結果:
78人の患者を集積した。32人(41%)は男性、34人(44%)は喫煙経験のない患者、25人(32%)はEGFR遺伝子変異もしくはALK融合遺伝子を有していた。PD群には40人(うち12人はEGFR遺伝子変異陽性)、D群には38人(うち13人はEGFR遺伝子変異陽性)が割り付けられた。独立評価委員会での判定により、統計学的に有意な奏効割合の差が検出された。奏効割合はPD群で42.5%、D群で15.8%、オッズ比は3.94、95%信頼区間は1.34-11.54、p=0.01だった。EGFR遺伝子変異のない患者では、奏効割合はPD群で35.7%,D群で12.0%だった(p=0.06)。一方、EGFR遺伝子変異を有する患者では、奏効割合はPD群で58.3%、D群で23.1%(p=0.14)だった。無増悪生存期間中央値はPD群で9.5ヶ月(95%信頼区間は4.2ヶ月-未到達)、D群で3.9ヶ月(95%信頼区間は3.2-5.7ヶ月)だった(ハザード比0.24、95%信頼区間は0.13-0.46、p<0.001)。EGFR遺伝子変異のない患者では、無増悪生存期間中央値はPD群で9.5ヶ月(95%信頼区間は3.9ヶ月-未到達)、D群で4.1ヶ月(95%信頼区間は3.5-5.3ヶ月)だった(p<0.001)。一方、EGFR遺伝子変異を有する患者では、無増悪生存期間中央値はPD群で6.8ヶ月(95%信頼区間は6.2ヶ月-未到達)、D群で3.5ヶ月(95%信頼区間は2.3-6.2ヶ月)だった(p=0.04)。安全性については、PD群の23%(40人中9人)、D群の5%(38人中2人)においてGrade 1-2の肺臓炎を認め、有意にPD群で高頻度だった(p=0.03)。また、PD群の28%(40人中11人)、D群の3%(38人中1人)において甲状腺機能低下症を認めた(p=0.002)。低マグネシウム血症はPD群では認められず、D群では18%に認めた(p=0.004)。また、リンパ球減少はPD群の20%で認め、D群では認められなかった(p=0.004)。未知の有害事象は認められなかった。
結論:
今回の第II相試験において、EGFR遺伝子変異陽性者を含む進行非小細胞肺がん患者において、プラチナ併用化学療法既治療の患者に対するペンブロリズマブ+ドセタキセル併用療法が、忍容可能でかつ奏効割合や無増悪生存期間を改善する可能性があることが示された。
EGFR遺伝子変異陽性の患者からの相談に答えていて、ふと思いなおした。
EGFR遺伝子変異陽性で、EGFRチロシンキナーゼ阻害薬による治療を開始した患者では、耐性化後に免疫チェックポイント阻害薬を使用せずにプラチナ併用化学療法を行う患者の方が圧倒的に多いのだ。
EGFR遺伝子変異が認められた段階で、PD-L1を評価しない慣例があるのが一因。
薬剤性肺障害を恐れて、EGFRチロシンキナーゼ阻害薬を使い切るまでは免疫チェックポイント阻害薬を使いたくない、というのが一因。
そんなニッチなunmet needに、本試験は切り込んでいるように思う。
今回の結果を受けて、敢えてEGFR遺伝子変異陽性患者に絞って臨床試験を行ってみれば面白いのではないだろうか。
現時点で、間違いなくunmet needはある。
Addition of Pembrolizumab to Docetaxel for Previously Treated Immunotherapy-Naive Patients With Advanced NSCLC
Oscar Arrieta et al., JAMA Oncol 2020
doi:10.1001/jamaoncol.2020.0409
背景:
社会経済的な要因のため、進行非小細胞肺がん患者の多くは初回治療としての免疫チェックポイント阻害薬を使用できずにいる。前治療でプラチナ併用化学療法を行い、病勢進行に至った免疫チェックポイント阻害薬未使用の患者に対して、引き続く免疫チェックポイント阻害薬併用化学療法が臨床的に有用なのかどうか、今のところデータがない。
目的:
EGFR遺伝子変異状態、もしくはPD-L1発現状態によらず、プラチナ併用化学療法による前治療後の進行非小細胞肺がん患者に対してペンブロリズマブとドセタキセルの併用療法を行った際の効果と安全性を評価すること。
試験デザインと対象患者:
今回のPROLUNG試験では、組織学的に診断された進行非小細胞肺がん患者78人を、ペンブロリズマブ+ドセタキセル併用療法群(PD群)とドセタキセル単剤療法群(D群)に、1:1の割合で無作為に割り付けた。試験実施時期は2016年12月から2019年5月とした。本試験はメキシコシティーの国立がん研究所単施設で行われた。
治療内容:
PD群では、ドセタキセル75mg/㎡を1日目、ペンブロリズマブ200mg/回を8日目に投与し、これを3週間ごとに、最大6コースまで反復し、その後は病勢進行もしくは忍容不能の毒性発現に至るまで、ペンブロリズマブのみを維持療法として継続した。D群では、ドセタキセル単剤療法を病勢進行もしくは忍容不能の毒性発現に至るまで継続した。
評価項目:
主要評価項目は奏効割合とした。副次評価項目は無増悪生存期間、全生存期間、安全性とした。
結果:
78人の患者を集積した。32人(41%)は男性、34人(44%)は喫煙経験のない患者、25人(32%)はEGFR遺伝子変異もしくはALK融合遺伝子を有していた。PD群には40人(うち12人はEGFR遺伝子変異陽性)、D群には38人(うち13人はEGFR遺伝子変異陽性)が割り付けられた。独立評価委員会での判定により、統計学的に有意な奏効割合の差が検出された。奏効割合はPD群で42.5%、D群で15.8%、オッズ比は3.94、95%信頼区間は1.34-11.54、p=0.01だった。EGFR遺伝子変異のない患者では、奏効割合はPD群で35.7%,D群で12.0%だった(p=0.06)。一方、EGFR遺伝子変異を有する患者では、奏効割合はPD群で58.3%、D群で23.1%(p=0.14)だった。無増悪生存期間中央値はPD群で9.5ヶ月(95%信頼区間は4.2ヶ月-未到達)、D群で3.9ヶ月(95%信頼区間は3.2-5.7ヶ月)だった(ハザード比0.24、95%信頼区間は0.13-0.46、p<0.001)。EGFR遺伝子変異のない患者では、無増悪生存期間中央値はPD群で9.5ヶ月(95%信頼区間は3.9ヶ月-未到達)、D群で4.1ヶ月(95%信頼区間は3.5-5.3ヶ月)だった(p<0.001)。一方、EGFR遺伝子変異を有する患者では、無増悪生存期間中央値はPD群で6.8ヶ月(95%信頼区間は6.2ヶ月-未到達)、D群で3.5ヶ月(95%信頼区間は2.3-6.2ヶ月)だった(p=0.04)。安全性については、PD群の23%(40人中9人)、D群の5%(38人中2人)においてGrade 1-2の肺臓炎を認め、有意にPD群で高頻度だった(p=0.03)。また、PD群の28%(40人中11人)、D群の3%(38人中1人)において甲状腺機能低下症を認めた(p=0.002)。低マグネシウム血症はPD群では認められず、D群では18%に認めた(p=0.004)。また、リンパ球減少はPD群の20%で認め、D群では認められなかった(p=0.004)。未知の有害事象は認められなかった。
結論:
今回の第II相試験において、EGFR遺伝子変異陽性者を含む進行非小細胞肺がん患者において、プラチナ併用化学療法既治療の患者に対するペンブロリズマブ+ドセタキセル併用療法が、忍容可能でかつ奏効割合や無増悪生存期間を改善する可能性があることが示された。
2020年04月26日
免疫チェックポイント阻害薬による術前免疫療法
ときどき思い立って、データベースを使って肺がん患者さんの過去を遡り、気づきを探すことにしている。
やはり、5年間以上の長期生存を達成した患者さんの臨床経過は参考になる。
こうした作業は、学会発表で経過をまとめる医師がときどき行う程度で、実際にはあまり為されていないのではないだろうか。
前向き臨床試験がすべてであり、標準治療以外の治療は行う価値はなく、実地臨床で診療する患者の過去なんて振り返らない、という医師には、おそらく永遠に見えてこない景色がある。
私は、臨床試験から得られる知見と、実地臨床から得られる経験(と振り返り)、そして社会人・家庭人としての常識、これらがうまくかみ合って、初めて最良の診療ができると信じている。
長生きしている患者さんの診療を振り返ってその都度感じるのは、その時々の患者の状況に応じて、知恵を絞って、諦めずに泥臭く悪戦苦闘すると、ときになんらかの光明が見えるということである。
ドライバー遺伝子変異陽性の患者でも、分子標的薬が効いていた期間よりも殺細胞性抗腫瘍薬が効いていた期間の方が長くなることもある。
脳転移再発した完全切除後の患者でも、脳転移の治療をした後に5年以上長生きすることもある。
免疫チェックポイント阻害薬が実地臨床に浸透して、どの程度長生きする患者が増えるのか、楽しみだ。
進行期の患者だけでなく、術後補助療法としても臨床試験が行われているが、なんとなく参加者は長生きしているような印象を受ける。
また、術前療法としても臨床試験が進行しているようで、以下の記事を見ると期待が持てる。
What’s the Current Status of Neoadjuvant Immunotherapy?
The ASCO Post
April 25, 2020
<肺がんに対する術前免疫療法>
免疫療法は、進行期肺がんに対する薬物療法として、そして完全切除後の肺がんに対する術後療法として進化してきた。術前療法としての意義も検討されつつある。免疫療法を行うことで、治療前には手術ができなかった患者に対して、手術ができるようになるかもしれない。また、免疫療法の効果が極めて良好な患者では、手術そのものが不要になるかもしれない。
こうした術前免疫療法の可能性については、すでに50以上の臨床試験が非小細胞肺がん患者を対象に広く行われており、その多くは第III相臨床試験である。
こうした臨床試験の初期のものは既に結果が報告されている。非小細胞肺がん患者20人を対象とした臨床試験(Forde PM, Chaft JE, Smith KN, et al: Neoadjuvant PD-1 blockade in resectable lung cancer. N Engl J Med 378:1976-1986, 2018., http://oitahaiganpractice.junglekouen.com/e932057.html)では、完全奏効はほとんど観察されなかった一方で、Major pathologic response rate(病理学的に、病巣内の腫瘍細胞のうち90%は死滅していた患者の割合)は45%(9人)で、3年間の間に術後再発を来した患者はわずか1人で、その患者も適切に再治療できている。長期経過観察において、寛解状態を維持している患者の血中を循環する腫瘍DNAは認められておらず、免疫療法がよく効いた患者では、腫瘍特異的T細胞クローン数が有意に高く保たれており、潜在的に抗腫瘍活性を惹起している。
非小細胞肺がんの術前免疫療法臨床試験における病理学的完全寛解割合は24%であり、これは術前化学療法におけるそれの20%よりも高い。さらには、術前免疫療法の方が毒性が軽い。特筆すべきことに、NADIM II試験(ClinicalTrials.gov identifier NCT03838159)において術前化学療法にニボルマブを上乗せしたところ、Major pathologic response rateは74%に上った。
術前免疫療法は、化学療法と併用される・されないに関わらず、忍容可能で病理学的寛解状態へ導きうるということで、こうした所見は複数の第III相臨床試験で検証中である。術前化学免疫療法と術前化学療法を比較する現在進行中の臨床試験には、CheckMate 816試験(ニボルマブ)、KEYNOTE-671試験(ペンブロリズマブ)、IMpassion030試験(アテゾリズマブ)が含まれる。AEGEAN試験は、抗PD-L1抗体であるデュルバルマブとプラセボを比較するコンセプトである。そのほかに、新規薬物を用いた臨床試験も進行中である。
2010年から2020年にかけては、進行期肺がん患者に対する分子標的薬や免疫チェックポイント阻害薬が勃興した時代だった。2020年から2030年は、こうした治療が早期肺がんの治療に応用し、再発の回避を目指すことになるだろう。
やはり、5年間以上の長期生存を達成した患者さんの臨床経過は参考になる。
こうした作業は、学会発表で経過をまとめる医師がときどき行う程度で、実際にはあまり為されていないのではないだろうか。
前向き臨床試験がすべてであり、標準治療以外の治療は行う価値はなく、実地臨床で診療する患者の過去なんて振り返らない、という医師には、おそらく永遠に見えてこない景色がある。
私は、臨床試験から得られる知見と、実地臨床から得られる経験(と振り返り)、そして社会人・家庭人としての常識、これらがうまくかみ合って、初めて最良の診療ができると信じている。
長生きしている患者さんの診療を振り返ってその都度感じるのは、その時々の患者の状況に応じて、知恵を絞って、諦めずに泥臭く悪戦苦闘すると、ときになんらかの光明が見えるということである。
ドライバー遺伝子変異陽性の患者でも、分子標的薬が効いていた期間よりも殺細胞性抗腫瘍薬が効いていた期間の方が長くなることもある。
脳転移再発した完全切除後の患者でも、脳転移の治療をした後に5年以上長生きすることもある。
免疫チェックポイント阻害薬が実地臨床に浸透して、どの程度長生きする患者が増えるのか、楽しみだ。
進行期の患者だけでなく、術後補助療法としても臨床試験が行われているが、なんとなく参加者は長生きしているような印象を受ける。
また、術前療法としても臨床試験が進行しているようで、以下の記事を見ると期待が持てる。
What’s the Current Status of Neoadjuvant Immunotherapy?
The ASCO Post
April 25, 2020
<肺がんに対する術前免疫療法>
免疫療法は、進行期肺がんに対する薬物療法として、そして完全切除後の肺がんに対する術後療法として進化してきた。術前療法としての意義も検討されつつある。免疫療法を行うことで、治療前には手術ができなかった患者に対して、手術ができるようになるかもしれない。また、免疫療法の効果が極めて良好な患者では、手術そのものが不要になるかもしれない。
こうした術前免疫療法の可能性については、すでに50以上の臨床試験が非小細胞肺がん患者を対象に広く行われており、その多くは第III相臨床試験である。
こうした臨床試験の初期のものは既に結果が報告されている。非小細胞肺がん患者20人を対象とした臨床試験(Forde PM, Chaft JE, Smith KN, et al: Neoadjuvant PD-1 blockade in resectable lung cancer. N Engl J Med 378:1976-1986, 2018., http://oitahaiganpractice.junglekouen.com/e932057.html)では、完全奏効はほとんど観察されなかった一方で、Major pathologic response rate(病理学的に、病巣内の腫瘍細胞のうち90%は死滅していた患者の割合)は45%(9人)で、3年間の間に術後再発を来した患者はわずか1人で、その患者も適切に再治療できている。長期経過観察において、寛解状態を維持している患者の血中を循環する腫瘍DNAは認められておらず、免疫療法がよく効いた患者では、腫瘍特異的T細胞クローン数が有意に高く保たれており、潜在的に抗腫瘍活性を惹起している。
非小細胞肺がんの術前免疫療法臨床試験における病理学的完全寛解割合は24%であり、これは術前化学療法におけるそれの20%よりも高い。さらには、術前免疫療法の方が毒性が軽い。特筆すべきことに、NADIM II試験(ClinicalTrials.gov identifier NCT03838159)において術前化学療法にニボルマブを上乗せしたところ、Major pathologic response rateは74%に上った。
術前免疫療法は、化学療法と併用される・されないに関わらず、忍容可能で病理学的寛解状態へ導きうるということで、こうした所見は複数の第III相臨床試験で検証中である。術前化学免疫療法と術前化学療法を比較する現在進行中の臨床試験には、CheckMate 816試験(ニボルマブ)、KEYNOTE-671試験(ペンブロリズマブ)、IMpassion030試験(アテゾリズマブ)が含まれる。AEGEAN試験は、抗PD-L1抗体であるデュルバルマブとプラセボを比較するコンセプトである。そのほかに、新規薬物を用いた臨床試験も進行中である。
2010年から2020年にかけては、進行期肺がん患者に対する分子標的薬や免疫チェックポイント阻害薬が勃興した時代だった。2020年から2030年は、こうした治療が早期肺がんの治療に応用し、再発の回避を目指すことになるだろう。
2020年04月22日
終末期ケアとCoVID-19緊急事態宣言のせめぎあい
がんの種類を問わず、社会復帰を目指したリハビリテーションを希望する患者、あるいは住み慣れた地域での終末期医療を希望する患者は、できるだけ受け入れるように努力している。
今日は、婦人科がんの患者受け入れについて、県外の医療機関から要請があった。
全国的に緊急事態宣言が発出されている中での、県外からの患者受け入れ要請。
こちらからの要望をお返事にまとめて、できるだけいい形でお受け入れできるように、先方でも当院でも準備を進めることにした。
現在の入院担当患者で、背景は様々ながら終末期と言ってよい患者は、5人いる。
進行肺がん、進行胃がん、気管支拡張症、認知症及び反復性胆道感染症といった背景である。
目下のところ一番つらそうなのは、黄疸が急速に進行しつつある胃がんの患者と、呼吸不全が進行しつつある気管支拡張症の患者だ。
ことに後者は、苦しい、きつい、早く死なせてくれ、と、診察の度に眉間にしわを寄せて切々と訴える。
患者もつらいが、家族もつらい。
緊急事態宣言を受けて、当院でも院長と感染対策委員会の指導のもと、院内感染予防対策を行っている。
面会は原則禁止、不要不急の病状説明も禁止、どうしても必要なら外来スペースを用いて短時間で病状説明を、という指導内容だった。
ましてや、関東や関西、福岡からの家族帰省・面談などもってのほか、という状況である。
実際、私自身の親族も現在良性疾患で入院中だが、県外在住の親族には、こちらで責任もって面倒見るから帰ってくるなと伝えている。
しかし、日頃患者に会えていない終末期がんのご家族ほど、せめて最後のひとときだけはと、現下の状況においても面会を切望する。
お気持ちはわかるのだけど、何とかしてあげたい気もするのだけど。
でも、なぜ今まで、こうした社会情勢になるまでに、会ってあげなかったの、という気にもなる。
実際のところ、病棟診療をしている最中、黄昏時になって、外来から発熱患者の診療依頼があった。
ここ3-4日にわたり、微熱だけが続いている70代後半の患者。
かかりつけの2病院に受診相談をしたところ、どちらからも受け付けの段階で(担当医への相談もなく)断られたとのこと。
保健所に相談したところ、自宅住所の最寄りの医療機関が当院だから、という理由で、当院受診を指示されたらしい。
県外・海外への移動歴なく、県外・海外の人との接触歴もなく、新型コロナウイルス感染確定者との接触歴もない。
それでも各種臨床検査を行ったところ、新型コロナウイルス肺炎が極めて疑わしいレントゲン、CT所見だった。
保健所に報告して、SARS-CoV-2 PCR検査用の検体を採取し、解熱薬を処方して自宅待機していただくこととした。
結果がはっきりするまで、どうか病状が急速に進行しないようにと祈るばかりである。
たとえ外来対応であっても、こうした形で前触れなくCoVID-19疑い患者と接する機会があると思うと、並行して他の外来・病棟診療をどのように進めていくか、とても悩んでしまう。
県外からの紹介患者は道義的に受け入れざるを得ないにせよ、大都市圏在住の家族の面会の件は、本当に頭が痛い。
今日は、婦人科がんの患者受け入れについて、県外の医療機関から要請があった。
全国的に緊急事態宣言が発出されている中での、県外からの患者受け入れ要請。
こちらからの要望をお返事にまとめて、できるだけいい形でお受け入れできるように、先方でも当院でも準備を進めることにした。
現在の入院担当患者で、背景は様々ながら終末期と言ってよい患者は、5人いる。
進行肺がん、進行胃がん、気管支拡張症、認知症及び反復性胆道感染症といった背景である。
目下のところ一番つらそうなのは、黄疸が急速に進行しつつある胃がんの患者と、呼吸不全が進行しつつある気管支拡張症の患者だ。
ことに後者は、苦しい、きつい、早く死なせてくれ、と、診察の度に眉間にしわを寄せて切々と訴える。
患者もつらいが、家族もつらい。
緊急事態宣言を受けて、当院でも院長と感染対策委員会の指導のもと、院内感染予防対策を行っている。
面会は原則禁止、不要不急の病状説明も禁止、どうしても必要なら外来スペースを用いて短時間で病状説明を、という指導内容だった。
ましてや、関東や関西、福岡からの家族帰省・面談などもってのほか、という状況である。
実際、私自身の親族も現在良性疾患で入院中だが、県外在住の親族には、こちらで責任もって面倒見るから帰ってくるなと伝えている。
しかし、日頃患者に会えていない終末期がんのご家族ほど、せめて最後のひとときだけはと、現下の状況においても面会を切望する。
お気持ちはわかるのだけど、何とかしてあげたい気もするのだけど。
でも、なぜ今まで、こうした社会情勢になるまでに、会ってあげなかったの、という気にもなる。
実際のところ、病棟診療をしている最中、黄昏時になって、外来から発熱患者の診療依頼があった。
ここ3-4日にわたり、微熱だけが続いている70代後半の患者。
かかりつけの2病院に受診相談をしたところ、どちらからも受け付けの段階で(担当医への相談もなく)断られたとのこと。
保健所に相談したところ、自宅住所の最寄りの医療機関が当院だから、という理由で、当院受診を指示されたらしい。
県外・海外への移動歴なく、県外・海外の人との接触歴もなく、新型コロナウイルス感染確定者との接触歴もない。
それでも各種臨床検査を行ったところ、新型コロナウイルス肺炎が極めて疑わしいレントゲン、CT所見だった。
保健所に報告して、SARS-CoV-2 PCR検査用の検体を採取し、解熱薬を処方して自宅待機していただくこととした。
結果がはっきりするまで、どうか病状が急速に進行しないようにと祈るばかりである。
たとえ外来対応であっても、こうした形で前触れなくCoVID-19疑い患者と接する機会があると思うと、並行して他の外来・病棟診療をどのように進めていくか、とても悩んでしまう。
県外からの紹介患者は道義的に受け入れざるを得ないにせよ、大都市圏在住の家族の面会の件は、本当に頭が痛い。
2020年04月18日
TepotinibがMET exon 14 skipping mutation陽性の非小細胞肺がんに対する承認を取得
この患者集団に対しては、クリゾチニブが最初に承認されると思っていたが、Tepotinibが先陣を切った。
http://oitahaiganpractice.junglekouen.com/e968768.html
https://kyodonewsprwire.jp/release/202003258400
<Tepotinibが「MET遺伝子エクソン14スキッピング変異陽性の切除不能な進行・再発の非小細胞肺癌」に対する製造販売承認を取得> 2020/03/25
・メルクバイオファーマ株式会社は、MET遺伝子エクソン14(METex14)スキッピング変異陽性の切除不能な進行・再発の非小細胞肺癌(以下、NSCLC)の治療薬、Tepotinibについて、厚生労働省から製造販売承認を取得した
・テポチニブは、世界に先駆けて日本で初めて、METex14スキッピング変異陽性の切除不能な進行・再発のNSCLCの治療薬として承認を受けた
・リキッドバイオプシーもしくは腫瘍生検により同定したMETex14スキッピング変異もしくはMET増幅を有する進行性NSCLC患者を対象にした進行中の第II相VISION臨床試験で、Tepotinib単剤での安全性と有効性を評価
・試験全体の奏効率(ORR)は、独立判定委員会(IRC)による評価で42.4%、奏効期間(DOR)中央値は、12.4か月
・これらの結果は、リキッドバイオプシーおよび腫瘍生検で変異同定した患者で一貫していた
・安全性を評価した130例で、副作用のほとんどはグレード1または2であり、死亡に至った副作用が1例(急性呼吸不全)認められた
・グレードを問わず10%以上の件数が報告された副作用は、末梢浮腫(53.8%)、悪心(23.8%)、下痢(20.8%)、および血中クレアチニン増加(13.8%)、低アルブミン血症(10.8%)、およびアミラーゼ増加(10.0%)
・11名の患者が副作用により投与中止となり、このうち、最も多く認められたのは末梢性浮腫(3.8%)だった
・コンパニオン診断薬には、MET遺伝子変異を特定するためのコンパニオン診断薬として製造販売承認されたArcher社の「Archer(R) MET コンパニオン診断システム」を使用する必要がある
・同診断システムは、血液検体及び腫瘍組織検体のどちらでも利用可能で、ともに核酸ベースの診断法を用いて検査する
http://oitahaiganpractice.junglekouen.com/e968768.html
https://kyodonewsprwire.jp/release/202003258400
<Tepotinibが「MET遺伝子エクソン14スキッピング変異陽性の切除不能な進行・再発の非小細胞肺癌」に対する製造販売承認を取得> 2020/03/25
・メルクバイオファーマ株式会社は、MET遺伝子エクソン14(METex14)スキッピング変異陽性の切除不能な進行・再発の非小細胞肺癌(以下、NSCLC)の治療薬、Tepotinibについて、厚生労働省から製造販売承認を取得した
・テポチニブは、世界に先駆けて日本で初めて、METex14スキッピング変異陽性の切除不能な進行・再発のNSCLCの治療薬として承認を受けた
・リキッドバイオプシーもしくは腫瘍生検により同定したMETex14スキッピング変異もしくはMET増幅を有する進行性NSCLC患者を対象にした進行中の第II相VISION臨床試験で、Tepotinib単剤での安全性と有効性を評価
・試験全体の奏効率(ORR)は、独立判定委員会(IRC)による評価で42.4%、奏効期間(DOR)中央値は、12.4か月
・これらの結果は、リキッドバイオプシーおよび腫瘍生検で変異同定した患者で一貫していた
・安全性を評価した130例で、副作用のほとんどはグレード1または2であり、死亡に至った副作用が1例(急性呼吸不全)認められた
・グレードを問わず10%以上の件数が報告された副作用は、末梢浮腫(53.8%)、悪心(23.8%)、下痢(20.8%)、および血中クレアチニン増加(13.8%)、低アルブミン血症(10.8%)、およびアミラーゼ増加(10.0%)
・11名の患者が副作用により投与中止となり、このうち、最も多く認められたのは末梢性浮腫(3.8%)だった
・コンパニオン診断薬には、MET遺伝子変異を特定するためのコンパニオン診断薬として製造販売承認されたArcher社の「Archer(R) MET コンパニオン診断システム」を使用する必要がある
・同診断システムは、血液検体及び腫瘍組織検体のどちらでも利用可能で、ともに核酸ベースの診断法を用いて検査する
2020年04月18日
術後補助化学療法にもオシメルチニブ・・・ADAURA試験、「顕著な有効性」を示す
EGFR遺伝子変異陽性の肺がん患者に対する術後補助化学療法、この分野ではLast Frontierといっていいだろう。
何度か記事として取り扱っている。
http://oitahaiganpractice.junglekouen.com/e833715.html
http://oitahaiganpractice.junglekouen.com/e900761.html
http://oitahaiganpractice.junglekouen.com/e969543.html
術後補助療法としてのオシメルチニブの有効性を検証した第III相ADAURA試験、「顕著な有効性」を示したとのこと。
しかし、手放しで喜ぶには抵抗がある。
少なくともUFTやプラチナ併用化学療法、ゲフィチニブの有効性が既に証明されている患者集団に対して、プラセボ対照臨床試験を行うことは倫理的に許されることなのか。
上記の既存治療との比較試験が新たに必要になるのならば、結局この試験、何のためにやったのか。
https://www.astrazeneca.co.jp/media/press-releases1/2020/2020041701.html
<タグリッソの第Ⅲ相ADAURA試験、EGFR遺伝子変異陽性肺がん患者さんに対する術後補助療法において顕著な有効性を示し、早期に非盲検化を予定> 2020年 4月 17日
・ADAURA試験は、肺がんの術後補助療法を対象にEGFR阻害剤を評価し、統計学的に有意かつ臨床的に意義のあるベネフィットを示した
・薬事承認申請を予定
・アストラゼネカは、4月10日、オシメルチニブが第Ⅲ相ADAURA試験において顕著な有効性を示したことにより、独立データモニタリング委員会の勧告に従って早期に非盲検化されることを発表した
・ADAURA試験は、完全腫瘍切除したIB期、II期、IIIA期の上皮成長因子受容体遺伝子変異陽性(EGFRm)非小細胞肺がん(NSCLC)患者さんを対象に術後補助療法としてのオシメルチニブの評価を行う第III相臨床試験
・第III相ADAURA試験の主要評価項目は無病生存期間
・本試験では、オシメルチニブをプラセボと比較し、最長3年の治療期間で評価した
・本試験は引き続き、副次評価項目である全生存期間の評価を行う
・なお、本試験における新たな安全上の問題は提起されなかった
ADAURA: Phase III, Double-blind, Randomized Study of Osimertinib Versus Placebo in EGFR Mutation-positive Early-stage NSCLC After Complete Surgical Resection.
Wu EL, Tsuboi M et al., Clin Lung Cancer. 2018 Jul;19(4):e533-e536
背景:
完全切除を行った後の早期非小細胞肺がん患者に対する、術後補助化学療法としてのEGFRチロシンキナーゼ阻害薬の役割は、現在検証が進んでいる段階に留まっている。多施設共同、二重盲検、無作為化、プラセボ対照臨床試験であるADAURA試験のデザインとその歴史的背景について紹介する。
患者と方法:
対象は18歳以上(日本と台湾では20歳以上)、原発性非小細胞非扁平上皮がん、病期はIB期-IIIA期、EGFR Exon 19欠失変異もしくはExon 21 L858R点突然変異を伴っている患者とした。適格患者はオシメルチニブ群(オシメルチニブ80mg/日を1日1回服用)とプラセボ群(偽薬を1日1回服用)に1:1の比率で無作為に割り付ける。プロトコール治療は、①再発が確認される、②プロトコール治療中止基準に該当する、③3年間のプロトコール治療期間を完遂する、のいずれかを満たすまで継続することとした。主要評価項目は無病生存期間とした。副次評価項目には2年無病生存割合、3年無病生存割合、5年無病生存割合、全生存期間、5年生存割合、安全性・忍容性を含めた。QoLの評価、薬力学も評価項目とした。探索的評価項目として、診断時点でT790M変異を伴っていた患者における有効性、再発後の予後、後治療、プロトコール治療開始前と再発後のリキッドバイオプシーの結果を含めた。
結果:
2015年08月から患者集積を開始し、2021年の第3四半期には結果が出ると予想される。
何度か記事として取り扱っている。
http://oitahaiganpractice.junglekouen.com/e833715.html
http://oitahaiganpractice.junglekouen.com/e900761.html
http://oitahaiganpractice.junglekouen.com/e969543.html
術後補助療法としてのオシメルチニブの有効性を検証した第III相ADAURA試験、「顕著な有効性」を示したとのこと。
しかし、手放しで喜ぶには抵抗がある。
少なくともUFTやプラチナ併用化学療法、ゲフィチニブの有効性が既に証明されている患者集団に対して、プラセボ対照臨床試験を行うことは倫理的に許されることなのか。
上記の既存治療との比較試験が新たに必要になるのならば、結局この試験、何のためにやったのか。
https://www.astrazeneca.co.jp/media/press-releases1/2020/2020041701.html
<タグリッソの第Ⅲ相ADAURA試験、EGFR遺伝子変異陽性肺がん患者さんに対する術後補助療法において顕著な有効性を示し、早期に非盲検化を予定> 2020年 4月 17日
・ADAURA試験は、肺がんの術後補助療法を対象にEGFR阻害剤を評価し、統計学的に有意かつ臨床的に意義のあるベネフィットを示した
・薬事承認申請を予定
・アストラゼネカは、4月10日、オシメルチニブが第Ⅲ相ADAURA試験において顕著な有効性を示したことにより、独立データモニタリング委員会の勧告に従って早期に非盲検化されることを発表した
・ADAURA試験は、完全腫瘍切除したIB期、II期、IIIA期の上皮成長因子受容体遺伝子変異陽性(EGFRm)非小細胞肺がん(NSCLC)患者さんを対象に術後補助療法としてのオシメルチニブの評価を行う第III相臨床試験
・第III相ADAURA試験の主要評価項目は無病生存期間
・本試験では、オシメルチニブをプラセボと比較し、最長3年の治療期間で評価した
・本試験は引き続き、副次評価項目である全生存期間の評価を行う
・なお、本試験における新たな安全上の問題は提起されなかった
ADAURA: Phase III, Double-blind, Randomized Study of Osimertinib Versus Placebo in EGFR Mutation-positive Early-stage NSCLC After Complete Surgical Resection.
Wu EL, Tsuboi M et al., Clin Lung Cancer. 2018 Jul;19(4):e533-e536
背景:
完全切除を行った後の早期非小細胞肺がん患者に対する、術後補助化学療法としてのEGFRチロシンキナーゼ阻害薬の役割は、現在検証が進んでいる段階に留まっている。多施設共同、二重盲検、無作為化、プラセボ対照臨床試験であるADAURA試験のデザインとその歴史的背景について紹介する。
患者と方法:
対象は18歳以上(日本と台湾では20歳以上)、原発性非小細胞非扁平上皮がん、病期はIB期-IIIA期、EGFR Exon 19欠失変異もしくはExon 21 L858R点突然変異を伴っている患者とした。適格患者はオシメルチニブ群(オシメルチニブ80mg/日を1日1回服用)とプラセボ群(偽薬を1日1回服用)に1:1の比率で無作為に割り付ける。プロトコール治療は、①再発が確認される、②プロトコール治療中止基準に該当する、③3年間のプロトコール治療期間を完遂する、のいずれかを満たすまで継続することとした。主要評価項目は無病生存期間とした。副次評価項目には2年無病生存割合、3年無病生存割合、5年無病生存割合、全生存期間、5年生存割合、安全性・忍容性を含めた。QoLの評価、薬力学も評価項目とした。探索的評価項目として、診断時点でT790M変異を伴っていた患者における有効性、再発後の予後、後治療、プロトコール治療開始前と再発後のリキッドバイオプシーの結果を含めた。
結果:
2015年08月から患者集積を開始し、2021年の第3四半期には結果が出ると予想される。
2020年04月18日
リキッドバイオプシーの回数制限緩和
2年ごとの診療報酬改定、個人レベルで細部を確認するのは難しい。
日経メディカルの記事を読んでいたら、こんな内容が記されていた。
引用する。
<リキッドバイオプシーを用いた肺癌のEGFR遺伝子検査が3回まで可能に> 2020/03/30
・2020年度の診療報酬改定で、リキッドバイオプシーを用いた肺癌のEGFR遺伝子検査が、3回まで実施できるようになる
・肺癌の詳細な診断及び治療法を選択する場合、又は肺癌の再発や増悪により、EGFR遺伝子変異の二次的遺伝子変異等が疑われ、再度治療法を選択する場合に、患者1人につき、診断及び治療法を選択する場合には1回、再度治療法を選択する場合には2回に限り算定できる
・EGFR遺伝子検査(血漿)について、同一の患者につき同一月において検査を2回以上実施した場合における2回目以降の当該検査の費用は、所定点数の100分の90に相当する点数により算定する
もう少し診療の流れに沿って書くと、保険診療の範囲内でのリキッドバイオプシーは、
・初回診断時は1回に限り施行可能
・オシメルチニブ以外のEGFRチロシンキナーゼ阻害薬での初回治療後に病勢進行に至り、オシメルチニブの治療を検討する場合、2回までは施行可能
→ということは、オシメルチニブ以外のEGFRチロシンキナーゼ阻害薬での初回治療後に病勢進行に至り、1回目のリキッドバイオプシーでT790M陰性だったら化学療法を行い、それでも病勢進行に至ったらもう一度リキッドバイオプシーができて、そこでT790M陽性になった場合にはオシメルチニブが使えるということだ
・オシメルチニブ以外のEGFRチロシンキナーゼ阻害薬での初回治療後に病勢進行に至り、1回目のリキッドバイオプシーでT790M陰性だったとしても、どうしても諦めきれなくて再度リキッドバイオプシーをやりたいというときは、あと1回だけ許してあげるけど、同じ月にやるんだったら病院への診療報酬を10%減らしますよ
安い検査ではないけれど、4回目以降は自己負担でやってもいいんじゃないの、という気はする。
1回25,000円で自分の運命が変わる可能性があるなら、私ならかけてみたい。
そうはいっても、リキッドバイオプシーの信頼性、それほど高くないと実感している。
先日も、明らかに多発肺転移、がん性胸膜炎、髄膜癌腫症がある患者に対して、胸水と血漿を用いたEGFR遺伝子変異検索を行ったところ、胸水からはExon 21点突然変異が検出され、血漿からは何も出てこなかった。
胸水は極めて量が少なく、肺を傷つけないように採取するのにかなりの冷や汗をかいたが、それでも採取してよかった。
リキッドバイオプシーだけでは診断しえなかったし、経気管支肺生検を行うにはさらなる覚悟が必要だった。
結局、経気管支肺生検は行わずに診断に至った。
リキッドバイオプシーは、他の手段ではEGFR遺伝子変異検索を行いえない、あるいは思うような結果が得られなかったのときの、あくまで補完的な手段として捉えておくべきだろう。
日経メディカルの記事を読んでいたら、こんな内容が記されていた。
引用する。
<リキッドバイオプシーを用いた肺癌のEGFR遺伝子検査が3回まで可能に> 2020/03/30
・2020年度の診療報酬改定で、リキッドバイオプシーを用いた肺癌のEGFR遺伝子検査が、3回まで実施できるようになる
・肺癌の詳細な診断及び治療法を選択する場合、又は肺癌の再発や増悪により、EGFR遺伝子変異の二次的遺伝子変異等が疑われ、再度治療法を選択する場合に、患者1人につき、診断及び治療法を選択する場合には1回、再度治療法を選択する場合には2回に限り算定できる
・EGFR遺伝子検査(血漿)について、同一の患者につき同一月において検査を2回以上実施した場合における2回目以降の当該検査の費用は、所定点数の100分の90に相当する点数により算定する
もう少し診療の流れに沿って書くと、保険診療の範囲内でのリキッドバイオプシーは、
・初回診断時は1回に限り施行可能
・オシメルチニブ以外のEGFRチロシンキナーゼ阻害薬での初回治療後に病勢進行に至り、オシメルチニブの治療を検討する場合、2回までは施行可能
→ということは、オシメルチニブ以外のEGFRチロシンキナーゼ阻害薬での初回治療後に病勢進行に至り、1回目のリキッドバイオプシーでT790M陰性だったら化学療法を行い、それでも病勢進行に至ったらもう一度リキッドバイオプシーができて、そこでT790M陽性になった場合にはオシメルチニブが使えるということだ
・オシメルチニブ以外のEGFRチロシンキナーゼ阻害薬での初回治療後に病勢進行に至り、1回目のリキッドバイオプシーでT790M陰性だったとしても、どうしても諦めきれなくて再度リキッドバイオプシーをやりたいというときは、あと1回だけ許してあげるけど、同じ月にやるんだったら病院への診療報酬を10%減らしますよ
安い検査ではないけれど、4回目以降は自己負担でやってもいいんじゃないの、という気はする。
1回25,000円で自分の運命が変わる可能性があるなら、私ならかけてみたい。
そうはいっても、リキッドバイオプシーの信頼性、それほど高くないと実感している。
先日も、明らかに多発肺転移、がん性胸膜炎、髄膜癌腫症がある患者に対して、胸水と血漿を用いたEGFR遺伝子変異検索を行ったところ、胸水からはExon 21点突然変異が検出され、血漿からは何も出てこなかった。
胸水は極めて量が少なく、肺を傷つけないように採取するのにかなりの冷や汗をかいたが、それでも採取してよかった。
リキッドバイオプシーだけでは診断しえなかったし、経気管支肺生検を行うにはさらなる覚悟が必要だった。
結局、経気管支肺生検は行わずに診断に至った。
リキッドバイオプシーは、他の手段ではEGFR遺伝子変異検索を行いえない、あるいは思うような結果が得られなかったのときの、あくまで補完的な手段として捉えておくべきだろう。
2020年04月17日
気管支鏡検査制限
いよいよ気管支鏡検査を制限しようという議論が真実味を持って語られ始めた。
すでに、急を要しない気管支鏡検査はできるだけ行わない、あるいは先延ばしにする流れになっている。
これだけ感染経路不明の患者が増えると、気管支鏡の対象となる患者がたまたま新型コロナウイルスキャリアだったという可能性も出てくる。
新型コロナウイルスでどうかは知らないが、結核菌では、気管支鏡の術者の感染リスクは通常の20倍ともいわれている。
術者以外にも複数の医師が介助につくことが多いので、もしその場でコロナウイルスに暴露されたら、その影響は甚大である。
しかし、肺がん疑いの患者の気管支鏡検査、「しない」とか、「延期する」とか、果たして倫理的に許されるだろうか。
以下の記事に挙げた患者は、一時は昏睡状態に陥っていたが、超音波気管支鏡下縦郭リンパ節生検でEGFR遺伝子変異陽性肺がんと診断され、オシメルチニブで治療を継続された結果、近々退院するようだ。
http://oitahaiganpractice.junglekouen.com/e971719.html
胸水や無数の多発肺転移はほぼ消失、無気肺は改善し、原発巣は劇的に縮小。
多発脳転移巣は大きさこそさほど変わらず、mid line shiftが残っているものの、病勢は制御されている様子。
何より、昏睡状態に陥っていた進行期肺がん患者が、歩いて家に帰ろうとしているというのは、一昔前ならば奇跡としか言いようがない。
まあしかし、肺がんの確定診断の80%を経皮的針生検で行う、という診療施設もあるわけで、欧米ではむしろそちらの方がスタンダードである。
これから先、経皮的針生検での検査比率を上げる医療機関が増えるかもしれない。
呼吸器内科医の仕事が減り、放射線科医の仕事が増える。
そして、いったんその流れが定着すると、新型コロナウイルスの脅威が緩和されても、元の状態に戻ることは難しいだろう。
新型コロナウイルスは、社会、経済、医療などなど、様々なシステムに変革を迫る。
厄介なことこの上ないが、この圧倒的な影響力に、宇宙の神秘を感じるのは私だけだろうか。
すでに、急を要しない気管支鏡検査はできるだけ行わない、あるいは先延ばしにする流れになっている。
これだけ感染経路不明の患者が増えると、気管支鏡の対象となる患者がたまたま新型コロナウイルスキャリアだったという可能性も出てくる。
新型コロナウイルスでどうかは知らないが、結核菌では、気管支鏡の術者の感染リスクは通常の20倍ともいわれている。
術者以外にも複数の医師が介助につくことが多いので、もしその場でコロナウイルスに暴露されたら、その影響は甚大である。
しかし、肺がん疑いの患者の気管支鏡検査、「しない」とか、「延期する」とか、果たして倫理的に許されるだろうか。
以下の記事に挙げた患者は、一時は昏睡状態に陥っていたが、超音波気管支鏡下縦郭リンパ節生検でEGFR遺伝子変異陽性肺がんと診断され、オシメルチニブで治療を継続された結果、近々退院するようだ。
http://oitahaiganpractice.junglekouen.com/e971719.html
胸水や無数の多発肺転移はほぼ消失、無気肺は改善し、原発巣は劇的に縮小。
多発脳転移巣は大きさこそさほど変わらず、mid line shiftが残っているものの、病勢は制御されている様子。
何より、昏睡状態に陥っていた進行期肺がん患者が、歩いて家に帰ろうとしているというのは、一昔前ならば奇跡としか言いようがない。
まあしかし、肺がんの確定診断の80%を経皮的針生検で行う、という診療施設もあるわけで、欧米ではむしろそちらの方がスタンダードである。
これから先、経皮的針生検での検査比率を上げる医療機関が増えるかもしれない。
呼吸器内科医の仕事が減り、放射線科医の仕事が増える。
そして、いったんその流れが定着すると、新型コロナウイルスの脅威が緩和されても、元の状態に戻ることは難しいだろう。
新型コロナウイルスは、社会、経済、医療などなど、様々なシステムに変革を迫る。
厄介なことこの上ないが、この圧倒的な影響力に、宇宙の神秘を感じるのは私だけだろうか。
2020年04月15日
EGFR遺伝子変異陽性、中枢神経系や髄膜癌腫症合併患者のためのオシメルチニブ
随分長い題名になってしまった。
オシメルチニブが中枢神経系の病変に対して効果が高いのはよく知られているところ。
http://oitahaiganpractice.junglekouen.com/e882512.html
http://oitahaiganpractice.junglekouen.com/e913700.html
http://oitahaiganpractice.junglekouen.com/e942269.html
今回は、最初から患者対象を中枢神経系への転移がある患者に絞った前向き臨床試験と、後方視的解析の報告。
全部お隣の国、韓国から。
Osimertinib in Patients With Epidermal Growth Factor Receptor Mutation-Positive Non-Small-Cell Lung Cancer and Leptomeningeal Metastases: The BLOOM Study.
Yang JCH et al., J Clin Oncol. 2020 Feb 20;38(6):538-547.
doi: 10.1200/JCO.19.00457.
目的:
今回の第I相試験(BLOOM試験)では、既存のEGFRチロシンキナーゼ阻害薬を使った治療の後に病勢進行に至った、髄膜癌腫症合併EGFR遺伝子変異陽性進行非小細胞肺がん患者を対象に、第3世代のEGFRチロシンキナーゼ阻害薬であるオシメルチニブについて評価した。
患者と方法:
腰椎穿刺による髄液細胞診により髄膜癌腫症が確認された患者を対象として、オシメルチニブ160mg/日を服用させた。評価項目は、奏効割合、奏効持続期間、無増悪生存期間、全生存期間、薬物動態、安全性とした。また、治療後の髄液細胞診所見や、神経学的症候についても評価した。測定可能病変の評価は、RECIST 1.1基準に沿って、担当医が行った。髄膜癌腫症に対する効果は、所定の判定基準(Response Assessment in Neuro-Oncology LM radiologic criteria)に沿って、効果判定委員会と担当医がそれぞれ行った。
結果:
41人の患者が登録された。効果判定委員会の評価では、髄膜癌腫症に関する奏効割合は62%(95%信頼区間は45-78%)、奏効持続期間の中央値は15.2ヶ月(95%信頼区間は7.5-17.5%)だった。担当医評価では、奏効割合は41%(95%信頼区間は26-58%)、奏効持続期間中央値は8.3ヶ月(95%信頼区間は5.6-16.5ヶ月)だった。担当医評価による無増悪生存期間中央値は、データ集積率78%の段階で8.6ヶ月(95%信頼区間は5.4-13.7ヶ月)だった。生存期間中央値は、データ集積率68%の段階で11.0ヶ月(95%信頼区間は8.0-18.0ヶ月)だった。髄液細胞診の陰性化は、40人中11人(28%、95%信頼区間は15-44%)で認められた。神経学的症候は、治療開始前に異常所見の見られた21人中12人(57%)で改善していた。有害事象と薬物動態は、既知のオシメルチニブの特性と同様だった。
Osimertinib for Patients With Leptomeningeal Metastases Associated With EGFR T790M-Positive Advanced NSCLC: The AURA Leptomeningeal Metastases Analysis.
Ahn MJ et al., J Thorac Oncol. 2020 Apr;15(4):637-648
doi: 10.1016/j.jtho.2019.12.113.
背景:
BLOOM試験において、髄膜癌腫症を合併したEGFR遺伝子変異陽性非小細胞肺がん患者に対して、オシメルチニブ160mg/日内服治療は、有望な効果を実証した。今回は、AURA拡大コホート試験、AURA2試験、AURA17試験、AURA3試験の結果から、髄膜癌腫症患者に対するオシメルチニブ80mg/日の後方視的解析を行った。
方法:
EGFR T790M耐性変異陽性で、既存のEGFRチロシンキナーゼ阻害薬による治療後に病勢進行に至った進行非小細胞肺がん患者に対して、オシメルチニブ80mg/日を投与した。神経症状がない、あるいは安定している中枢神経系病変合併患者(髄膜癌腫症を含む)を対象とした。各臨床試験参加登録時に、髄膜癌腫症の所見を認めた患者は、modified Response Assessment in Neuro-Oncology LM criteria基準に則って、効果判定委員会が治療効果判定を行った。髄膜癌腫症に関する奏効割合、奏効持続期間、無増悪生存期間、全生存期間を評価した。非中枢神経系の病変と髄膜癌腫症病変の治療効果に相関がみられるかどうか、AURA LM試験とBLOOM試験の参加者に関しては、横断的な解析を行った。
結果:
22人の患者が解析対象となった。髄膜癌腫症に対するオシメルチニブの奏効割合は55%(95%信頼区間は32-76%)だった。髄膜癌腫症に関する奏効持続期間は、中央値に達しなかった(95%信頼区間は2.8ヶ月以上)。髄膜癌腫症無増悪生存期間は11.1ヶ月(95%信頼区間は4.6ヶ月以上)、生存期間中央値は18.8ヶ月(95%信頼区間は6.3ヶ月以上)だった。非中枢神経系病変と髄膜癌腫症病変の治療への反応性は、ほぼ同等だった。
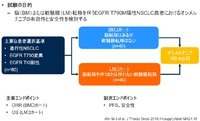
Phase II Study of 160mg of Osimertinib in EGFR T790M Positive NSCLC with Brain or Leptomeningeal Metastases Who Progressed on Prior EGFR TKI
Ahn M-J et al., WCLC 2019 Abst.#MA21.10

オシメルチニブが中枢神経系の病変に対して効果が高いのはよく知られているところ。
http://oitahaiganpractice.junglekouen.com/e882512.html
http://oitahaiganpractice.junglekouen.com/e913700.html
http://oitahaiganpractice.junglekouen.com/e942269.html
今回は、最初から患者対象を中枢神経系への転移がある患者に絞った前向き臨床試験と、後方視的解析の報告。
全部お隣の国、韓国から。
Osimertinib in Patients With Epidermal Growth Factor Receptor Mutation-Positive Non-Small-Cell Lung Cancer and Leptomeningeal Metastases: The BLOOM Study.
Yang JCH et al., J Clin Oncol. 2020 Feb 20;38(6):538-547.
doi: 10.1200/JCO.19.00457.
目的:
今回の第I相試験(BLOOM試験)では、既存のEGFRチロシンキナーゼ阻害薬を使った治療の後に病勢進行に至った、髄膜癌腫症合併EGFR遺伝子変異陽性進行非小細胞肺がん患者を対象に、第3世代のEGFRチロシンキナーゼ阻害薬であるオシメルチニブについて評価した。
患者と方法:
腰椎穿刺による髄液細胞診により髄膜癌腫症が確認された患者を対象として、オシメルチニブ160mg/日を服用させた。評価項目は、奏効割合、奏効持続期間、無増悪生存期間、全生存期間、薬物動態、安全性とした。また、治療後の髄液細胞診所見や、神経学的症候についても評価した。測定可能病変の評価は、RECIST 1.1基準に沿って、担当医が行った。髄膜癌腫症に対する効果は、所定の判定基準(Response Assessment in Neuro-Oncology LM radiologic criteria)に沿って、効果判定委員会と担当医がそれぞれ行った。
結果:
41人の患者が登録された。効果判定委員会の評価では、髄膜癌腫症に関する奏効割合は62%(95%信頼区間は45-78%)、奏効持続期間の中央値は15.2ヶ月(95%信頼区間は7.5-17.5%)だった。担当医評価では、奏効割合は41%(95%信頼区間は26-58%)、奏効持続期間中央値は8.3ヶ月(95%信頼区間は5.6-16.5ヶ月)だった。担当医評価による無増悪生存期間中央値は、データ集積率78%の段階で8.6ヶ月(95%信頼区間は5.4-13.7ヶ月)だった。生存期間中央値は、データ集積率68%の段階で11.0ヶ月(95%信頼区間は8.0-18.0ヶ月)だった。髄液細胞診の陰性化は、40人中11人(28%、95%信頼区間は15-44%)で認められた。神経学的症候は、治療開始前に異常所見の見られた21人中12人(57%)で改善していた。有害事象と薬物動態は、既知のオシメルチニブの特性と同様だった。
Osimertinib for Patients With Leptomeningeal Metastases Associated With EGFR T790M-Positive Advanced NSCLC: The AURA Leptomeningeal Metastases Analysis.
Ahn MJ et al., J Thorac Oncol. 2020 Apr;15(4):637-648
doi: 10.1016/j.jtho.2019.12.113.
背景:
BLOOM試験において、髄膜癌腫症を合併したEGFR遺伝子変異陽性非小細胞肺がん患者に対して、オシメルチニブ160mg/日内服治療は、有望な効果を実証した。今回は、AURA拡大コホート試験、AURA2試験、AURA17試験、AURA3試験の結果から、髄膜癌腫症患者に対するオシメルチニブ80mg/日の後方視的解析を行った。
方法:
EGFR T790M耐性変異陽性で、既存のEGFRチロシンキナーゼ阻害薬による治療後に病勢進行に至った進行非小細胞肺がん患者に対して、オシメルチニブ80mg/日を投与した。神経症状がない、あるいは安定している中枢神経系病変合併患者(髄膜癌腫症を含む)を対象とした。各臨床試験参加登録時に、髄膜癌腫症の所見を認めた患者は、modified Response Assessment in Neuro-Oncology LM criteria基準に則って、効果判定委員会が治療効果判定を行った。髄膜癌腫症に関する奏効割合、奏効持続期間、無増悪生存期間、全生存期間を評価した。非中枢神経系の病変と髄膜癌腫症病変の治療効果に相関がみられるかどうか、AURA LM試験とBLOOM試験の参加者に関しては、横断的な解析を行った。
結果:
22人の患者が解析対象となった。髄膜癌腫症に対するオシメルチニブの奏効割合は55%(95%信頼区間は32-76%)だった。髄膜癌腫症に関する奏効持続期間は、中央値に達しなかった(95%信頼区間は2.8ヶ月以上)。髄膜癌腫症無増悪生存期間は11.1ヶ月(95%信頼区間は4.6ヶ月以上)、生存期間中央値は18.8ヶ月(95%信頼区間は6.3ヶ月以上)だった。非中枢神経系病変と髄膜癌腫症病変の治療への反応性は、ほぼ同等だった。
Phase II Study of 160mg of Osimertinib in EGFR T790M Positive NSCLC with Brain or Leptomeningeal Metastases Who Progressed on Prior EGFR TKI
Ahn M-J et al., WCLC 2019 Abst.#MA21.10


2020年04月11日
脳転移、髄膜癌腫症とペンブロリズマブ
様々ある肺がんの合併症の中でも、厄介極まりないものに髄膜癌腫症(がん性髄膜炎)がある。
何度煮え湯を飲まされたことか。
髄膜癌腫症を発症すると、進行性の神経症状のために一気にPSが低下し、がん薬物療法の継続が困難となってしまう。
脳転移ならば、まだ放射線治療という手段があるからいいが、脳と脊髄を覆う脳脊髄腔がまとめて冒される髄膜癌腫症となると、そうはいかない。
脳神経外科に依頼して、オンマイヤーリザーバーを留置して治療することがあると教科書には載っているが、実際に見たことはない。
全脳・全脊髄照射をやっている施設もあるというが、これも実際に見たことはない。
ドライバー遺伝子変異陽性の患者なら、オシメルチニブとか、アレクチニブとかで、ある程度の効果が期待できる。
それではドライバー遺伝子変異陰性だったらどうすればいいのか、という話。
放射線治療で病巣からがん抗原を炙り出して、そこにペンブロリズマブをかませる、というのは、よいアイデアかもしれない。
それでも、TPSがそこそこ陽性の患者に絞った方が良さそうだが。
海外の第II相臨床試験の結果と、国内の症例報告について取り上げる。
どちらも興味深い話。
とくに、ドライバー遺伝子変異陰性の髄膜癌腫症の患者が症状発現後2年にわたり無増悪生存しているというのは、症例報告とは言えとても興味深い話である。
Pembrolizumab for management of patients with NSCLC and brain metastases: long-term results and biomarker analysis from a non-randomised, open-label, phase 2 trial.
Goldberg SB et al. Lancet Oncol 2020
doi: 10.1016/S1470-2045(20)30111-X.
背景:
未治療の脳転移を有する非小細胞肺がんや悪性黒色腫の患者を対象とし、中枢神経系病変に対するPD-1阻害効果を検証するため、ペンブロリズマブ単剤療法の第II相試験を行った。今回は、非小細胞肺がんコホートについての直近の分析結果を報告する。
方法:
本試験はエール大学がんセンター単施設で、オープンラベル、第II相試験として行った。18歳以上、5-20mm大の脳転移を少なくとも1か所有するIV期の非小細胞肺がん患者で、脳転移に対しては未治療もしくは放射線治療後に増悪しつつある、神経症状がない、もしくはコルチコステロイド投与を必要としない、ECOG-PS 0もしくは1の患者を対象とした。中枢神経病変の評価は、modified RECIST基準を用いて行った。参加にあたり、他臓器の病変の有無は問われなかった。患者は、ペンブロリズマブ 10mg/kgを2週間ごとに静脈内投与された。患者を2つのコホートに分けた。コホート1は、PD-L1発現が少なくとも1%以上ある患者、コホート2は、PD-L1発現が1%未満、もしくは評価不能だった患者とした。主要評価項目は脳転移巣の奏効割合(部分奏効もしくは完全奏効の患者の割合)とした。治療を受けたすべての患者を有効性および安全性の評価対象とした。現時点で、本試験の患者集積は終了している。
結果:
2014年3月31日から2018年5月21日までに、42人の患者がプロトコール治療を受けた。経過観察期間中央値は8.3ヶ月(四分位間は4.5-26.2ヶ月)だった。コホート1の患者群37人のうち、11人(29.7%、95%信頼区間は15.9-47.0%)で奏効が得られ、うち4人では完全に病巣が消失していた。病勢コントロール割合は40.5%だった。奏効持続期間中央値は5.7ヶ月だった。7人(18.9%)では、中枢神経系に加えて、その他の病巣でも奏効が得られた。無増悪生存期間中央値は1.9ヶ月、中枢神経系無増悪生存期間中央値は2.3ヶ月で、1年無増悪生存割合は33%だった。生存期間中央値は9.9ヶ月で、1年生存割合は40%、2年生存割合は34%だった。Grade 3-4の有害事象は、肺臓炎2人、構成失行1人、大腸炎1人、副腎機能障害1人、高血糖1人、高カリウム血症1人だった。深刻な有害事象は42人中6人(14%)で認め、肺臓炎2人、急性腎障害1人、大腸炎1人、高カリウム血症1人、副腎機能障害1人だった。治療関連死は認めなかった。
Whole-brain Radiation and Pembrolizumab Treatment for a Non-small-cell Lung Cancer Patient with Meningeal Carcinomatosis Lacking Driver Oncogenes Led to a Long-term Survival: A Case Report.
Nakashima K et al., Intern Med 2020
doi: 10.2169/internalmedicine.4232-19.
進行原発性肺腺癌、PD-L1 60%陽性、ドライバー遺伝子変異陰性、二次化学療法の後に突然のめまい、聴覚障害、意識障害に見舞われ、髄膜癌腫症と診断した66歳女性について報告する。全脳照射とペンブロリズマブ投与を行い、引き続く三次化学療法とペンブロリズマブの併用療法を現在も継続している。本論文を執筆した段階で、髄膜癌腫症発覚から病状の進行なく、23ヶ月が経過している。今回の経験から、全脳照射と免疫チェックポイント阻害薬の併用療法は、髄膜癌腫症を発症したドライバー遺伝子変異陰性非小細胞肺がん患者に対して効果的と考える。
何度煮え湯を飲まされたことか。
髄膜癌腫症を発症すると、進行性の神経症状のために一気にPSが低下し、がん薬物療法の継続が困難となってしまう。
脳転移ならば、まだ放射線治療という手段があるからいいが、脳と脊髄を覆う脳脊髄腔がまとめて冒される髄膜癌腫症となると、そうはいかない。
脳神経外科に依頼して、オンマイヤーリザーバーを留置して治療することがあると教科書には載っているが、実際に見たことはない。
全脳・全脊髄照射をやっている施設もあるというが、これも実際に見たことはない。
ドライバー遺伝子変異陽性の患者なら、オシメルチニブとか、アレクチニブとかで、ある程度の効果が期待できる。
それではドライバー遺伝子変異陰性だったらどうすればいいのか、という話。
放射線治療で病巣からがん抗原を炙り出して、そこにペンブロリズマブをかませる、というのは、よいアイデアかもしれない。
それでも、TPSがそこそこ陽性の患者に絞った方が良さそうだが。
海外の第II相臨床試験の結果と、国内の症例報告について取り上げる。
どちらも興味深い話。
とくに、ドライバー遺伝子変異陰性の髄膜癌腫症の患者が症状発現後2年にわたり無増悪生存しているというのは、症例報告とは言えとても興味深い話である。
Pembrolizumab for management of patients with NSCLC and brain metastases: long-term results and biomarker analysis from a non-randomised, open-label, phase 2 trial.
Goldberg SB et al. Lancet Oncol 2020
doi: 10.1016/S1470-2045(20)30111-X.
背景:
未治療の脳転移を有する非小細胞肺がんや悪性黒色腫の患者を対象とし、中枢神経系病変に対するPD-1阻害効果を検証するため、ペンブロリズマブ単剤療法の第II相試験を行った。今回は、非小細胞肺がんコホートについての直近の分析結果を報告する。
方法:
本試験はエール大学がんセンター単施設で、オープンラベル、第II相試験として行った。18歳以上、5-20mm大の脳転移を少なくとも1か所有するIV期の非小細胞肺がん患者で、脳転移に対しては未治療もしくは放射線治療後に増悪しつつある、神経症状がない、もしくはコルチコステロイド投与を必要としない、ECOG-PS 0もしくは1の患者を対象とした。中枢神経病変の評価は、modified RECIST基準を用いて行った。参加にあたり、他臓器の病変の有無は問われなかった。患者は、ペンブロリズマブ 10mg/kgを2週間ごとに静脈内投与された。患者を2つのコホートに分けた。コホート1は、PD-L1発現が少なくとも1%以上ある患者、コホート2は、PD-L1発現が1%未満、もしくは評価不能だった患者とした。主要評価項目は脳転移巣の奏効割合(部分奏効もしくは完全奏効の患者の割合)とした。治療を受けたすべての患者を有効性および安全性の評価対象とした。現時点で、本試験の患者集積は終了している。
結果:
2014年3月31日から2018年5月21日までに、42人の患者がプロトコール治療を受けた。経過観察期間中央値は8.3ヶ月(四分位間は4.5-26.2ヶ月)だった。コホート1の患者群37人のうち、11人(29.7%、95%信頼区間は15.9-47.0%)で奏効が得られ、うち4人では完全に病巣が消失していた。病勢コントロール割合は40.5%だった。奏効持続期間中央値は5.7ヶ月だった。7人(18.9%)では、中枢神経系に加えて、その他の病巣でも奏効が得られた。無増悪生存期間中央値は1.9ヶ月、中枢神経系無増悪生存期間中央値は2.3ヶ月で、1年無増悪生存割合は33%だった。生存期間中央値は9.9ヶ月で、1年生存割合は40%、2年生存割合は34%だった。Grade 3-4の有害事象は、肺臓炎2人、構成失行1人、大腸炎1人、副腎機能障害1人、高血糖1人、高カリウム血症1人だった。深刻な有害事象は42人中6人(14%)で認め、肺臓炎2人、急性腎障害1人、大腸炎1人、高カリウム血症1人、副腎機能障害1人だった。治療関連死は認めなかった。
Whole-brain Radiation and Pembrolizumab Treatment for a Non-small-cell Lung Cancer Patient with Meningeal Carcinomatosis Lacking Driver Oncogenes Led to a Long-term Survival: A Case Report.
Nakashima K et al., Intern Med 2020
doi: 10.2169/internalmedicine.4232-19.
進行原発性肺腺癌、PD-L1 60%陽性、ドライバー遺伝子変異陰性、二次化学療法の後に突然のめまい、聴覚障害、意識障害に見舞われ、髄膜癌腫症と診断した66歳女性について報告する。全脳照射とペンブロリズマブ投与を行い、引き続く三次化学療法とペンブロリズマブの併用療法を現在も継続している。本論文を執筆した段階で、髄膜癌腫症発覚から病状の進行なく、23ヶ月が経過している。今回の経験から、全脳照射と免疫チェックポイント阻害薬の併用療法は、髄膜癌腫症を発症したドライバー遺伝子変異陰性非小細胞肺がん患者に対して効果的と考える。
2020年04月07日
小細胞肺がん二次治療としてのアムルビシン単剤療法の効果
ひとつ前の記事で、Lubrinectedinのことを書いていて、そういえば小細胞肺がん二次治療におけるアムルビシンのことをまとめていなかったなと気が付いた。
肺がん診療ガイドラインを眺めて、我が国のアムルビシン療法の背景になっている論文の要約をまとめてみた。
奏効割合30%強、無増悪生存期間中央値3ヶ月強、生存期間中央値9ヶ月そこそこ、というのは、アムルビシンもLubrinectedinもいい勝負という気がする。
もしかしたら、Lubrinectedinは我が国ではもう少し良い成績を残すかもしれないが。
A single-arm confirmatory study of amrubicin therapy in patients with refractory small-cell lung cancer: Japan Clinical Oncology Group Study (JCOG0901).
Murakami H et al., Lung Cancer 2014
doi: 10.1016/j.lungcan.2014.01.012.
目的:
治療抵抗性(refractory relapse)再発小細胞がんの患者を対象に、トポイソメラーゼII阻害薬であるアムルビシン単剤療法の有効性と安全性を、オープンラベル多施設共同単アーム臨床試験で検証した。
患者と方法:
化学療法抵抗性となった小細胞肺がん患者を対象に、アムルビシン40mg/㎡を3日間連続で投与し、21日間サイクルで繰り返した。主要評価項目は奏効割合とし、副次評価項目は無増悪生存期間、全生存期間、安全性とした。
結果:
2009年11月から2011年2月にかけて、82人の患者を登録した。アムルビシンの治療コース数の中央値は4コース(1-22コース)だった。奏効割合は32.9%で、95%信頼区間は22.9-44.2%だった。無増悪生存期間中央値は3.5ヶ月(95%信頼区間は3.0ヶ月-4.3ヶ月)、全生存期間中央値は8.9ヶ月(95%信頼区間は7.6ヶ月-11.3ヶ月)だった。過去にエトポシドの治療を受けたことがあるかないかで、奏効割合(21.4% vs 45.0%、p=0.034)、無増悪生存期間(2.9ヶ月 vs 5.1ヶ月、p=0.0009)、全生存期間(7.9ヶ月 vs 13.1ヶ月、p=0.0128)に有意差が見られた。好中球減少は最も頻度の高い有害事象(93.9%)であり、発熱性好中球減少も26.8%で認めた。治療関連死はなかった。
結論:
アムルビシン単剤療法は、再発小細胞がんに対する効果的かつ安全な治療オプションとして検討されるべき治療である。エトポシドによる前治療歴がアムルビシンの効果に影響を与えている可能性がある。
Amrubicin for relapsed small-cell lung cancer: a systematic review and meta-analysis of 803 patients.
Horita N.et al., Sci Rep 2016
doi: 10.1038/srep18999.
現在我が国では、アムルビシンは再発小細胞肺がんに対してのみ適用が認められている。これまでの報告では、アムルビシンの効果と副作用にはかなりの幅がある。今回のシステマティック・レビューとメタアナリシスにおいて、対象とした臨床試験の適格基準は、小細胞がんの患者に対する二次治療として、アムルビシン単剤療法の有効性と安全性を検討した臨床試験であり、生データを参照できる前向き臨床試験とした。9件の臨床試験、803人の患者を対象とした。3ヶ月無増悪生存割合は63%(95%信頼区間は57-69%)、6ヶ月無増悪生存割合は28%(95%信頼区間は21-35%)、9ヶ月無増悪生存割合は10%(95%信頼区間は6-14%)だった。また、6ヶ月生存割合は69%(95%信頼区間は61-78%)、12ヶ月生存割合は36%(95%信頼区間は28-44%)、18ヶ月生存割合は15%(95%信頼区間は8-21%)だった。Grade 3-4の好中球減少を70%で、発熱性好中球減少を12%で認めた。
肺がん診療ガイドラインを眺めて、我が国のアムルビシン療法の背景になっている論文の要約をまとめてみた。
奏効割合30%強、無増悪生存期間中央値3ヶ月強、生存期間中央値9ヶ月そこそこ、というのは、アムルビシンもLubrinectedinもいい勝負という気がする。
もしかしたら、Lubrinectedinは我が国ではもう少し良い成績を残すかもしれないが。
A single-arm confirmatory study of amrubicin therapy in patients with refractory small-cell lung cancer: Japan Clinical Oncology Group Study (JCOG0901).
Murakami H et al., Lung Cancer 2014
doi: 10.1016/j.lungcan.2014.01.012.
目的:
治療抵抗性(refractory relapse)再発小細胞がんの患者を対象に、トポイソメラーゼII阻害薬であるアムルビシン単剤療法の有効性と安全性を、オープンラベル多施設共同単アーム臨床試験で検証した。
患者と方法:
化学療法抵抗性となった小細胞肺がん患者を対象に、アムルビシン40mg/㎡を3日間連続で投与し、21日間サイクルで繰り返した。主要評価項目は奏効割合とし、副次評価項目は無増悪生存期間、全生存期間、安全性とした。
結果:
2009年11月から2011年2月にかけて、82人の患者を登録した。アムルビシンの治療コース数の中央値は4コース(1-22コース)だった。奏効割合は32.9%で、95%信頼区間は22.9-44.2%だった。無増悪生存期間中央値は3.5ヶ月(95%信頼区間は3.0ヶ月-4.3ヶ月)、全生存期間中央値は8.9ヶ月(95%信頼区間は7.6ヶ月-11.3ヶ月)だった。過去にエトポシドの治療を受けたことがあるかないかで、奏効割合(21.4% vs 45.0%、p=0.034)、無増悪生存期間(2.9ヶ月 vs 5.1ヶ月、p=0.0009)、全生存期間(7.9ヶ月 vs 13.1ヶ月、p=0.0128)に有意差が見られた。好中球減少は最も頻度の高い有害事象(93.9%)であり、発熱性好中球減少も26.8%で認めた。治療関連死はなかった。
結論:
アムルビシン単剤療法は、再発小細胞がんに対する効果的かつ安全な治療オプションとして検討されるべき治療である。エトポシドによる前治療歴がアムルビシンの効果に影響を与えている可能性がある。
Amrubicin for relapsed small-cell lung cancer: a systematic review and meta-analysis of 803 patients.
Horita N.et al., Sci Rep 2016
doi: 10.1038/srep18999.
現在我が国では、アムルビシンは再発小細胞肺がんに対してのみ適用が認められている。これまでの報告では、アムルビシンの効果と副作用にはかなりの幅がある。今回のシステマティック・レビューとメタアナリシスにおいて、対象とした臨床試験の適格基準は、小細胞がんの患者に対する二次治療として、アムルビシン単剤療法の有効性と安全性を検討した臨床試験であり、生データを参照できる前向き臨床試験とした。9件の臨床試験、803人の患者を対象とした。3ヶ月無増悪生存割合は63%(95%信頼区間は57-69%)、6ヶ月無増悪生存割合は28%(95%信頼区間は21-35%)、9ヶ月無増悪生存割合は10%(95%信頼区間は6-14%)だった。また、6ヶ月生存割合は69%(95%信頼区間は61-78%)、12ヶ月生存割合は36%(95%信頼区間は28-44%)、18ヶ月生存割合は15%(95%信頼区間は8-21%)だった。Grade 3-4の好中球減少を70%で、発熱性好中球減少を12%で認めた。
2020年04月07日
小細胞肺癌二次治療におけるLurbinectedin
ASCO 2019で報告されていたLurbinectedinの第2相試験、論文化されていた。
今回は単剤としての治療効果の報告だが、何故か現在進行中の第3相試験は、ドキソルビシンとの併用療法としての効果を検証するものらしい。
ドキソルビシンにこだわるところが、いかにも欧州主導の小細胞がん関連臨床試験、という薫りがする。
sensitive relapse症例におけるPEI療法やノギテカン単剤、アムルビシン単剤療法との比較試験、refractory relapse症例におけるアムルビシンとの比較試験など、見てみたいところ。
http://oitahaiganpractice.junglekouen.com/e815982.html
http://oitahaiganpractice.junglekouen.com/e972856.html
また、小細胞肺癌の患者の中には、例えば限局型小細胞肺癌で、化学放射線療法後に再燃した患者であるとか、PS不良のためにアテゾリズマブが併用できなかった患者もいるが、こうした患者に対して二次治療以降で免疫チェックポイント阻害薬の出番はあるのだろうか。
確か、米国食品医薬品局では、三次治療以降のニボルマブは承認されていたように思うのだが、我が国ではどんな議論が進んでいるのだろうか。
http://oitahaiganpractice.junglekouen.com/e940275.html
それから、Rova-Tはどうなったんだろう・・・。
http://oitahaiganpractice.junglekouen.com/e913905.html
http://oitahaiganpractice.junglekouen.com/e858706.html
Lurbinectedin as second-line treatment for patients with small-cell lung cancer: a single-arm, open-label, phase 2 basket trial
Paz-Ares et al., ASCO 2019 Abst.#8506
José Trigo, MD et al., Lancet Oncol 2020
DOI:https://doi.org/10.1016/S1470-2045(20)30068-1
背景:
初回化学療法が無効中止となった後の小細胞癌に対する治療選択肢はほとんどない。Lurbinectedinはがん化に関わる転写因子を選択的に阻害する薬である。今回の第2相臨床試験において、プラチナ併用化学療法後に病勢進行に至った小細胞肺癌患者に対するLurbinectedinの活性と安全性について評価した。
方法:
今回の単アーム、オープンラベル、第2相バスケット臨床試験において、欧州6か国と米国の26施設から患者を集積した。
患者適格基準は、
・18歳以上
・病理学的に小細胞肺癌と確定診断されている
・ECOG-PSは2以下
・RECIST ver.1.1基準に合致する測定可能病変を有する
・脳転移がない
・臓器機能が保たれている
・前治療として1レジメンだけ化学療法がおこなわれており、最終投与から少なくとも3週間は経過している
こととした。免疫チェックポイント阻害薬の治療歴は可とした。
病勢進行もしくは毒性による中止に至るまで、体表面積1㎡あたり3.2mgのlurbinectedinを3週間に1度、1時間の時間をかけて投与した。主要評価項目は、RECIST 1.1基準に則った奏効割合とした。治療を受けた全ての患者は、有効性と安全性の評価対象となった。本試験は現在も継続中である(ClinicalTrials.gov, NCT02454972)
結果:
2015年10月16日から2019年1月15日にかけて、105人の患者が登録され、lurbinectedinの投与を受けた。経過観察期間中央値は17.1ヶ月(四分位区間は6.5-25.3ヶ月)だった。奏効割合は35.2%(95%信頼区間は26.2-45.2%)だった。 頻度の高いGrade 3-4の有害事象は、貧血(9%)、白血球減少(29%)、好中球減少(46%)、血小板減少(7%)だった。治療関連の深刻な有害事象は、11人(10%)で認められ、好中球減少、発熱性好中球減少が5人ずつ発生で最も多かった。治療関連死は認めなかった。



結果の解釈:
Lurbinectedinは小細胞癌に対する二次化学療法として、腫瘍縮小効果と受容・対処可能な毒性プロファイルを併せ持つ有望な薬と考えられた。lurbinectedinは、とりわけ初回治療後の再燃時には有効な治療オプションが乏しい小細胞肺がんにあって新たな可能性を秘めた治療であり、現在はドキソルビシン併用での二次治療として第3相臨床試験が進行中である。
今回は単剤としての治療効果の報告だが、何故か現在進行中の第3相試験は、ドキソルビシンとの併用療法としての効果を検証するものらしい。
ドキソルビシンにこだわるところが、いかにも欧州主導の小細胞がん関連臨床試験、という薫りがする。
sensitive relapse症例におけるPEI療法やノギテカン単剤、アムルビシン単剤療法との比較試験、refractory relapse症例におけるアムルビシンとの比較試験など、見てみたいところ。
http://oitahaiganpractice.junglekouen.com/e815982.html
http://oitahaiganpractice.junglekouen.com/e972856.html
また、小細胞肺癌の患者の中には、例えば限局型小細胞肺癌で、化学放射線療法後に再燃した患者であるとか、PS不良のためにアテゾリズマブが併用できなかった患者もいるが、こうした患者に対して二次治療以降で免疫チェックポイント阻害薬の出番はあるのだろうか。
確か、米国食品医薬品局では、三次治療以降のニボルマブは承認されていたように思うのだが、我が国ではどんな議論が進んでいるのだろうか。
http://oitahaiganpractice.junglekouen.com/e940275.html
それから、Rova-Tはどうなったんだろう・・・。
http://oitahaiganpractice.junglekouen.com/e913905.html
http://oitahaiganpractice.junglekouen.com/e858706.html
Lurbinectedin as second-line treatment for patients with small-cell lung cancer: a single-arm, open-label, phase 2 basket trial
Paz-Ares et al., ASCO 2019 Abst.#8506
José Trigo, MD et al., Lancet Oncol 2020
DOI:https://doi.org/10.1016/S1470-2045(20)30068-1
背景:
初回化学療法が無効中止となった後の小細胞癌に対する治療選択肢はほとんどない。Lurbinectedinはがん化に関わる転写因子を選択的に阻害する薬である。今回の第2相臨床試験において、プラチナ併用化学療法後に病勢進行に至った小細胞肺癌患者に対するLurbinectedinの活性と安全性について評価した。
方法:
今回の単アーム、オープンラベル、第2相バスケット臨床試験において、欧州6か国と米国の26施設から患者を集積した。
患者適格基準は、
・18歳以上
・病理学的に小細胞肺癌と確定診断されている
・ECOG-PSは2以下
・RECIST ver.1.1基準に合致する測定可能病変を有する
・脳転移がない
・臓器機能が保たれている
・前治療として1レジメンだけ化学療法がおこなわれており、最終投与から少なくとも3週間は経過している
こととした。免疫チェックポイント阻害薬の治療歴は可とした。
病勢進行もしくは毒性による中止に至るまで、体表面積1㎡あたり3.2mgのlurbinectedinを3週間に1度、1時間の時間をかけて投与した。主要評価項目は、RECIST 1.1基準に則った奏効割合とした。治療を受けた全ての患者は、有効性と安全性の評価対象となった。本試験は現在も継続中である(ClinicalTrials.gov, NCT02454972)
結果:
2015年10月16日から2019年1月15日にかけて、105人の患者が登録され、lurbinectedinの投与を受けた。経過観察期間中央値は17.1ヶ月(四分位区間は6.5-25.3ヶ月)だった。奏効割合は35.2%(95%信頼区間は26.2-45.2%)だった。 頻度の高いGrade 3-4の有害事象は、貧血(9%)、白血球減少(29%)、好中球減少(46%)、血小板減少(7%)だった。治療関連の深刻な有害事象は、11人(10%)で認められ、好中球減少、発熱性好中球減少が5人ずつ発生で最も多かった。治療関連死は認めなかった。



結果の解釈:
Lurbinectedinは小細胞癌に対する二次化学療法として、腫瘍縮小効果と受容・対処可能な毒性プロファイルを併せ持つ有望な薬と考えられた。lurbinectedinは、とりわけ初回治療後の再燃時には有効な治療オプションが乏しい小細胞肺がんにあって新たな可能性を秘めた治療であり、現在はドキソルビシン併用での二次治療として第3相臨床試験が進行中である。
2020年04月07日
「病院はホテルじゃない」から、「ホテルは病院じゃない」へ
新型コロナウイルス感染症の拡大に伴い、7都府県に限定された形ではあるが、近々に緊急事態宣言が発出される見通しとなった。
2020/04/07に発出、2020/04/08に発効する見通しとのこと。
これを受けて、直ちに小池都知事は、発効後に緊急事態措置を開始すると記者会見で述べた。
東京都だけでなく、病床を含めた医療資源の不足が深刻化している。
いよいよ、無症状者・軽症者は病院では賄いきれなくなり、東京都は東京駅近くの東横インの協力を得て、まずは200床のホテル客室を確保し、そこに無症状者・軽症者を移動させる見通しとのこと。
ふと思い出すことがある。
関東で修行をしてからやがて15年がたとうとしているが、当時の私にとって大きなカルチャーショックだったことだ。
それは、
「病院はホテルではないんですよ」
「どうしても退院して自宅に帰るのが嫌だということであれば、近在のホテルや旅館を利用してください」
と、退院予定日を控えながら、退院を渋っている患者さん・ご家族への、指導医の言葉だった。
理性では理解できる。
がん専門施設において、呼吸器内科が利用できる病床数には限りがあり、できるだけ多くの患者さんに均等に治療を提供しようとするならば、医学的に退院可能となった患者さんを漫然と入院させておくべきではない。
それは、他の患者さんの治療の遅延、場合によっては他の患者さんの治療機会の逸失を招きかねない。
とは言いながらも、自分の担当患者に対して、
「病院はホテルではないんです」
と断じる姿は、ある種の衝撃だった。
それから約15年。
肺がん内科診療の世界でも外来治療が主流となり、こうしたやり取りは以前よりも減ったのかも知れない。
いや、もしかしたら、入院治療を希望する患者さんに対して外来治療を勧めるにあたって、
「病院はホテルではないんです」
「どうしても外来で治療を受けるのが嫌だということであれば、近在のホテルや旅館に滞在して、治療後に病状が悪化したら受診してください」
といった説明が、今でも行われているのかも知れない。
そして今、ホテル関係者からすれば(私の実家は旅館なので、あながち無関係ではない)、
「ホテルは病院ではないんですよ」
と言いたくなるような状況が出現している。
政治の要請で、新型コロナウイルス感染患者を受け入れた、ホテル三日月や東横イン経営者の英断に敬意を表する。
風評被害を考えると、並大抵の度量ではできないことだ。
私が実家の旅館に無症候性キャリア、軽症者の受け入れを要請されたとしても、簡単には決断できないだろう。
親や、実家に出入りする高齢の親族が感染し、命を落とすようなことになれば、悔やんでも悔やみきれない。
医療従事者は、人々の健康のために奉仕するという職業倫理を以て業務にあたっているのでまだしもだが、宿泊施設の業務に従事する人は、決してそうではないのだ。
果たして、大分県内の宿泊施設のうち、どの程度が県や市町村の要請に応じて、客室を拠出することができるだろうか。
そして、現場での肌感覚として感じることだが、新型コロナウイルス感染症流行地域への目に見えない差別意識は、確実にある。
私の勤務先がある市町村でも新型コロナウイルス感染者が報告されているが、他の市町村にある病院から、転院受け入れを差し控えたい、という声が聞こえてきている。
転院調整をしている当の患者は、もともとは先方から難治性の病態に対してなんとか治療をしてほしい、との要請を受けて対応した患者であるにも関わらず、である。
当院でクラスター感染が発生しているならまだしもだが、こうした態度は医療機関相互の関係に、後々禍根を残しかねない。
新型コロナウイルス感染症にあまりにも気を取られて、悪性新生物や心疾患、脳血管疾患、一般の肺炎といった日本人の死因の上位を占める疾患の診療がおろそかになれば、より深刻な事態を招くことだろう。
2020/04/07に発出、2020/04/08に発効する見通しとのこと。
これを受けて、直ちに小池都知事は、発効後に緊急事態措置を開始すると記者会見で述べた。
東京都だけでなく、病床を含めた医療資源の不足が深刻化している。
いよいよ、無症状者・軽症者は病院では賄いきれなくなり、東京都は東京駅近くの東横インの協力を得て、まずは200床のホテル客室を確保し、そこに無症状者・軽症者を移動させる見通しとのこと。
ふと思い出すことがある。
関東で修行をしてからやがて15年がたとうとしているが、当時の私にとって大きなカルチャーショックだったことだ。
それは、
「病院はホテルではないんですよ」
「どうしても退院して自宅に帰るのが嫌だということであれば、近在のホテルや旅館を利用してください」
と、退院予定日を控えながら、退院を渋っている患者さん・ご家族への、指導医の言葉だった。
理性では理解できる。
がん専門施設において、呼吸器内科が利用できる病床数には限りがあり、できるだけ多くの患者さんに均等に治療を提供しようとするならば、医学的に退院可能となった患者さんを漫然と入院させておくべきではない。
それは、他の患者さんの治療の遅延、場合によっては他の患者さんの治療機会の逸失を招きかねない。
とは言いながらも、自分の担当患者に対して、
「病院はホテルではないんです」
と断じる姿は、ある種の衝撃だった。
それから約15年。
肺がん内科診療の世界でも外来治療が主流となり、こうしたやり取りは以前よりも減ったのかも知れない。
いや、もしかしたら、入院治療を希望する患者さんに対して外来治療を勧めるにあたって、
「病院はホテルではないんです」
「どうしても外来で治療を受けるのが嫌だということであれば、近在のホテルや旅館に滞在して、治療後に病状が悪化したら受診してください」
といった説明が、今でも行われているのかも知れない。
そして今、ホテル関係者からすれば(私の実家は旅館なので、あながち無関係ではない)、
「ホテルは病院ではないんですよ」
と言いたくなるような状況が出現している。
政治の要請で、新型コロナウイルス感染患者を受け入れた、ホテル三日月や東横イン経営者の英断に敬意を表する。
風評被害を考えると、並大抵の度量ではできないことだ。
私が実家の旅館に無症候性キャリア、軽症者の受け入れを要請されたとしても、簡単には決断できないだろう。
親や、実家に出入りする高齢の親族が感染し、命を落とすようなことになれば、悔やんでも悔やみきれない。
医療従事者は、人々の健康のために奉仕するという職業倫理を以て業務にあたっているのでまだしもだが、宿泊施設の業務に従事する人は、決してそうではないのだ。
果たして、大分県内の宿泊施設のうち、どの程度が県や市町村の要請に応じて、客室を拠出することができるだろうか。
そして、現場での肌感覚として感じることだが、新型コロナウイルス感染症流行地域への目に見えない差別意識は、確実にある。
私の勤務先がある市町村でも新型コロナウイルス感染者が報告されているが、他の市町村にある病院から、転院受け入れを差し控えたい、という声が聞こえてきている。
転院調整をしている当の患者は、もともとは先方から難治性の病態に対してなんとか治療をしてほしい、との要請を受けて対応した患者であるにも関わらず、である。
当院でクラスター感染が発生しているならまだしもだが、こうした態度は医療機関相互の関係に、後々禍根を残しかねない。
新型コロナウイルス感染症にあまりにも気を取られて、悪性新生物や心疾患、脳血管疾患、一般の肺炎といった日本人の死因の上位を占める疾患の診療がおろそかになれば、より深刻な事態を招くことだろう。
2020年04月05日
新型コロナウイルス感染症対策として、サージカルマスクは有効なのか?
2020/04/04の記事では、非感染性(論文では、塩化ナトリウムを含む微粒子と記載されていた)の人工微粒子をどの程度マスクが遮断できるかということで、ガーゼマスクは97%、医療用マスク(サージカルマスク)でさえも44%の人工微粒子を透過させてしまうと記載した。
http://oitahaiganpractice.junglekouen.com/e972744.html
言い方を変えれば、ガーゼマスクの微粒子遮断効果はわずか3%、医療用マスクの遮断効果は56%と見ることもでき、その差は歴然である。
では、44%の微粒子透過を許してしまうサージカルマスク、医学的(ウイルス学的)な見地から見れば、どの程度感染者からのウイルス粒子飛散を抑制することができるのか。
それを検証したのが本報告である。
NHKのニュースで取り扱われていたので、論文を検索して読んでみた。
本試験は、WHO、香港大学、ハーバード大学、メリーランド大学の共同研究として、2013年の3月から2016年の5月にかけて、香港のある私立病院で、外来患者を対象に行われた。
当初はインフルエンザ感染を主な対象として、試験後半ではその他のウイルスも対象として試験が行われ、少数ながらコロナウイルス感染症者も対象に含まれていたために、たまたま今回のCoVID-19 pandemicにfitする報告となった。
今回の記事では、煩雑になるため細かい方法は記載しなかったが、試験参加者にはインフルエンザ迅速検査が無償で行われること、30分かかる呼気サンプル採取に協力したら1回あたり30$相当の商品券をもらえること、さらに参加者全員に20$相当の体温計が提供されることになっていたことなどが記されていた。結果として、サージカルマスクをしたときとしないときの2回のサンプル採取に1時間以上をかけて協力し、60$相当の商品券と20$相当の体温計を受け取った49人から得られたデータが、我々に最も示唆を与える結果を提供してくれることになった。
少ないサンプル数での検討なのでどこまで信頼性、再現性が担保されるのかわからないが、ウイルスによってこれだけサージカルマスクの有効性が異なるのかと、いささか驚いた。
コロナウイルス感染症患者にサージカルマスクを装着させた場合、今回の報告では完全にウイルス拡散を抑制できたわけであり、かなりのウイルス拡散抑制効果が期待できそうだ。
一方、インフルエンザウイルスやライノウイルスのエアロゾルに対しては、サージカルマスクはあまり意味がないことも示されていた。
また、咳症状のないコロナウイルス感染患者の飛沫サンプル、エアロゾルサンプルからはコロナウイルスは検出されなかったとのことだが、これは巷で言われているようなSARS-CoV-2の特性(無症状キャリアからも拡散しうる)とは異なる。
SARS-CoV-2感染が確認され、咳症状を伴う患者にサージカルマスク着用を義務付けるのは必須といっていいが、咳症状を伴わない患者からウイルス拡散を抑止する目的で、あるいは一般健常者(中にはSARS-CoV-2キャリアも含む)が知らないうちにウイルスを拡散させることを防止する目的でサージカルマスクを着用するかどうかは、サージカルマスクの資源量とのトレード・オフとなる。
いずれにせよ、サージカルマスク着用の目的は、自分を他者から拡散されるウイルスから守ることではない(少なくとも、そうした効果は科学的に検証されていない)ことは誰もが知っておくべきであり、絶対的にサージカルマスクが不足している現状では、感染者に対応している医療現場や、これから患者受け入れを開始する宿泊施設等へ優先的にサージカルマスクを供給するべきである。
Respiratory virus shedding in exhaled breath and efficacy of face masks
Nancy H. L. Leung. et al., Nat Med 2020
https://doi.org/10.1038/s41591-020-0843-2
呼吸器系のウイルス感染症は、呼吸器ウイルス疾患、あるいは「風邪」とひとくくりに語られる症候群を引き起こす。こうした呼吸器ウイルス疾患はおしなべて軽症であることが多いが、ときに重篤・致死的になることもある。原因となるウイルスは、ヒト-ヒト間で直接・間接の接触、気道系飛沫(発生源から直ちに地面へ落下する比較的大きな飛沫から、直径>5μmの大きめのエアロゾル)、微粒子エアロゾル(直径≦5μmの飛沫・飛沫核)を介して広がっていく。接触感染を予防する目的での手指衛生、気道系飛沫を介しての感染を予防する目的でのマスク着用は、インフルエンザ拡散を緩和する対策として重要とされてきた一方で、他の呼吸器疾患ウイルスの拡散予防策としてどうなのかはあまり知られていない。このことは、CoVID-19に関しても同様である。
いくつかの保健政策当局は、個々の患者から感染が広がることを予防するために、患者にマスクを着用させることを推奨している。医療現場で使用される、いわゆるサージカルマスクは、本来は外科医が患者の創部に細菌を持ち込まないようにするため、患者を術後感染合併症から守るための予防手段として現場に持ち込まれたものである。後に、患者から医療者への二次感染を予防する手段としても利用されるようになった。しかしながら、マスクの科学的有効性を検証した報告は、非感染性の飛沫をどの程度フィルターとして遮断できるかという物理的な実験に基づくものがほとんどであり、呼吸器疾患ウイルスを含む飛沫遮断策として有効かどうかまで一般化することは難しい。呼吸器疾患ウイルスの遮断効果、呼吸器感染症に罹患した患者からのウイルス拡散をどの程度医療用マスクが遮断するかについては情報が乏しく、それもインフルエンザウイルスに関する報告がほとんどである。
今回は、コロナウイルス、インフルエンザウイルス、ライノウイルスについて、飛沫やエアロゾルが感染拡大にどの程度重要なのかを検証した。急性呼吸器ウイルス感染症に罹患した患者を対象として、その呼気中に含まれるウイルス量を測定し、サージカルマスクのウイルス拡散抑制効果を検討した。
3,363人の患者をスクリーニングし、最終的に246人の患者を呼気サンプル提供者として登録した。122人(50%)は呼気サンプル採取時にサージカルマスクを着用しない群(非マスク群)とし、124人(50%)はサージカルマスクを着用する群(マスク群)とした。そのうち、49人(20%)の患者は、マスクを着用したとき、しなかったときの両方で呼気サンプルを採取させてくれた。
RT-PCRにより、少なくとも1種類の呼吸器疾患ウイルスが同定されたのは246人中123人(50%)だった。そのうち111人(90%)は、季節性コロナウイルス17人、インフルエンザウイルス43人、ライノウイルス54人で占められており、その中にはコロナウイルスとインフルエンザウイルスの重複感染が1人、ライノウイルスとインフルエンザウイルスの重複感染が2人含まれていた。この111人が、今回の調査対象となった。
この3種のウイルス感染症患者の間には、ちょっとした背景の違いがあった。全体の24%の患者で37.8℃以上の発熱を認めたが、コロナウイルス感染者とライノウイルス感染者の合計よりも、インフルエンザウイルス感染者の方が発熱患者が2倍以上多かった。コロナウイルス感染者は咳を伴うことが最も多く、30分間の呼気採取時間の間に平均17回咳をしていた。無作為化された非マスク群とマスク群の背景は同等だった。
患者の鼻腔擦過サンプル、咽頭擦過サンプル、飛沫サンプル、エアロゾルサンプル中のウイルス量を測定した。飛沫サンプルとエアロゾルサンプルについてはマスクをした状態、あるいはしなかった状態で採取し、比較した。平均して、ウイルス量は咽頭擦過サンプルよりも鼻腔擦過サンプルの方が多かった(コロナウイルス:8.1 vs 3.9、インフルエンザウイルス:6.7 vs 4.0、ライノウイルス:6.8 vs 3.3、単位はlog10ウイルスコピー数)。ウイルスRNAは、飛沫サンプルあるいはエアロゾルサンプルにおいて、3種全てのウイルスで同定され、コロナウイルス、インフルエンザウイルス、ライノウイルスの順で述べると、マスクをしない状態では飛沫サンプルのそれぞれ30%、26%、28%で、エアロゾルサンプルのそれぞれ40%、35%、56%で検出された。
コロナウイルスに関して言えば、OC43株とHKU1株は飛沫サンプル、エアロゾルサンプルの両方から検出されたが、NL63株はエアロゾルサンプルのみから検出され、飛沫サンプルからは検出されなかった。非マスク群の飛沫サンプル10件のうち3件(30%)から、エアロゾルサンプル10件のうち4件(40%)からウイルスが検出されたが、マスク群では飛沫サンプル、エアロゾルサンプルいずれからも全くウイルスは検出されなかった。統計学的には、サージカルマスク着用により、エアロゾルサンプルからのコロナウイルス検出を有意に抑えることができ(p=0.04)、飛沫サンプルからも抑制される傾向が見られた(p=0.07)。
インフルエンザウイルスでは、非マスク群の飛沫サンプル23件のうち6件(26%)から、エアロゾルサンプル23件のうち8件(35%)からウイルスが検出されたが、マスク群のサンプルでは飛沫サンプル27件のうち1件(4%)から、エアロゾルサンプル27件のうち6件(22%)からウイルスが検出された。さらに言えば、非マスク群のエアロゾルサンプルからウイルスが検出された8件について、そのうちの5件ではウイルス培養を行い、そのうち4件で培養陽性となった。マスク群のエアロゾルサンプルからウイルスが検出された6件についても、そのうちの4件ではウイルス培養を行い、うち2件で培養陽性となった。統計学的には、サージカルマスク着用により飛沫サンプルからのインフルエンザウイルス検出を有意に抑えることができた(p=0.04)が、エアロゾルサンプルでは抑制できなかった(p=0.36)。
ライノウイルスでは、非マスク群の飛沫サンプル32件のうち9件(28%)から、エアロゾルサンプル34件のうち19件(35%)からウイルスが検出されたが、マスク群のサンプルでは飛沫サンプル27件のうち6件(22%)から、エアロゾルサンプル32件のうち12件(38%)からウイルスが検出された。ライノウイルスに関して言えば、サージカルマスク着用の有用性は統計学的に認められなかった(飛沫サンプルでp=0.77、エアロゾルサンプルでp=0.15)。
今回の研究に参加した246人のうち、72人(29%)は呼気サンプル採取の間、一度も咳をすることがなかった。このうち、コロナウイルスが検出された4人では、飛沫サンプル、エアロゾルサンプルのいずれからもコロナウイルスは検出されなかった。インフルエンザウイルスが検出された9人では、そのうち1人のエアロゾルサンプルからウイルスが検出され、飛沫サンプルからは検出されなかった。ライノウイルスが検出された17人では、そのうち3人では飛沫サンプルから、5人ではエアロゾルサンプルからウイルスが検出された。
http://oitahaiganpractice.junglekouen.com/e972744.html
言い方を変えれば、ガーゼマスクの微粒子遮断効果はわずか3%、医療用マスクの遮断効果は56%と見ることもでき、その差は歴然である。
では、44%の微粒子透過を許してしまうサージカルマスク、医学的(ウイルス学的)な見地から見れば、どの程度感染者からのウイルス粒子飛散を抑制することができるのか。
それを検証したのが本報告である。
NHKのニュースで取り扱われていたので、論文を検索して読んでみた。
本試験は、WHO、香港大学、ハーバード大学、メリーランド大学の共同研究として、2013年の3月から2016年の5月にかけて、香港のある私立病院で、外来患者を対象に行われた。
当初はインフルエンザ感染を主な対象として、試験後半ではその他のウイルスも対象として試験が行われ、少数ながらコロナウイルス感染症者も対象に含まれていたために、たまたま今回のCoVID-19 pandemicにfitする報告となった。
今回の記事では、煩雑になるため細かい方法は記載しなかったが、試験参加者にはインフルエンザ迅速検査が無償で行われること、30分かかる呼気サンプル採取に協力したら1回あたり30$相当の商品券をもらえること、さらに参加者全員に20$相当の体温計が提供されることになっていたことなどが記されていた。結果として、サージカルマスクをしたときとしないときの2回のサンプル採取に1時間以上をかけて協力し、60$相当の商品券と20$相当の体温計を受け取った49人から得られたデータが、我々に最も示唆を与える結果を提供してくれることになった。
少ないサンプル数での検討なのでどこまで信頼性、再現性が担保されるのかわからないが、ウイルスによってこれだけサージカルマスクの有効性が異なるのかと、いささか驚いた。
コロナウイルス感染症患者にサージカルマスクを装着させた場合、今回の報告では完全にウイルス拡散を抑制できたわけであり、かなりのウイルス拡散抑制効果が期待できそうだ。
一方、インフルエンザウイルスやライノウイルスのエアロゾルに対しては、サージカルマスクはあまり意味がないことも示されていた。
また、咳症状のないコロナウイルス感染患者の飛沫サンプル、エアロゾルサンプルからはコロナウイルスは検出されなかったとのことだが、これは巷で言われているようなSARS-CoV-2の特性(無症状キャリアからも拡散しうる)とは異なる。
SARS-CoV-2感染が確認され、咳症状を伴う患者にサージカルマスク着用を義務付けるのは必須といっていいが、咳症状を伴わない患者からウイルス拡散を抑止する目的で、あるいは一般健常者(中にはSARS-CoV-2キャリアも含む)が知らないうちにウイルスを拡散させることを防止する目的でサージカルマスクを着用するかどうかは、サージカルマスクの資源量とのトレード・オフとなる。
いずれにせよ、サージカルマスク着用の目的は、自分を他者から拡散されるウイルスから守ることではない(少なくとも、そうした効果は科学的に検証されていない)ことは誰もが知っておくべきであり、絶対的にサージカルマスクが不足している現状では、感染者に対応している医療現場や、これから患者受け入れを開始する宿泊施設等へ優先的にサージカルマスクを供給するべきである。
Respiratory virus shedding in exhaled breath and efficacy of face masks
Nancy H. L. Leung. et al., Nat Med 2020
https://doi.org/10.1038/s41591-020-0843-2
呼吸器系のウイルス感染症は、呼吸器ウイルス疾患、あるいは「風邪」とひとくくりに語られる症候群を引き起こす。こうした呼吸器ウイルス疾患はおしなべて軽症であることが多いが、ときに重篤・致死的になることもある。原因となるウイルスは、ヒト-ヒト間で直接・間接の接触、気道系飛沫(発生源から直ちに地面へ落下する比較的大きな飛沫から、直径>5μmの大きめのエアロゾル)、微粒子エアロゾル(直径≦5μmの飛沫・飛沫核)を介して広がっていく。接触感染を予防する目的での手指衛生、気道系飛沫を介しての感染を予防する目的でのマスク着用は、インフルエンザ拡散を緩和する対策として重要とされてきた一方で、他の呼吸器疾患ウイルスの拡散予防策としてどうなのかはあまり知られていない。このことは、CoVID-19に関しても同様である。
いくつかの保健政策当局は、個々の患者から感染が広がることを予防するために、患者にマスクを着用させることを推奨している。医療現場で使用される、いわゆるサージカルマスクは、本来は外科医が患者の創部に細菌を持ち込まないようにするため、患者を術後感染合併症から守るための予防手段として現場に持ち込まれたものである。後に、患者から医療者への二次感染を予防する手段としても利用されるようになった。しかしながら、マスクの科学的有効性を検証した報告は、非感染性の飛沫をどの程度フィルターとして遮断できるかという物理的な実験に基づくものがほとんどであり、呼吸器疾患ウイルスを含む飛沫遮断策として有効かどうかまで一般化することは難しい。呼吸器疾患ウイルスの遮断効果、呼吸器感染症に罹患した患者からのウイルス拡散をどの程度医療用マスクが遮断するかについては情報が乏しく、それもインフルエンザウイルスに関する報告がほとんどである。
今回は、コロナウイルス、インフルエンザウイルス、ライノウイルスについて、飛沫やエアロゾルが感染拡大にどの程度重要なのかを検証した。急性呼吸器ウイルス感染症に罹患した患者を対象として、その呼気中に含まれるウイルス量を測定し、サージカルマスクのウイルス拡散抑制効果を検討した。
3,363人の患者をスクリーニングし、最終的に246人の患者を呼気サンプル提供者として登録した。122人(50%)は呼気サンプル採取時にサージカルマスクを着用しない群(非マスク群)とし、124人(50%)はサージカルマスクを着用する群(マスク群)とした。そのうち、49人(20%)の患者は、マスクを着用したとき、しなかったときの両方で呼気サンプルを採取させてくれた。
RT-PCRにより、少なくとも1種類の呼吸器疾患ウイルスが同定されたのは246人中123人(50%)だった。そのうち111人(90%)は、季節性コロナウイルス17人、インフルエンザウイルス43人、ライノウイルス54人で占められており、その中にはコロナウイルスとインフルエンザウイルスの重複感染が1人、ライノウイルスとインフルエンザウイルスの重複感染が2人含まれていた。この111人が、今回の調査対象となった。
この3種のウイルス感染症患者の間には、ちょっとした背景の違いがあった。全体の24%の患者で37.8℃以上の発熱を認めたが、コロナウイルス感染者とライノウイルス感染者の合計よりも、インフルエンザウイルス感染者の方が発熱患者が2倍以上多かった。コロナウイルス感染者は咳を伴うことが最も多く、30分間の呼気採取時間の間に平均17回咳をしていた。無作為化された非マスク群とマスク群の背景は同等だった。
患者の鼻腔擦過サンプル、咽頭擦過サンプル、飛沫サンプル、エアロゾルサンプル中のウイルス量を測定した。飛沫サンプルとエアロゾルサンプルについてはマスクをした状態、あるいはしなかった状態で採取し、比較した。平均して、ウイルス量は咽頭擦過サンプルよりも鼻腔擦過サンプルの方が多かった(コロナウイルス:8.1 vs 3.9、インフルエンザウイルス:6.7 vs 4.0、ライノウイルス:6.8 vs 3.3、単位はlog10ウイルスコピー数)。ウイルスRNAは、飛沫サンプルあるいはエアロゾルサンプルにおいて、3種全てのウイルスで同定され、コロナウイルス、インフルエンザウイルス、ライノウイルスの順で述べると、マスクをしない状態では飛沫サンプルのそれぞれ30%、26%、28%で、エアロゾルサンプルのそれぞれ40%、35%、56%で検出された。
コロナウイルスに関して言えば、OC43株とHKU1株は飛沫サンプル、エアロゾルサンプルの両方から検出されたが、NL63株はエアロゾルサンプルのみから検出され、飛沫サンプルからは検出されなかった。非マスク群の飛沫サンプル10件のうち3件(30%)から、エアロゾルサンプル10件のうち4件(40%)からウイルスが検出されたが、マスク群では飛沫サンプル、エアロゾルサンプルいずれからも全くウイルスは検出されなかった。統計学的には、サージカルマスク着用により、エアロゾルサンプルからのコロナウイルス検出を有意に抑えることができ(p=0.04)、飛沫サンプルからも抑制される傾向が見られた(p=0.07)。
インフルエンザウイルスでは、非マスク群の飛沫サンプル23件のうち6件(26%)から、エアロゾルサンプル23件のうち8件(35%)からウイルスが検出されたが、マスク群のサンプルでは飛沫サンプル27件のうち1件(4%)から、エアロゾルサンプル27件のうち6件(22%)からウイルスが検出された。さらに言えば、非マスク群のエアロゾルサンプルからウイルスが検出された8件について、そのうちの5件ではウイルス培養を行い、そのうち4件で培養陽性となった。マスク群のエアロゾルサンプルからウイルスが検出された6件についても、そのうちの4件ではウイルス培養を行い、うち2件で培養陽性となった。統計学的には、サージカルマスク着用により飛沫サンプルからのインフルエンザウイルス検出を有意に抑えることができた(p=0.04)が、エアロゾルサンプルでは抑制できなかった(p=0.36)。
ライノウイルスでは、非マスク群の飛沫サンプル32件のうち9件(28%)から、エアロゾルサンプル34件のうち19件(35%)からウイルスが検出されたが、マスク群のサンプルでは飛沫サンプル27件のうち6件(22%)から、エアロゾルサンプル32件のうち12件(38%)からウイルスが検出された。ライノウイルスに関して言えば、サージカルマスク着用の有用性は統計学的に認められなかった(飛沫サンプルでp=0.77、エアロゾルサンプルでp=0.15)。
今回の研究に参加した246人のうち、72人(29%)は呼気サンプル採取の間、一度も咳をすることがなかった。このうち、コロナウイルスが検出された4人では、飛沫サンプル、エアロゾルサンプルのいずれからもコロナウイルスは検出されなかった。インフルエンザウイルスが検出された9人では、そのうち1人のエアロゾルサンプルからウイルスが検出され、飛沫サンプルからは検出されなかった。ライノウイルスが検出された17人では、そのうち3人では飛沫サンプルから、5人ではエアロゾルサンプルからウイルスが検出された。
2020年04月05日
新型コロナウイルス感染症対策として、ガーゼマスクは有効なのか?
最近突如として始まった、各大臣のマスク着用が話題になっている。
中でも、安倍首相が率先して使用しているガーゼマスクは、一部で失笑を買っている。
アベノミクスにあやかって、アベノマスクという用語まで出てきているようだ。
以下の論文を見る限り、吸入予防対策としてのガーゼマスクは、エアロゾルを想定した人工微粒子を97%透過したそうで、ザルみたいなもんである。
一方、医療用マスクは、44%の透過性に留まるとのこと。
布マスク装着は医療従事者は避けた方が良さそうだが、医療用マスクについては、あながち、全く意味がないとも言い切れない結果だ。
さて、それではガーゼマスクを発症者、あるいは無症候性の新型コロナウイルスキャリア(=誰もがそうである可能性あり)に装着させた場合、エアロゾル拡散を防ぐ効果がどれくらいあるのだろうか。
国民の意識向上を促す意味ではガーゼマスク配布の意味はあるかもしれないが、科学的に有効な対策なのかどうかは、並行してきちんと検証してほしい。
現段階では、有効とも無効とも断じるべきではない。
reduce, reuse, recycleという観点から言えば、本当に有効ならばガーゼマスク利用の意義はとても高い。
私も学校給食の給食係の時にはガーゼマスクを使っていた(しょっちゅう忘れ物をして怒られていた)世代なので、ガーゼマスクがこうした形で活躍できるのであれば、それはそれで嬉しい。
A cluster randomised trial of cloth masks compared with medical masks in healthcare workers
MacIntyre. et al., BMJ Open 2015
http://dx.doi.org/10.1136/ bmjopen-2014-006577
目的:
本研究の目的は、病院内医療従事者の感染予防対策として、布マスクと不織布製医療用マスクの効果を比較することである。帰無仮説は、布マスクと医療用マスクの間に効果の違いがない、ということとした(布マスクと医療用マスクの効果に有意差がつくことを検証した)。
方法:
ベトナムのハノイにおける14病院の、院内感染高リスクの計74病棟において、18歳以上でフルタイム勤務をする医療従事者を対象とした。病棟ごとに、1)医療用マスクを使う病棟、2)布マスクを使う病棟、3)通常実地医療に即した対応をする病棟(コントロール群)に無作為割付し、勤務シフトごとにマスクを装着して業務についてもらい、連続4週間継続した。医療用マスクは1日2枚支給して使い捨て、布マスクは期間中ずっと、洗濯を繰り返しながら利用継続してもらった。主要評価項目は、臨床的に問題となる呼吸器疾患、インフルエンザ様疾患、呼吸器系の症状を起こすウイルスの検出割合とした。
結果:感染症に関連した全てのアウトカムについて、布マスクは最悪の結果となった。医療用マスク群と比較して、布マスク群は有意にインフルエンザ様疾患に罹患する割合が高かった(相対危険度 13.00、95%信頼区間 1.69-100.07)。コントロール群を個別に調べて、医療用マスク群と布マスク群に区分してそれぞれの群に加えたところ、布マスク群はインフルエンザ様疾患に罹患する割合(相対危険度 6.64、95%信頼区間は1.45-28.65)や、検査により何らかのウイルス感染が判明する割合(相対危険度 1.72、95%信頼区間1.01-2.94)が高かった。既定の微粒子がそれぞれのマスクをどの程度透過するか、という実験では、布マスクでは97%までが透過したのに対して、医療用マスクでは44%にとどまった。
中でも、安倍首相が率先して使用しているガーゼマスクは、一部で失笑を買っている。
アベノミクスにあやかって、アベノマスクという用語まで出てきているようだ。
以下の論文を見る限り、吸入予防対策としてのガーゼマスクは、エアロゾルを想定した人工微粒子を97%透過したそうで、ザルみたいなもんである。
一方、医療用マスクは、44%の透過性に留まるとのこと。
布マスク装着は医療従事者は避けた方が良さそうだが、医療用マスクについては、あながち、全く意味がないとも言い切れない結果だ。
さて、それではガーゼマスクを発症者、あるいは無症候性の新型コロナウイルスキャリア(=誰もがそうである可能性あり)に装着させた場合、エアロゾル拡散を防ぐ効果がどれくらいあるのだろうか。
国民の意識向上を促す意味ではガーゼマスク配布の意味はあるかもしれないが、科学的に有効な対策なのかどうかは、並行してきちんと検証してほしい。
現段階では、有効とも無効とも断じるべきではない。
reduce, reuse, recycleという観点から言えば、本当に有効ならばガーゼマスク利用の意義はとても高い。
私も学校給食の給食係の時にはガーゼマスクを使っていた(しょっちゅう忘れ物をして怒られていた)世代なので、ガーゼマスクがこうした形で活躍できるのであれば、それはそれで嬉しい。
A cluster randomised trial of cloth masks compared with medical masks in healthcare workers
MacIntyre. et al., BMJ Open 2015
http://dx.doi.org/10.1136/ bmjopen-2014-006577
目的:
本研究の目的は、病院内医療従事者の感染予防対策として、布マスクと不織布製医療用マスクの効果を比較することである。帰無仮説は、布マスクと医療用マスクの間に効果の違いがない、ということとした(布マスクと医療用マスクの効果に有意差がつくことを検証した)。
方法:
ベトナムのハノイにおける14病院の、院内感染高リスクの計74病棟において、18歳以上でフルタイム勤務をする医療従事者を対象とした。病棟ごとに、1)医療用マスクを使う病棟、2)布マスクを使う病棟、3)通常実地医療に即した対応をする病棟(コントロール群)に無作為割付し、勤務シフトごとにマスクを装着して業務についてもらい、連続4週間継続した。医療用マスクは1日2枚支給して使い捨て、布マスクは期間中ずっと、洗濯を繰り返しながら利用継続してもらった。主要評価項目は、臨床的に問題となる呼吸器疾患、インフルエンザ様疾患、呼吸器系の症状を起こすウイルスの検出割合とした。
結果:感染症に関連した全てのアウトカムについて、布マスクは最悪の結果となった。医療用マスク群と比較して、布マスク群は有意にインフルエンザ様疾患に罹患する割合が高かった(相対危険度 13.00、95%信頼区間 1.69-100.07)。コントロール群を個別に調べて、医療用マスク群と布マスク群に区分してそれぞれの群に加えたところ、布マスク群はインフルエンザ様疾患に罹患する割合(相対危険度 6.64、95%信頼区間は1.45-28.65)や、検査により何らかのウイルス感染が判明する割合(相対危険度 1.72、95%信頼区間1.01-2.94)が高かった。既定の微粒子がそれぞれのマスクをどの程度透過するか、という実験では、布マスクでは97%までが透過したのに対して、医療用マスクでは44%にとどまった。
2020年04月03日
EGFR exon 20挿入変異とTAK-788
EGFR遺伝子変異のうち約6%を占めるEGFR exon 20挿入変異は、EGFR遺伝子変異とはいいながら、実際にはEGFR遺伝子変異陰性とほぼ同義である。
EGFR阻害薬の効果がほぼ期待できないからだ。
今年に入って、uncommon EGFR mutationに対するオシメルチニブの臨床試験の記事を書いた。
http://oitahaiganpractice.junglekouen.com/e968312.html
この臨床試験でも、exon 20挿入変異の患者は除外されている。
過去に、exon 20挿入変異に対して、Poziotinibが有効だという記事を書いた。
http://oitahaiganpractice.junglekouen.com/e914150.html
2019年のASCOでは、exon 20挿入変異に特化したEGFR阻害薬であるTAK-788についての報告があった。
今のところ、この2薬剤が有望株だと思われるが、まだまだ実用化には時間がかかりそうだ。
Antitumor activity of TAK-788 in NSCLC with EGFR exon 20 insertions.
Jänne PA, et al. ASCO 2019 Abst.#9007
目的 :
EGFR exon 20挿入変異を有する進行非小細胞肺がん患者を対象に、TAK-788を投与した場合の有効性および安全性を検討した
方法 :
EGFR exon 20挿入変異を有する進行非小細胞肺がん患者(第I相用量漸増コホートから6人、第II相拡大コホートから22人)を対象とした。
第I相:用量漸増コホート(3+3デザイン)、対象は進行非小細胞肺がん患者
第II相:拡大コホート(遺伝子異常等で分類した複数のコホート)、今回の解析対象は既治療のEGFR exon 20挿入変異陽性進行非小細胞肺がん患者
主要評価項目:有効性で、EGFR exon 20挿入変異陽性患者の奏効割合で評価
副次評価項目:安全性:第I相および第II相でTAK-788を投与された全ての患者で評価
結果:
exon 20挿入変異の対象患者は28人。
年齢中央値62歳、女性が75%、白人が71%、アジア人18%、腺がん96%。
前治療としてEGFR阻害薬を使用した患者は18%、免疫チェックポイント阻害薬を使用した患者は61%。
脳転移があった患者は43%。

exon 20挿入変異の患者における奏効割合は43%、病勢コントロール割合は86%、無増悪生存期間中央値は7.3ヶ月。
そのうち、脳転移があった患者では奏効割合は25%、病勢コントロール割合は67%、無増悪生存期間中央値は3.7ヶ月。
脳転移がなかった患者では奏効割合は56%、病勢コントロール割合は100%、無増悪生存期間中央値は8.1ヶ月。

全く腫瘍縮小効果が得られなかった患者はたった1人。

主な有害事象は消化器症状と皮膚障害だった。

EGFR阻害薬の効果がほぼ期待できないからだ。
今年に入って、uncommon EGFR mutationに対するオシメルチニブの臨床試験の記事を書いた。
http://oitahaiganpractice.junglekouen.com/e968312.html
この臨床試験でも、exon 20挿入変異の患者は除外されている。
過去に、exon 20挿入変異に対して、Poziotinibが有効だという記事を書いた。
http://oitahaiganpractice.junglekouen.com/e914150.html
2019年のASCOでは、exon 20挿入変異に特化したEGFR阻害薬であるTAK-788についての報告があった。
今のところ、この2薬剤が有望株だと思われるが、まだまだ実用化には時間がかかりそうだ。
Antitumor activity of TAK-788 in NSCLC with EGFR exon 20 insertions.
Jänne PA, et al. ASCO 2019 Abst.#9007
目的 :
EGFR exon 20挿入変異を有する進行非小細胞肺がん患者を対象に、TAK-788を投与した場合の有効性および安全性を検討した
方法 :
EGFR exon 20挿入変異を有する進行非小細胞肺がん患者(第I相用量漸増コホートから6人、第II相拡大コホートから22人)を対象とした。
第I相:用量漸増コホート(3+3デザイン)、対象は進行非小細胞肺がん患者
第II相:拡大コホート(遺伝子異常等で分類した複数のコホート)、今回の解析対象は既治療のEGFR exon 20挿入変異陽性進行非小細胞肺がん患者
主要評価項目:有効性で、EGFR exon 20挿入変異陽性患者の奏効割合で評価
副次評価項目:安全性:第I相および第II相でTAK-788を投与された全ての患者で評価
結果:
exon 20挿入変異の対象患者は28人。
年齢中央値62歳、女性が75%、白人が71%、アジア人18%、腺がん96%。
前治療としてEGFR阻害薬を使用した患者は18%、免疫チェックポイント阻害薬を使用した患者は61%。
脳転移があった患者は43%。

exon 20挿入変異の患者における奏効割合は43%、病勢コントロール割合は86%、無増悪生存期間中央値は7.3ヶ月。
そのうち、脳転移があった患者では奏効割合は25%、病勢コントロール割合は67%、無増悪生存期間中央値は3.7ヶ月。
脳転移がなかった患者では奏効割合は56%、病勢コントロール割合は100%、無増悪生存期間中央値は8.1ヶ月。

全く腫瘍縮小効果が得られなかった患者はたった1人。

主な有害事象は消化器症状と皮膚障害だった。




