2017年01月20日
再生検を取り巻く環境の変化
年明けに煩った鼻水と咳が未だに尾を引いていて、すっきりしない。
もう2週間になる。
年が明けるとともに、身の回りでインフルエンザ患者が激増した。
わが職場で、2016年12月期にインフルエンザと診断された患者はわずか1人だった。
2017年1月になると、半月で既に30人に達している。
自分ももしやと思い、2回もインフルエンザ迅速検査をしたが、陰性だった。
さすがに3回目をする気は起きない。
EGFR遺伝子変異検索についても、この年末年始にぼんやりしている間に大きな変化が起こった。
いよいよ、我が国でもEGFR遺伝子変異を血液検査で行えるようになった。
ただし、他国における適用条件とは一部異なる。
EGFR遺伝子変異を初回診断する際には、血漿検査は使えない。
過去にEGFR遺伝子変異陽性が確認され、初回治療後病勢進行した際のT790M再検索を目的とする場合のみが血漿検査の対象となる。
ロシュ・ダイアグノスティクス社のT790M血漿検査適応取得のプレスリリース
http://www.roche-diagnostics.jp/news/16/12/27.html
我が国では肺がんの診断時に気管支鏡が行われることが多いが、患者さんは検査について酷評される。
肺がんの診断のみならず、気管支鏡検査一般に言えることだ。
肺がんの診断目的ならまだしも、がん以外の、しかもそれほど緊急性のない状況では、なかなか受け入れてもらえない。
2回目の検査となると、さらにハードルは高くなる。
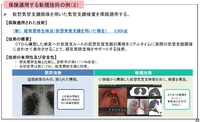
以下の調査では、もう二度と気管支鏡をしたくないという人が35%、再度受けなくはないがつらかったという人が42%、併せて約77%の人が、気管支鏡検査でかなりつらい思いをしている。
その結果、治療変更が必要になった際、血漿検査の結果で治療薬の選択ができるなら受けたいという人が、ほぼ同率の78%を占める。
問題はそこからで、血漿検査で陰性だったとしても、気管支鏡や針生検の結果陽性になる可能性があるのなら受けてみたい、という人は、全体の89%を占めていた。
再生検に関する意識調査
https://oncolo.jp/reserch/20161214
こうした患者意識を踏まえ、アストラゼネカ社はT790M血漿検査が保険償還されるまでの移行措置として、前倒しでT790M血漿検査の受託を始めた。
採血から血漿分離、凍結保存までを4時間以内に終えなければならないという制約があるため、検査部門の協力が不可欠だが、既に多くの公的医療機関で受託可能になっていると聞く。
アストラゼネカ社のT790M血漿検査の倫理供給
https://www.astrazeneca.co.jp/media/press-releases1/2017/20170105.html
こうしたニーズがあることは医療者として知っておかなければならず、血漿検査で陰性であったとしても、当初は患者が気管支鏡や針生検を拒否していたとしても、もう一度これら検査の必要性を説明しなければならない。
さて、生検が可能な部位に病巣がある場合、
・先に血漿検査をして、陰性なら気管支鏡や針生検を行う
・先に気管支鏡や針生検をして、陰性なら血漿検査をする
のどちらが順序として正しいのか。
私なら、さきに血漿検査をして、陰性だった場合に組織検査をしたい。
3つ理由がある。
1)楽に検査が受けられるなら、それに越したことはない
気管支鏡の説明をして、実際に気管支鏡を実施する立場の者としては、やらずに済むならそれに越したことはない。
何より、患者が楽である。
きつくて危険な思いをしなくて済む。
初めての気管支鏡検査でとてもつらい思いをした、もう二度と受けたくない、という声はとても多い。
近々、そうした患者の再生検目的気管支鏡検査が2件予定されており、気が滅入ることこの上ない。
面倒だ、といっているわけではなくて、他に楽な手段があればいいのに、ということだ。
検査をするほうの立場としても、面倒な検査説明、同意取得、合併症や患者からの苦情におびえながらの検査実施は、避けられるなら避けたい。
2)血漿検査が陽性になるかどうかは、病状の進行をある程度反映している
決定的な証拠はないものの、血漿検査によるEGFR遺伝子変異検出研究に関わっている先生方の生の声を聞くと、血漿検査でEGFR遺伝子変異が検出されるかどうかと、病状進行の程度は、関連がありそうだ。
肺がんが一部に留まらず、血流に乗って全身的な広がりを見せた場合、EGFR遺伝子変異が血漿検査で検出されることが多いようだ。
もちろんこれは、肺がん細胞に由来するDNAが血流に漏れ出ているかどうかを示しているだけで、その患者にT790M変異があるかどうかを直接示しているわけではない。
換言すれば、もともとEGFR遺伝子変異陽性だった患者の病状が進行した場合、血漿検査でそのEGFR遺伝子変異が検出される可能性は高くなるだろうが、そこにT790M変異が加わっているかどうかは別の問題である。
一方で、血漿検査においてT790Mが検出された場合には、血流に乗って全身へ転移した(あるいは転移しつつある)がん細胞がT790M変異を持っていることは確実だろう。
血漿検査においてT790M変異陽性が確認されれば、血流を介して全身に広がった肺がん細胞を第3世代EGFR-TKIで治療することが出来るだろう。
一方、組織生検でT790M変異を検出したとしても、患者の中でのがん細胞の多様性を踏まえて厳密に言うなら、その組織を採取した病巣でしか第3世代EGFR-TKIの治療効果が予測できない。
ほかの病巣では、T790M変異が陰性で、治療効果が期待できないかもしれない。
過去に経験した患者で、股関節の部位から苦労して再生検し、T790M変異が検出されたため勇躍してOsimertinibを開始したにも関わらず、再生検部位は著明に縮小したものの、他の部位には全く効かずに、ほどなく終末期治療に移行したという方がいた。
多分この患者では、血漿検査を行うとT790M変異は陰性だったのではないか。
もちろん、血漿検査が陽性だったとしても、縮小させたい病巣の生検が可能なら、それも併せてするに越したことはない。
血漿検査、特定の病巣の組織検査の両方でT790M変異が陽性なら、最もよい第3世代EGFR-TKIの対象になるだろう。
3)以下の論文に、「まず血漿検査をしてT790M陽性ならそのまま第3世代EGFR阻害薬を使用して、陰性だったら組織生検をしよう」と書いてある
Association Between Plasma Genotyping and Outcomes of Treatment With Osimertinib (AZD9291) in Advanced Non-Small-Cell Lung Cancer.
Oxnard GR, Thress KS, Alden RS, Lawrance R, Paweletz CP, Cantarini M, Yang JC, Barrett JC, Jänne PA.
J Clin Oncol. 2016 Oct 1;34(28):3375-82.
この論文の結果は注意深く解釈しなければならないが、実地臨床における再生検の進め方と結果の解釈について、かなり重要な示唆を与えてくれる。
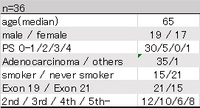
・AURA試験の第I相部分に参加した患者のうち、治療歴のない患者、exon 19もしくはexon 21以外の稀なEGFR遺伝子変異を有する患者、EGFR遺伝子変異のない患者は除外し、308人を解析対象とした
・腫瘍組織の遺伝子解析結果と治療経過がわかる患者(患者群①)は237人だった
・血漿の遺伝子解析結果と治療経過がわかる患者(患者群②)は271人だった
・腫瘍組織と血漿両方の遺伝子解析結果と治療経過がわかる患者(患者群③)は216人だった
<以下、患者群①の解析>
・奏効割合は、腫瘍組織でT790M陽性だった患者で108/173=62%、陰性だった患者で15/58=26%
・無増悪生存期間はT790M陽性の患者で9.7ヶ月、陰性の患者で3.4ヶ月
<以下、患者群②の解析>
・奏効割合は、血漿でT790M陽性だった患者で103/164=63%、陰性だった患者で47/102=47%
・無増悪生存期間は、血漿でT790M陽性だった患者で9.7ヶ月、陰性の患者で8.2ヶ月
<以下、患者群③の解析>
・腫瘍組織でexon 19陽性と判定された患者のうち、血漿でもexon 19陽性と判定された患者は112/136=82.3%だった
・腫瘍組織でexon 21陽性と判定された患者のうち、血漿でもexon 21陽性と判定された患者は63/73=86.3%だった
・腫瘍組織でexon 19とexon 21どちらかが陽性となった患者を調べたところ、肝転移を有する患者群(61/65=94%)では肝転移のない患者群(114/144=79%)より血漿でも陽性となることが多かった(p=0.008)
・腫瘍組織でexon 19とexon 21どちらかが陽性となった患者を調べたところ、胸郭外転移巣のない患者群(36/48=75%)では胸郭外転移巣のある患者群(139/161=86%)より血漿で陽性となることが少なさそうだった(p=0.06)
・腫瘍組織でT790M陽性と判定された患者のうち、血漿でもT790M陽性と判定された患者は111/158=70.3%だった
・腫瘍組織でT790M陽性と判定された患者158人のうち、血漿でexon 19またはexon 21が陽性となった患者137人中では血漿でT790Mも陽性となる割合が高い(110/137=80.3%)一方で、血漿でexon 19またはexon 21が陰性だった患者21人中では血漿でT790Mが陽性となる割合は低かった(1/21=4.8%)
・腫瘍組織でexon 19陰性と判定された患者のうち、血漿でもexon 19陰性と判定された患者は78/80=97.5%だった
・腫瘍組織でexon 21陰性と判定された患者のうち、血漿でもexon 21陰性と判定された患者は138/143=96.5%だった
・腫瘍組織でT790M陰性と判定された患者のうち、血漿でもT790M陰性と判定された患者は40/58=69.0%だった
・腫瘍組織でT790M陰性、血漿でT790M陽性と判定された患者が18人いたが、検査法をかえて血漿検査をしても14/18=78%が再度陽性と判定され、これは検査法による疑陽性ではなさそうだった
・血漿でT790M陰性と判定された患者のうち、腫瘍組織でT790M陽性と判定された患者の奏効割合31/45=69%および無増悪生存期間中央値16.5ヶ月は、腫瘍組織でT790M陰性と判定された患者の奏効割合10/40=25%および無増悪生存期間中央値2.8ヶ月よりも有意に優れていた(p<0.001, p<0.001)
・血漿でT790M陽性と判定された患者のうち、腫瘍組織でT790M陽性と判定された患者の奏効割合69/108=64%および無増悪生存期間中央値9.3ヶ月は、腫瘍組織でT790M陰性と判定された患者の奏効割合5/18=28%および無増悪生存期間中央値4.2ヶ月よりも有意に優れていた(p=0.004, p=0.002)
・血漿でT790Mが陰性、exon 19 / exon 21が陽性だった患者群における奏効割合は26/69=38%, 無増悪生存期間中央値は4.4ヶ月だった
・血漿でT790Mが陰性、exon 19 / exon 21も陰性だった患者群における奏効割合は21/33=64%、無増悪生存期間中央値は15.2ヶ月だった
・もともとexon 19 /exon 21が陽性の患者群で、血漿においてexon 19 / exon 21 / T790Mいずれも陰性の患者では、病勢の進行が緩やかなため、そもそもctDNAが検出感度以下であるのかもしれない
・以上のことから、血漿検査においてT790Mが陰性だった場合、その結果が信頼できるものかどうかについてはexon 19 / exon 21の結果がどうだったかも参照しなくてはならない
・治療により耐性化した肺がんは未治療の肺がんに比べて多様性のある細胞集団で、どこかひとつの病巣の生検で全体像を推し量れるとは考えないほうがいい
・血漿でT790M陰性と判定されても、できる限り腫瘍組織生検を行い、T790M陽性と判定されればかなり治療効果が期待できる
もう2週間になる。
年が明けるとともに、身の回りでインフルエンザ患者が激増した。
わが職場で、2016年12月期にインフルエンザと診断された患者はわずか1人だった。
2017年1月になると、半月で既に30人に達している。
自分ももしやと思い、2回もインフルエンザ迅速検査をしたが、陰性だった。
さすがに3回目をする気は起きない。
EGFR遺伝子変異検索についても、この年末年始にぼんやりしている間に大きな変化が起こった。
いよいよ、我が国でもEGFR遺伝子変異を血液検査で行えるようになった。
ただし、他国における適用条件とは一部異なる。
EGFR遺伝子変異を初回診断する際には、血漿検査は使えない。
過去にEGFR遺伝子変異陽性が確認され、初回治療後病勢進行した際のT790M再検索を目的とする場合のみが血漿検査の対象となる。
ロシュ・ダイアグノスティクス社のT790M血漿検査適応取得のプレスリリース
http://www.roche-diagnostics.jp/news/16/12/27.html
我が国では肺がんの診断時に気管支鏡が行われることが多いが、患者さんは検査について酷評される。
肺がんの診断のみならず、気管支鏡検査一般に言えることだ。
肺がんの診断目的ならまだしも、がん以外の、しかもそれほど緊急性のない状況では、なかなか受け入れてもらえない。
2回目の検査となると、さらにハードルは高くなる。
以下の調査では、もう二度と気管支鏡をしたくないという人が35%、再度受けなくはないがつらかったという人が42%、併せて約77%の人が、気管支鏡検査でかなりつらい思いをしている。
その結果、治療変更が必要になった際、血漿検査の結果で治療薬の選択ができるなら受けたいという人が、ほぼ同率の78%を占める。
問題はそこからで、血漿検査で陰性だったとしても、気管支鏡や針生検の結果陽性になる可能性があるのなら受けてみたい、という人は、全体の89%を占めていた。
再生検に関する意識調査
https://oncolo.jp/reserch/20161214
こうした患者意識を踏まえ、アストラゼネカ社はT790M血漿検査が保険償還されるまでの移行措置として、前倒しでT790M血漿検査の受託を始めた。
採血から血漿分離、凍結保存までを4時間以内に終えなければならないという制約があるため、検査部門の協力が不可欠だが、既に多くの公的医療機関で受託可能になっていると聞く。
アストラゼネカ社のT790M血漿検査の倫理供給
https://www.astrazeneca.co.jp/media/press-releases1/2017/20170105.html
こうしたニーズがあることは医療者として知っておかなければならず、血漿検査で陰性であったとしても、当初は患者が気管支鏡や針生検を拒否していたとしても、もう一度これら検査の必要性を説明しなければならない。
さて、生検が可能な部位に病巣がある場合、
・先に血漿検査をして、陰性なら気管支鏡や針生検を行う
・先に気管支鏡や針生検をして、陰性なら血漿検査をする
のどちらが順序として正しいのか。
私なら、さきに血漿検査をして、陰性だった場合に組織検査をしたい。
3つ理由がある。
1)楽に検査が受けられるなら、それに越したことはない
気管支鏡の説明をして、実際に気管支鏡を実施する立場の者としては、やらずに済むならそれに越したことはない。
何より、患者が楽である。
きつくて危険な思いをしなくて済む。
初めての気管支鏡検査でとてもつらい思いをした、もう二度と受けたくない、という声はとても多い。
近々、そうした患者の再生検目的気管支鏡検査が2件予定されており、気が滅入ることこの上ない。
面倒だ、といっているわけではなくて、他に楽な手段があればいいのに、ということだ。
検査をするほうの立場としても、面倒な検査説明、同意取得、合併症や患者からの苦情におびえながらの検査実施は、避けられるなら避けたい。
2)血漿検査が陽性になるかどうかは、病状の進行をある程度反映している
決定的な証拠はないものの、血漿検査によるEGFR遺伝子変異検出研究に関わっている先生方の生の声を聞くと、血漿検査でEGFR遺伝子変異が検出されるかどうかと、病状進行の程度は、関連がありそうだ。
肺がんが一部に留まらず、血流に乗って全身的な広がりを見せた場合、EGFR遺伝子変異が血漿検査で検出されることが多いようだ。
もちろんこれは、肺がん細胞に由来するDNAが血流に漏れ出ているかどうかを示しているだけで、その患者にT790M変異があるかどうかを直接示しているわけではない。
換言すれば、もともとEGFR遺伝子変異陽性だった患者の病状が進行した場合、血漿検査でそのEGFR遺伝子変異が検出される可能性は高くなるだろうが、そこにT790M変異が加わっているかどうかは別の問題である。
一方で、血漿検査においてT790Mが検出された場合には、血流に乗って全身へ転移した(あるいは転移しつつある)がん細胞がT790M変異を持っていることは確実だろう。
血漿検査においてT790M変異陽性が確認されれば、血流を介して全身に広がった肺がん細胞を第3世代EGFR-TKIで治療することが出来るだろう。
一方、組織生検でT790M変異を検出したとしても、患者の中でのがん細胞の多様性を踏まえて厳密に言うなら、その組織を採取した病巣でしか第3世代EGFR-TKIの治療効果が予測できない。
ほかの病巣では、T790M変異が陰性で、治療効果が期待できないかもしれない。
過去に経験した患者で、股関節の部位から苦労して再生検し、T790M変異が検出されたため勇躍してOsimertinibを開始したにも関わらず、再生検部位は著明に縮小したものの、他の部位には全く効かずに、ほどなく終末期治療に移行したという方がいた。
多分この患者では、血漿検査を行うとT790M変異は陰性だったのではないか。
もちろん、血漿検査が陽性だったとしても、縮小させたい病巣の生検が可能なら、それも併せてするに越したことはない。
血漿検査、特定の病巣の組織検査の両方でT790M変異が陽性なら、最もよい第3世代EGFR-TKIの対象になるだろう。
3)以下の論文に、「まず血漿検査をしてT790M陽性ならそのまま第3世代EGFR阻害薬を使用して、陰性だったら組織生検をしよう」と書いてある
Association Between Plasma Genotyping and Outcomes of Treatment With Osimertinib (AZD9291) in Advanced Non-Small-Cell Lung Cancer.
Oxnard GR, Thress KS, Alden RS, Lawrance R, Paweletz CP, Cantarini M, Yang JC, Barrett JC, Jänne PA.
J Clin Oncol. 2016 Oct 1;34(28):3375-82.
この論文の結果は注意深く解釈しなければならないが、実地臨床における再生検の進め方と結果の解釈について、かなり重要な示唆を与えてくれる。
・AURA試験の第I相部分に参加した患者のうち、治療歴のない患者、exon 19もしくはexon 21以外の稀なEGFR遺伝子変異を有する患者、EGFR遺伝子変異のない患者は除外し、308人を解析対象とした
・腫瘍組織の遺伝子解析結果と治療経過がわかる患者(患者群①)は237人だった
・血漿の遺伝子解析結果と治療経過がわかる患者(患者群②)は271人だった
・腫瘍組織と血漿両方の遺伝子解析結果と治療経過がわかる患者(患者群③)は216人だった
<以下、患者群①の解析>
・奏効割合は、腫瘍組織でT790M陽性だった患者で108/173=62%、陰性だった患者で15/58=26%
・無増悪生存期間はT790M陽性の患者で9.7ヶ月、陰性の患者で3.4ヶ月
<以下、患者群②の解析>
・奏効割合は、血漿でT790M陽性だった患者で103/164=63%、陰性だった患者で47/102=47%
・無増悪生存期間は、血漿でT790M陽性だった患者で9.7ヶ月、陰性の患者で8.2ヶ月
<以下、患者群③の解析>
・腫瘍組織でexon 19陽性と判定された患者のうち、血漿でもexon 19陽性と判定された患者は112/136=82.3%だった
・腫瘍組織でexon 21陽性と判定された患者のうち、血漿でもexon 21陽性と判定された患者は63/73=86.3%だった
・腫瘍組織でexon 19とexon 21どちらかが陽性となった患者を調べたところ、肝転移を有する患者群(61/65=94%)では肝転移のない患者群(114/144=79%)より血漿でも陽性となることが多かった(p=0.008)
・腫瘍組織でexon 19とexon 21どちらかが陽性となった患者を調べたところ、胸郭外転移巣のない患者群(36/48=75%)では胸郭外転移巣のある患者群(139/161=86%)より血漿で陽性となることが少なさそうだった(p=0.06)
・腫瘍組織でT790M陽性と判定された患者のうち、血漿でもT790M陽性と判定された患者は111/158=70.3%だった
・腫瘍組織でT790M陽性と判定された患者158人のうち、血漿でexon 19またはexon 21が陽性となった患者137人中では血漿でT790Mも陽性となる割合が高い(110/137=80.3%)一方で、血漿でexon 19またはexon 21が陰性だった患者21人中では血漿でT790Mが陽性となる割合は低かった(1/21=4.8%)
・腫瘍組織でexon 19陰性と判定された患者のうち、血漿でもexon 19陰性と判定された患者は78/80=97.5%だった
・腫瘍組織でexon 21陰性と判定された患者のうち、血漿でもexon 21陰性と判定された患者は138/143=96.5%だった
・腫瘍組織でT790M陰性と判定された患者のうち、血漿でもT790M陰性と判定された患者は40/58=69.0%だった
・腫瘍組織でT790M陰性、血漿でT790M陽性と判定された患者が18人いたが、検査法をかえて血漿検査をしても14/18=78%が再度陽性と判定され、これは検査法による疑陽性ではなさそうだった
・血漿でT790M陰性と判定された患者のうち、腫瘍組織でT790M陽性と判定された患者の奏効割合31/45=69%および無増悪生存期間中央値16.5ヶ月は、腫瘍組織でT790M陰性と判定された患者の奏効割合10/40=25%および無増悪生存期間中央値2.8ヶ月よりも有意に優れていた(p<0.001, p<0.001)
・血漿でT790M陽性と判定された患者のうち、腫瘍組織でT790M陽性と判定された患者の奏効割合69/108=64%および無増悪生存期間中央値9.3ヶ月は、腫瘍組織でT790M陰性と判定された患者の奏効割合5/18=28%および無増悪生存期間中央値4.2ヶ月よりも有意に優れていた(p=0.004, p=0.002)
・血漿でT790Mが陰性、exon 19 / exon 21が陽性だった患者群における奏効割合は26/69=38%, 無増悪生存期間中央値は4.4ヶ月だった
・血漿でT790Mが陰性、exon 19 / exon 21も陰性だった患者群における奏効割合は21/33=64%、無増悪生存期間中央値は15.2ヶ月だった
・もともとexon 19 /exon 21が陽性の患者群で、血漿においてexon 19 / exon 21 / T790Mいずれも陰性の患者では、病勢の進行が緩やかなため、そもそもctDNAが検出感度以下であるのかもしれない
・以上のことから、血漿検査においてT790Mが陰性だった場合、その結果が信頼できるものかどうかについてはexon 19 / exon 21の結果がどうだったかも参照しなくてはならない
・治療により耐性化した肺がんは未治療の肺がんに比べて多様性のある細胞集団で、どこかひとつの病巣の生検で全体像を推し量れるとは考えないほうがいい
・血漿でT790M陰性と判定されても、できる限り腫瘍組織生検を行い、T790M陽性と判定されればかなり治療効果が期待できる
フィルムとシャウカステンの文化
診断がつかないことの喜び
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
肺がんCT検診の比較試験:JECS Study
人工知能による胸部レントゲン読影支援
末梢病変穿刺用キット・・・Periview Flex
IMpower133試験、updated data
EGFR耐性機構としてのRET融合遺伝子出現と、オシメルチニブ+selpercatinib併用療法
RET陽性肺がんの臨床的特徴と治療反応性 シンガポール国立がんセンターの報告から
RET融合遺伝子陽性肺がんに対するselpercatinibの第III相試験:LIBRETTO-431試験の概要
オンコマインDx Target Test マルチ CDxシステム一時供給停止
学会報告0004:術前診断のついていなかった小細胞肺がん手術例のまとめ
あれから20年も、この先10年も
臨床像を信じるか、病理像を信じるか
「Class IIIB」を異なる立場で見てみると
経気管支肺生検の下準備
ドライバー遺伝子変異検査に関する要望書
ドライバー変異林立時代の診断の在り方を真剣に考える
TepotinibがMET exon 14 skipping mutation陽性の非小細胞肺がんに対する承認を取得
リキッドバイオプシーの回数制限緩和
診断がつかないことの喜び
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
肺がんCT検診の比較試験:JECS Study
人工知能による胸部レントゲン読影支援
末梢病変穿刺用キット・・・Periview Flex
IMpower133試験、updated data
EGFR耐性機構としてのRET融合遺伝子出現と、オシメルチニブ+selpercatinib併用療法
RET陽性肺がんの臨床的特徴と治療反応性 シンガポール国立がんセンターの報告から
RET融合遺伝子陽性肺がんに対するselpercatinibの第III相試験:LIBRETTO-431試験の概要
オンコマインDx Target Test マルチ CDxシステム一時供給停止
学会報告0004:術前診断のついていなかった小細胞肺がん手術例のまとめ
あれから20年も、この先10年も
臨床像を信じるか、病理像を信じるか
「Class IIIB」を異なる立場で見てみると
経気管支肺生検の下準備
ドライバー遺伝子変異検査に関する要望書
ドライバー変異林立時代の診断の在り方を真剣に考える
TepotinibがMET exon 14 skipping mutation陽性の非小細胞肺がんに対する承認を取得
リキッドバイオプシーの回数制限緩和
Posted by tak at 01:22│Comments(3)
│検査法
この記事へのコメント
tak先生、いつものようにタイムリーな研究を紹介頂き有り難うございます。家内は主治医からの紹介で、リキッドバイオプシーの治験を受ける予定だったのですが、病院内の事務手続きが遅れに遅れ、今月、待てずに生検を受けました。生検を嫌がっていましたので、リキッドバイオプシーで変異が確認出来なければ、生検という2段階方式は良いと思っていましたが、検査結果を得るのに2から3週間かかりますので、入院までとなると、最長6から7週間次の治療に移れないことになってしまいます。現場で使うにはもう少し検査期間を短くしないと、病状によっては厳しいと思いました。他方、今回は主治医にお願いして、麻酔を使って貰ったところ、生検は随分楽だったと家内は言っていました。
Posted by あさかぜ at 2017年01月22日 12:07
あさかぜさんへ
コメントありがとうございます。リキッドバイオプシーはT790M(を含めたEGFR変異)検索をできるだけ多くの患者さんに受けて頂くために大切な検査です。しかし、今のところ我が国では初回の通常生検でEGFR遺伝子変異が確認されたのち、病勢進行してからの再生検目的でしか認められていません。初回診断時には使えません。また、これは強調しておかなければなりませんが、リキッドバイオプシーでT790Mが検出されなかったからといって、その患者さんにT790Mが関わっていないとは言い切れないことです。「血漿でT790M陰性と判定された患者のうち、腫瘍組織でT790M陽性と判定された患者の奏効割合31/45=69%および無増悪生存期間中央値16.5ヶ月は、腫瘍組織でT790M陰性と判定された患者の奏効割合10/40=25%および無増悪生存期間中央値2.8ヶ月よりも有意に優れていた(p<0.001, p<0.001)」というのはは、患者さんも医療者も重く受け止めなければならない結果です。むしろ、リキッドバイオプシーでT790M陰性だった患者さんにこそ、通常生検でのT790M検索を受けて頂きたいです。
はっきりいって、通常生検が可能な患者さんは、同時に両検査を受けてもいいんじゃないでしょうか。高額な薬を効果が出るかどうかもわからずに使い続けるよりは、1回の検査にそこそこのお金をかけてその後の治療の見通しをきちんとつけた方が有意義です。
検査結果を得るまでのタイムラグは確かに問題です。全ての患者さんが検査結果が出るまでの1ヶ月を待てる病状とは限りません。
気管支鏡生検時の麻酔(鎮静)は、現場の検査医がしっかり考えないといけません。大学で若手の仕事を見ていても、再生検を患者さんに受け入れてもらいやすくするために、初回生検時から検査の苦痛を少なくする、といった配慮はまだ欠けているようです。もっとも、鎮静をかけすぎると検査そのもののリスクが高くなることもありますから、その点は要考慮です。
コメントありがとうございます。リキッドバイオプシーはT790M(を含めたEGFR変異)検索をできるだけ多くの患者さんに受けて頂くために大切な検査です。しかし、今のところ我が国では初回の通常生検でEGFR遺伝子変異が確認されたのち、病勢進行してからの再生検目的でしか認められていません。初回診断時には使えません。また、これは強調しておかなければなりませんが、リキッドバイオプシーでT790Mが検出されなかったからといって、その患者さんにT790Mが関わっていないとは言い切れないことです。「血漿でT790M陰性と判定された患者のうち、腫瘍組織でT790M陽性と判定された患者の奏効割合31/45=69%および無増悪生存期間中央値16.5ヶ月は、腫瘍組織でT790M陰性と判定された患者の奏効割合10/40=25%および無増悪生存期間中央値2.8ヶ月よりも有意に優れていた(p<0.001, p<0.001)」というのはは、患者さんも医療者も重く受け止めなければならない結果です。むしろ、リキッドバイオプシーでT790M陰性だった患者さんにこそ、通常生検でのT790M検索を受けて頂きたいです。
はっきりいって、通常生検が可能な患者さんは、同時に両検査を受けてもいいんじゃないでしょうか。高額な薬を効果が出るかどうかもわからずに使い続けるよりは、1回の検査にそこそこのお金をかけてその後の治療の見通しをきちんとつけた方が有意義です。
検査結果を得るまでのタイムラグは確かに問題です。全ての患者さんが検査結果が出るまでの1ヶ月を待てる病状とは限りません。
気管支鏡生検時の麻酔(鎮静)は、現場の検査医がしっかり考えないといけません。大学で若手の仕事を見ていても、再生検を患者さんに受け入れてもらいやすくするために、初回生検時から検査の苦痛を少なくする、といった配慮はまだ欠けているようです。もっとも、鎮静をかけすぎると検査そのもののリスクが高くなることもありますから、その点は要考慮です。
Posted by tak at 2017年01月25日 08:52
tak先生、いつもながらの切れ味鋭い回答を有り難うございます。
①本論文における両検査検査の差異の病状判断への応用についてのご考察、②両検査への取組意義とも、リキッドバイオプシーが利用できる様になった今、大変重要なご示唆だと思います。
少なくとも、検査結果に一喜一憂する患者にとっては、大変有益な情報と思いますので、皆さんにも知って欲しいと思います。
個人的には、生検だけ陽性でそこにしか効かないというケースが怖いので、その様にならないように祈りたいと思います。
①本論文における両検査検査の差異の病状判断への応用についてのご考察、②両検査への取組意義とも、リキッドバイオプシーが利用できる様になった今、大変重要なご示唆だと思います。
少なくとも、検査結果に一喜一憂する患者にとっては、大変有益な情報と思いますので、皆さんにも知って欲しいと思います。
個人的には、生検だけ陽性でそこにしか効かないというケースが怖いので、その様にならないように祈りたいと思います。
Posted by あさかぜ at 2017年01月25日 20:05