2020年04月11日
脳転移、髄膜癌腫症とペンブロリズマブ
様々ある肺がんの合併症の中でも、厄介極まりないものに髄膜癌腫症(がん性髄膜炎)がある。
何度煮え湯を飲まされたことか。
髄膜癌腫症を発症すると、進行性の神経症状のために一気にPSが低下し、がん薬物療法の継続が困難となってしまう。
脳転移ならば、まだ放射線治療という手段があるからいいが、脳と脊髄を覆う脳脊髄腔がまとめて冒される髄膜癌腫症となると、そうはいかない。
脳神経外科に依頼して、オンマイヤーリザーバーを留置して治療することがあると教科書には載っているが、実際に見たことはない。
全脳・全脊髄照射をやっている施設もあるというが、これも実際に見たことはない。
ドライバー遺伝子変異陽性の患者なら、オシメルチニブとか、アレクチニブとかで、ある程度の効果が期待できる。
それではドライバー遺伝子変異陰性だったらどうすればいいのか、という話。
放射線治療で病巣からがん抗原を炙り出して、そこにペンブロリズマブをかませる、というのは、よいアイデアかもしれない。
それでも、TPSがそこそこ陽性の患者に絞った方が良さそうだが。
海外の第II相臨床試験の結果と、国内の症例報告について取り上げる。
どちらも興味深い話。
とくに、ドライバー遺伝子変異陰性の髄膜癌腫症の患者が症状発現後2年にわたり無増悪生存しているというのは、症例報告とは言えとても興味深い話である。
Pembrolizumab for management of patients with NSCLC and brain metastases: long-term results and biomarker analysis from a non-randomised, open-label, phase 2 trial.
Goldberg SB et al. Lancet Oncol 2020
doi: 10.1016/S1470-2045(20)30111-X.
背景:
未治療の脳転移を有する非小細胞肺がんや悪性黒色腫の患者を対象とし、中枢神経系病変に対するPD-1阻害効果を検証するため、ペンブロリズマブ単剤療法の第II相試験を行った。今回は、非小細胞肺がんコホートについての直近の分析結果を報告する。
方法:
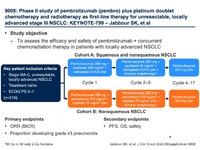
本試験はエール大学がんセンター単施設で、オープンラベル、第II相試験として行った。18歳以上、5-20mm大の脳転移を少なくとも1か所有するIV期の非小細胞肺がん患者で、脳転移に対しては未治療もしくは放射線治療後に増悪しつつある、神経症状がない、もしくはコルチコステロイド投与を必要としない、ECOG-PS 0もしくは1の患者を対象とした。中枢神経病変の評価は、modified RECIST基準を用いて行った。参加にあたり、他臓器の病変の有無は問われなかった。患者は、ペンブロリズマブ 10mg/kgを2週間ごとに静脈内投与された。患者を2つのコホートに分けた。コホート1は、PD-L1発現が少なくとも1%以上ある患者、コホート2は、PD-L1発現が1%未満、もしくは評価不能だった患者とした。主要評価項目は脳転移巣の奏効割合(部分奏効もしくは完全奏効の患者の割合)とした。治療を受けたすべての患者を有効性および安全性の評価対象とした。現時点で、本試験の患者集積は終了している。
結果:
2014年3月31日から2018年5月21日までに、42人の患者がプロトコール治療を受けた。経過観察期間中央値は8.3ヶ月(四分位間は4.5-26.2ヶ月)だった。コホート1の患者群37人のうち、11人(29.7%、95%信頼区間は15.9-47.0%)で奏効が得られ、うち4人では完全に病巣が消失していた。病勢コントロール割合は40.5%だった。奏効持続期間中央値は5.7ヶ月だった。7人(18.9%)では、中枢神経系に加えて、その他の病巣でも奏効が得られた。無増悪生存期間中央値は1.9ヶ月、中枢神経系無増悪生存期間中央値は2.3ヶ月で、1年無増悪生存割合は33%だった。生存期間中央値は9.9ヶ月で、1年生存割合は40%、2年生存割合は34%だった。Grade 3-4の有害事象は、肺臓炎2人、構成失行1人、大腸炎1人、副腎機能障害1人、高血糖1人、高カリウム血症1人だった。深刻な有害事象は42人中6人(14%)で認め、肺臓炎2人、急性腎障害1人、大腸炎1人、高カリウム血症1人、副腎機能障害1人だった。治療関連死は認めなかった。
Whole-brain Radiation and Pembrolizumab Treatment for a Non-small-cell Lung Cancer Patient with Meningeal Carcinomatosis Lacking Driver Oncogenes Led to a Long-term Survival: A Case Report.
Nakashima K et al., Intern Med 2020
doi: 10.2169/internalmedicine.4232-19.
進行原発性肺腺癌、PD-L1 60%陽性、ドライバー遺伝子変異陰性、二次化学療法の後に突然のめまい、聴覚障害、意識障害に見舞われ、髄膜癌腫症と診断した66歳女性について報告する。全脳照射とペンブロリズマブ投与を行い、引き続く三次化学療法とペンブロリズマブの併用療法を現在も継続している。本論文を執筆した段階で、髄膜癌腫症発覚から病状の進行なく、23ヶ月が経過している。今回の経験から、全脳照射と免疫チェックポイント阻害薬の併用療法は、髄膜癌腫症を発症したドライバー遺伝子変異陰性非小細胞肺がん患者に対して効果的と考える。
何度煮え湯を飲まされたことか。
髄膜癌腫症を発症すると、進行性の神経症状のために一気にPSが低下し、がん薬物療法の継続が困難となってしまう。
脳転移ならば、まだ放射線治療という手段があるからいいが、脳と脊髄を覆う脳脊髄腔がまとめて冒される髄膜癌腫症となると、そうはいかない。
脳神経外科に依頼して、オンマイヤーリザーバーを留置して治療することがあると教科書には載っているが、実際に見たことはない。
全脳・全脊髄照射をやっている施設もあるというが、これも実際に見たことはない。
ドライバー遺伝子変異陽性の患者なら、オシメルチニブとか、アレクチニブとかで、ある程度の効果が期待できる。
それではドライバー遺伝子変異陰性だったらどうすればいいのか、という話。
放射線治療で病巣からがん抗原を炙り出して、そこにペンブロリズマブをかませる、というのは、よいアイデアかもしれない。
それでも、TPSがそこそこ陽性の患者に絞った方が良さそうだが。
海外の第II相臨床試験の結果と、国内の症例報告について取り上げる。
どちらも興味深い話。
とくに、ドライバー遺伝子変異陰性の髄膜癌腫症の患者が症状発現後2年にわたり無増悪生存しているというのは、症例報告とは言えとても興味深い話である。
Pembrolizumab for management of patients with NSCLC and brain metastases: long-term results and biomarker analysis from a non-randomised, open-label, phase 2 trial.
Goldberg SB et al. Lancet Oncol 2020
doi: 10.1016/S1470-2045(20)30111-X.
背景:
未治療の脳転移を有する非小細胞肺がんや悪性黒色腫の患者を対象とし、中枢神経系病変に対するPD-1阻害効果を検証するため、ペンブロリズマブ単剤療法の第II相試験を行った。今回は、非小細胞肺がんコホートについての直近の分析結果を報告する。
方法:
本試験はエール大学がんセンター単施設で、オープンラベル、第II相試験として行った。18歳以上、5-20mm大の脳転移を少なくとも1か所有するIV期の非小細胞肺がん患者で、脳転移に対しては未治療もしくは放射線治療後に増悪しつつある、神経症状がない、もしくはコルチコステロイド投与を必要としない、ECOG-PS 0もしくは1の患者を対象とした。中枢神経病変の評価は、modified RECIST基準を用いて行った。参加にあたり、他臓器の病変の有無は問われなかった。患者は、ペンブロリズマブ 10mg/kgを2週間ごとに静脈内投与された。患者を2つのコホートに分けた。コホート1は、PD-L1発現が少なくとも1%以上ある患者、コホート2は、PD-L1発現が1%未満、もしくは評価不能だった患者とした。主要評価項目は脳転移巣の奏効割合(部分奏効もしくは完全奏効の患者の割合)とした。治療を受けたすべての患者を有効性および安全性の評価対象とした。現時点で、本試験の患者集積は終了している。
結果:
2014年3月31日から2018年5月21日までに、42人の患者がプロトコール治療を受けた。経過観察期間中央値は8.3ヶ月(四分位間は4.5-26.2ヶ月)だった。コホート1の患者群37人のうち、11人(29.7%、95%信頼区間は15.9-47.0%)で奏効が得られ、うち4人では完全に病巣が消失していた。病勢コントロール割合は40.5%だった。奏効持続期間中央値は5.7ヶ月だった。7人(18.9%)では、中枢神経系に加えて、その他の病巣でも奏効が得られた。無増悪生存期間中央値は1.9ヶ月、中枢神経系無増悪生存期間中央値は2.3ヶ月で、1年無増悪生存割合は33%だった。生存期間中央値は9.9ヶ月で、1年生存割合は40%、2年生存割合は34%だった。Grade 3-4の有害事象は、肺臓炎2人、構成失行1人、大腸炎1人、副腎機能障害1人、高血糖1人、高カリウム血症1人だった。深刻な有害事象は42人中6人(14%)で認め、肺臓炎2人、急性腎障害1人、大腸炎1人、高カリウム血症1人、副腎機能障害1人だった。治療関連死は認めなかった。
Whole-brain Radiation and Pembrolizumab Treatment for a Non-small-cell Lung Cancer Patient with Meningeal Carcinomatosis Lacking Driver Oncogenes Led to a Long-term Survival: A Case Report.
Nakashima K et al., Intern Med 2020
doi: 10.2169/internalmedicine.4232-19.
進行原発性肺腺癌、PD-L1 60%陽性、ドライバー遺伝子変異陰性、二次化学療法の後に突然のめまい、聴覚障害、意識障害に見舞われ、髄膜癌腫症と診断した66歳女性について報告する。全脳照射とペンブロリズマブ投与を行い、引き続く三次化学療法とペンブロリズマブの併用療法を現在も継続している。本論文を執筆した段階で、髄膜癌腫症発覚から病状の進行なく、23ヶ月が経過している。今回の経験から、全脳照射と免疫チェックポイント阻害薬の併用療法は、髄膜癌腫症を発症したドライバー遺伝子変異陰性非小細胞肺がん患者に対して効果的と考える。
2022年01月05日の記事より・・・がん治療とその後の療養生活
進行非小細胞肺がんオリゴ転移巣に対する定位照射のランダム化第II相比較試験
放射線治療を前処置とした免疫チェックポイント阻害薬
ドライバー遺伝子変異陽性患者におけるPACIFICレジメンの有効性
病勢進行後の治療をどう考えるか
限局型肺小細胞がんにおける海馬回避予防的全脳照射
髄膜癌腫症と姑息的全脳全脊髄放射線照射
姑息的放射線照射による遠隔腫瘍縮小(アブスコパル)効果と免疫チェックポイント阻害薬 その2
姑息的放射線照射による遠隔腫瘍縮小(アブスコパル)効果と免疫チェックポイント阻害薬 その1
肺がん診療におけるステロイド薬の使い方
アンサーとセファランチン、放射線治療とリンパ球
PACIFIC試験における5年生存割合は42.9%
学会報告0005:脳転移再発、定位放射線照射後の長期生存
ONO-4538-52/TASUKI-52試験
第3世代EGFRチロシンキナーゼ阻害薬使用後の中枢神経転移を有する患者に、オシメルチニブ「倍返し」
KEYNOTE-799試験 化学免疫放射線療法
間質性肺炎合併患者に対する定位放射線照射
oligometaに対するEGFRチロシンキナーゼ阻害薬と定位放射線照射の併用療法
全脳照射の時、海馬を避けることに意味はあるのか
脳転移を有する進行非小細胞肺がんに対する治療
進行非小細胞肺がんオリゴ転移巣に対する定位照射のランダム化第II相比較試験
放射線治療を前処置とした免疫チェックポイント阻害薬
ドライバー遺伝子変異陽性患者におけるPACIFICレジメンの有効性
病勢進行後の治療をどう考えるか
限局型肺小細胞がんにおける海馬回避予防的全脳照射
髄膜癌腫症と姑息的全脳全脊髄放射線照射
姑息的放射線照射による遠隔腫瘍縮小(アブスコパル)効果と免疫チェックポイント阻害薬 その2
姑息的放射線照射による遠隔腫瘍縮小(アブスコパル)効果と免疫チェックポイント阻害薬 その1
肺がん診療におけるステロイド薬の使い方
アンサーとセファランチン、放射線治療とリンパ球
PACIFIC試験における5年生存割合は42.9%
学会報告0005:脳転移再発、定位放射線照射後の長期生存
ONO-4538-52/TASUKI-52試験
第3世代EGFRチロシンキナーゼ阻害薬使用後の中枢神経転移を有する患者に、オシメルチニブ「倍返し」
KEYNOTE-799試験 化学免疫放射線療法
間質性肺炎合併患者に対する定位放射線照射
oligometaに対するEGFRチロシンキナーゼ阻害薬と定位放射線照射の併用療法
全脳照射の時、海馬を避けることに意味はあるのか
脳転移を有する進行非小細胞肺がんに対する治療