2017年07月30日
ICIsと分子標的薬の口演発表まとめ
2017年7月29日 日本臨床腫瘍学会総会3日目(神戸市)
口演発表のまとめ
O3-1-2:
日本人の非小細胞肺癌患者に対するニボルマブの間質性肺疾患:死亡リスク因子の検討
・発表内容をはしょりすぎていて、結局結論がわからなかった
・今回の中間解析時点で、間質性肺疾患として160人が報告された
・感染症など病因が明らかなものや、病状が悪くてCTが撮影できなかったものなど、計20人を解析対象から除外した
・免疫チェックポイント阻害薬関連間質性肺炎の画像的特徴
1)腫瘍周囲への陰影出現(peritumoral infiltration)
2)既存の放射線性線維化肺や感染巣の悪化
3)肺癌病巣がある側の肺で陰影が優勢
・画像所見を以下のごとく分類
1)急性間質性肺炎様パターン
2)Faint infiltrationパターン
3)過敏性肺臓炎様パターン
4)器質化肺炎 / 好酸球性肺炎様パターン
5)非特異的間質性肺炎様パターン
・全体を典型例と非典型例に分類
・典型例は92人、そのうち23人(25%)は死亡
・非典型例は48人、そのうち5人(10%)は死亡
・予後不良とされる急性間質性肺炎様パターンは20人(全体の14.3%)で、そのうち14人(70%)は死亡した
・予後良好とされる器質化肺炎 / 好酸球性肺炎パターンは61人(全体の43.6%)で、そのうち6人(9.8%)は死亡した
・急性間質性肺炎様パターン以外の患者120人中14人(10.8%)が死亡した
→免疫チェックポイント阻害薬関連の間質性肺炎は、殺細胞性抗がん薬関連の間質性肺炎より予後良好とされていたが、実際にはそうでもない(10人に1人は死亡する)
→典型例として発症したら4人に1人は死亡するというのは、結構深刻な気がする
→男性、治療前CRP>5mg/dlが間質性肺炎による死亡リスク因子とのこと
O3-1-3:
日本人の非小細胞肺癌患者に対するニボルマブの間質性肺疾患:中間集計における発症リスク因子の検討
・市販後臨床調査は総数3,635人で解析予定
・直近までに、ニボルマブの使用登録をした患者数は10,606人に上る
・今回は、1,005人の時点で中間解析を行った
・間質性肺炎発症報告数は58人(5.8%)で、11人(1.1%)が死亡した
・間質性肺炎発症の危険因子は、75歳以上であること、CTで既存肺に異常陰影を認めること、二次治療の使用であること、の3点だった
→O3-1-2とは解析の母集団が異なるため、わかりにくい
→危険因子がそのまま非小細胞肺癌におけるニボルマブの適用条件というのは、どうなんだろうか
→三次治療移行で使った方が安全性が高いということか
→そういえば、gefitinibで間質性肺炎の緊急安全性情報が出され、その後の調査で判明した間質性肺炎合併率は5.7%くらいだった
→実感としては、gefitinibによる間質性肺炎は当時ほどには見なくなった
O3-1-4:
非小細胞肺癌におけるNivolumabの治療効果と早期免疫関連有害事象の関係についての前向き観察研究
・免疫関連有害事象が出ると免疫チェックポイント阻害薬の治療効果が出やすいとするレトロスペクティブな報告は既にいくつかある
→Freeman et al., Clin Cancer Res 2016
→Hasan et al., Oncoimmunology 2016
・今回は、非小細胞肺癌に対するNivolumab療法開始後2週間以内に免疫関連有害事象が出るかどうかと治療効果の関連性を前向きに検討した
・対象患者数は43人
・早期免疫関連有害事象は発疹、下痢、発熱が多かった
・無増悪生存期間は早期免疫関連有害事象あり群で有意に延長していた(p=0.012)

O3-2-1:
Updated survival outcomes of NEJ005 / TCOG0902, a randomized pII of gefitinib and chemotherapy in EGFR-mutant NSCLC
・EGFR遺伝子変異陽性の進行非小細胞肺癌患者に対し、CBDCA+PEM+gefitinib併用療法→PEM+gefitinib維持療法を行うか、CBDCA+PEM併用療法→gefitinib療法→PEM維持療法→gefitinib維持療法・・・と交代療法を行うか

・後治療にOsimertinibは入っていない
→第III相試験であるNEJ009では、Osimertinibの影響をどのように考えるかが難しい
→FLAURA試験がpositiveとなってしまった以上、NEJ009の結論が出たときに、GefitinibをOsimertinibに置き換えたらどうなるのか、Osimertnib単剤と今回の併用療法ではどちらを優先するべきなのか、という議論が当然出てくるだろう
O3-2-2:
Randomaized phase 1b / 3 study of erlotinib plus ramcirumab ( RAM ) in first-line EGFR mut(+) stage IV NSCLC: phase 1b safety
・RELAY study: NCT02411448
・phase 1bに12人組み入れ、忍容性ありと認められればphase IIIに進む段取り
・日本から7人、欧米から7人が参加
・全ての患者に、なんらかの有害事象が出た
・日本人では、下痢を6人(86%)で認めた
・既知の有害事象のみだったため、現在はphase III試験が進行中
O3-2-3:
EGFR遺伝子変異陽性進行非扁平上皮非小細胞肺癌に対するアファチニブ+ベバシツマブ併用療法の第I相試験
・既報では、この患者群に対するErlotinib+bevacizumab併用療法の無増悪生存期間中央値は16ヶ月、Gefitinib+bevacizumab併用療法の無増悪生存期間中央値は14.4ヶ月
・それでは、Afatinibではどうなるか
・Afatinib 30mg/日+Bevacizumab 15mg/kgを開始量として、第I相試験を行った
・3+3 cohortで開始
・5人で試験終了
・Afatinib 30mg/日+Bevacizumab 15mg/kgでは用量制限毒性は出現せず
・Afatinib 40mg/日+Bevacizumab 15mg/kgでは2人中2人でGrade 3の下痢
・以上から、推奨用量はAfatinib 30mg/日+Bevacizumab 15mg/kgに決定
・奏効割合は40%
・病勢コントロール割合は100%
・無増悪生存期間は8.7ヶ月から18.2ヶ月
・現在は10-20人程度を組み入れ予定のexpansion cohort studyを実施中
O3-3-5:
LUX-Lung 8 (LL-8)phase III trial: Long-term response to second-line afatinib in patients with advanced SCC of the lung
・基本的には後出しじゃんけんの解析
・LL-8で1年以上生存した患者21人を検証
・この患者群での奏効割合は48%、生存期間中央値は21.1ヶ月(12.9-31.6)、ちなみに全体の生存期間中央値は7.9ヶ月
・21人中4人は50mg/日へ増量されており、それ以外の患者でも40mg/日で維持された患者が多かった
・この患者群での治療継続期間中央値は17.6ヶ月
・この患者群でErbB familyの変異解析をしてみた
EGFR遺伝子変異陽性(R1052K, V8431, L858R):全体の20%
HER2遺伝子変異陽性(E395L, Q57R):全体の20%
ErbB4遺伝子変異陽性(G668V):全体の10%
残りの50%はwild type
→Afatinibの毒性に耐えられた患者は長生きできたということだろうか
→1年以上生存できなかった患者との比較はされていなかったので、単に治療がよく効いた患者を解析したというだけの報告で、なんともコメントのしようがない
→目新しいのはErbB familyの解析をしたことだが、臨床的にどの程度の意義があるのかはよくわからない(対照群でもやっていて、差が出ていれば話は違うけれど)
O3-4-1:
Phase II study of Crizotinib in East Asian patients with ROS1+ advanced non-small cell lung cancer ( NSCLC )
・ROS1肺癌はgrobalには肺癌の1-2%、日本国内では2-4%程度
・ROS1+, ALK-が確認された患者が対象で、前治療は3レジメンまで許容

・前治療のレジメン数によらず、奏効割合はほぼ70%
・主な有害事象は嘔気や下痢で、ALK陽性肺癌に対してCrizotinibを使ったときとさしてかわらない
・RT-PCRとFISHの結果の相同性はある程度担保されている
O3-4-2:
Afatinib vs Gefitinib in patients with EGFRm+ NSCLC: Updated OS data from the phase IIb trial LUX-Lung 7 ( LL-7 )
・2016年12月5日時点でcut off, updated analysis

・自施設のみで調べた感じでは、Afatinib群でもGefitinib群でも、PD後にT790Mが検出された患者は46-47%程度という実感
→後治療のデータ、ことにT790M出現割合と第3世代TKI使用後の成績は興味深い
→FLAURA studyの結果示されるOSのデータによっては、治療シーケンスを考える必要が出てくるだろうが、早くて来年、場合によっては再来年以降にならないと見通せないだろう
O3-4-3:
First-line Afatinib for advanced EGFRm+ NSCLC: analysis of long term responders ( LTRs ) in the LUX-Lung 3, 6, 7 trials
・LTRsを「3年以上治療を継続された人」と定義
・LTRsで各種解析
・Afatinibを使用した患者のうちLTRはおおむね10-12%程度
・LL7において、LTRはGefitinib群の4%だった
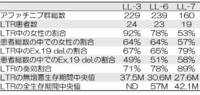
→O3-3-5同様、後出しじゃんけん解析
→女性、Ex.19 del.にLTRが多い
口演発表のまとめ
O3-1-2:
日本人の非小細胞肺癌患者に対するニボルマブの間質性肺疾患:死亡リスク因子の検討
・発表内容をはしょりすぎていて、結局結論がわからなかった
・今回の中間解析時点で、間質性肺疾患として160人が報告された
・感染症など病因が明らかなものや、病状が悪くてCTが撮影できなかったものなど、計20人を解析対象から除外した
・免疫チェックポイント阻害薬関連間質性肺炎の画像的特徴
1)腫瘍周囲への陰影出現(peritumoral infiltration)
2)既存の放射線性線維化肺や感染巣の悪化
3)肺癌病巣がある側の肺で陰影が優勢
・画像所見を以下のごとく分類
1)急性間質性肺炎様パターン
2)Faint infiltrationパターン
3)過敏性肺臓炎様パターン
4)器質化肺炎 / 好酸球性肺炎様パターン
5)非特異的間質性肺炎様パターン
・全体を典型例と非典型例に分類
・典型例は92人、そのうち23人(25%)は死亡
・非典型例は48人、そのうち5人(10%)は死亡
・予後不良とされる急性間質性肺炎様パターンは20人(全体の14.3%)で、そのうち14人(70%)は死亡した
・予後良好とされる器質化肺炎 / 好酸球性肺炎パターンは61人(全体の43.6%)で、そのうち6人(9.8%)は死亡した
・急性間質性肺炎様パターン以外の患者120人中14人(10.8%)が死亡した
→免疫チェックポイント阻害薬関連の間質性肺炎は、殺細胞性抗がん薬関連の間質性肺炎より予後良好とされていたが、実際にはそうでもない(10人に1人は死亡する)
→典型例として発症したら4人に1人は死亡するというのは、結構深刻な気がする
→男性、治療前CRP>5mg/dlが間質性肺炎による死亡リスク因子とのこと
O3-1-3:
日本人の非小細胞肺癌患者に対するニボルマブの間質性肺疾患:中間集計における発症リスク因子の検討
・市販後臨床調査は総数3,635人で解析予定
・直近までに、ニボルマブの使用登録をした患者数は10,606人に上る
・今回は、1,005人の時点で中間解析を行った
・間質性肺炎発症報告数は58人(5.8%)で、11人(1.1%)が死亡した
・間質性肺炎発症の危険因子は、75歳以上であること、CTで既存肺に異常陰影を認めること、二次治療の使用であること、の3点だった
→O3-1-2とは解析の母集団が異なるため、わかりにくい
→危険因子がそのまま非小細胞肺癌におけるニボルマブの適用条件というのは、どうなんだろうか
→三次治療移行で使った方が安全性が高いということか
→そういえば、gefitinibで間質性肺炎の緊急安全性情報が出され、その後の調査で判明した間質性肺炎合併率は5.7%くらいだった
→実感としては、gefitinibによる間質性肺炎は当時ほどには見なくなった
O3-1-4:
非小細胞肺癌におけるNivolumabの治療効果と早期免疫関連有害事象の関係についての前向き観察研究
・免疫関連有害事象が出ると免疫チェックポイント阻害薬の治療効果が出やすいとするレトロスペクティブな報告は既にいくつかある
→Freeman et al., Clin Cancer Res 2016
→Hasan et al., Oncoimmunology 2016
・今回は、非小細胞肺癌に対するNivolumab療法開始後2週間以内に免疫関連有害事象が出るかどうかと治療効果の関連性を前向きに検討した
・対象患者数は43人
・早期免疫関連有害事象は発疹、下痢、発熱が多かった
・無増悪生存期間は早期免疫関連有害事象あり群で有意に延長していた(p=0.012)

O3-2-1:
Updated survival outcomes of NEJ005 / TCOG0902, a randomized pII of gefitinib and chemotherapy in EGFR-mutant NSCLC
・EGFR遺伝子変異陽性の進行非小細胞肺癌患者に対し、CBDCA+PEM+gefitinib併用療法→PEM+gefitinib維持療法を行うか、CBDCA+PEM併用療法→gefitinib療法→PEM維持療法→gefitinib維持療法・・・と交代療法を行うか

・後治療にOsimertinibは入っていない
→第III相試験であるNEJ009では、Osimertinibの影響をどのように考えるかが難しい
→FLAURA試験がpositiveとなってしまった以上、NEJ009の結論が出たときに、GefitinibをOsimertinibに置き換えたらどうなるのか、Osimertnib単剤と今回の併用療法ではどちらを優先するべきなのか、という議論が当然出てくるだろう
O3-2-2:
Randomaized phase 1b / 3 study of erlotinib plus ramcirumab ( RAM ) in first-line EGFR mut(+) stage IV NSCLC: phase 1b safety
・RELAY study: NCT02411448
・phase 1bに12人組み入れ、忍容性ありと認められればphase IIIに進む段取り
・日本から7人、欧米から7人が参加
・全ての患者に、なんらかの有害事象が出た
・日本人では、下痢を6人(86%)で認めた
・既知の有害事象のみだったため、現在はphase III試験が進行中
O3-2-3:
EGFR遺伝子変異陽性進行非扁平上皮非小細胞肺癌に対するアファチニブ+ベバシツマブ併用療法の第I相試験
・既報では、この患者群に対するErlotinib+bevacizumab併用療法の無増悪生存期間中央値は16ヶ月、Gefitinib+bevacizumab併用療法の無増悪生存期間中央値は14.4ヶ月
・それでは、Afatinibではどうなるか
・Afatinib 30mg/日+Bevacizumab 15mg/kgを開始量として、第I相試験を行った
・3+3 cohortで開始
・5人で試験終了
・Afatinib 30mg/日+Bevacizumab 15mg/kgでは用量制限毒性は出現せず
・Afatinib 40mg/日+Bevacizumab 15mg/kgでは2人中2人でGrade 3の下痢
・以上から、推奨用量はAfatinib 30mg/日+Bevacizumab 15mg/kgに決定
・奏効割合は40%
・病勢コントロール割合は100%
・無増悪生存期間は8.7ヶ月から18.2ヶ月
・現在は10-20人程度を組み入れ予定のexpansion cohort studyを実施中
O3-3-5:
LUX-Lung 8 (LL-8)phase III trial: Long-term response to second-line afatinib in patients with advanced SCC of the lung
・基本的には後出しじゃんけんの解析
・LL-8で1年以上生存した患者21人を検証
・この患者群での奏効割合は48%、生存期間中央値は21.1ヶ月(12.9-31.6)、ちなみに全体の生存期間中央値は7.9ヶ月
・21人中4人は50mg/日へ増量されており、それ以外の患者でも40mg/日で維持された患者が多かった
・この患者群での治療継続期間中央値は17.6ヶ月
・この患者群でErbB familyの変異解析をしてみた
EGFR遺伝子変異陽性(R1052K, V8431, L858R):全体の20%
HER2遺伝子変異陽性(E395L, Q57R):全体の20%
ErbB4遺伝子変異陽性(G668V):全体の10%
残りの50%はwild type
→Afatinibの毒性に耐えられた患者は長生きできたということだろうか
→1年以上生存できなかった患者との比較はされていなかったので、単に治療がよく効いた患者を解析したというだけの報告で、なんともコメントのしようがない
→目新しいのはErbB familyの解析をしたことだが、臨床的にどの程度の意義があるのかはよくわからない(対照群でもやっていて、差が出ていれば話は違うけれど)
O3-4-1:
Phase II study of Crizotinib in East Asian patients with ROS1+ advanced non-small cell lung cancer ( NSCLC )
・ROS1肺癌はgrobalには肺癌の1-2%、日本国内では2-4%程度
・ROS1+, ALK-が確認された患者が対象で、前治療は3レジメンまで許容

・前治療のレジメン数によらず、奏効割合はほぼ70%
・主な有害事象は嘔気や下痢で、ALK陽性肺癌に対してCrizotinibを使ったときとさしてかわらない
・RT-PCRとFISHの結果の相同性はある程度担保されている
O3-4-2:
Afatinib vs Gefitinib in patients with EGFRm+ NSCLC: Updated OS data from the phase IIb trial LUX-Lung 7 ( LL-7 )
・2016年12月5日時点でcut off, updated analysis

・自施設のみで調べた感じでは、Afatinib群でもGefitinib群でも、PD後にT790Mが検出された患者は46-47%程度という実感
→後治療のデータ、ことにT790M出現割合と第3世代TKI使用後の成績は興味深い
→FLAURA studyの結果示されるOSのデータによっては、治療シーケンスを考える必要が出てくるだろうが、早くて来年、場合によっては再来年以降にならないと見通せないだろう
O3-4-3:
First-line Afatinib for advanced EGFRm+ NSCLC: analysis of long term responders ( LTRs ) in the LUX-Lung 3, 6, 7 trials
・LTRsを「3年以上治療を継続された人」と定義
・LTRsで各種解析
・Afatinibを使用した患者のうちLTRはおおむね10-12%程度
・LL7において、LTRはGefitinib群の4%だった

→O3-3-5同様、後出しじゃんけん解析
→女性、Ex.19 del.にLTRが多い
・Reiwa研究から・・・オシメルチニブ初回治療後、その他のEGFR-TKIでrechallenge治療をしたら
・Osi-risk TORG-TG2101試験・・・オシメルチニブ投与中止後のEGFR-TKI再投与とその安全性について
セルペルカチニブ、上市
CLIP1-LTK融合遺伝子の発見・・・LC-SCRUM Asiaから
セルペルカチニブ、2021年12月13日発売予定
セルペルカチニブと過敏症
血液脳関門とがん薬物療法
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
脳転移を有する患者集団に対しても、免疫チェックポイント阻害薬は有効なのか
HER2エクソン20挿入変異陽性非小細胞肺がんに対するpoziotinib
セルペルカチニブの添付文書
第4世代ALK阻害薬・・・TPX-0131とNVL-655
セルペルカチニブ、製造販売承認
HER2遺伝子変異陽性肺がんに対するtrastuzumab deruxtecan
オシメルチニブ耐性化後は、耐性機序同定や分子標的治療は意味がないのか
EGFR/ALK陽性非小細胞肺がんに対するカルボプラチン+ペメトレキセド+ペンブロリズマブ併用療法
中国人患者におけるRET阻害薬(Selpercatinib, Pralsetinib)の有効性
オシメルチニブによる術前療法・・・NeoADAURAの前哨戦
病勢進行後の治療をどう考えるか
RET阻害薬、セルペルカチニブがやってくる
・Osi-risk TORG-TG2101試験・・・オシメルチニブ投与中止後のEGFR-TKI再投与とその安全性について
セルペルカチニブ、上市
CLIP1-LTK融合遺伝子の発見・・・LC-SCRUM Asiaから
セルペルカチニブ、2021年12月13日発売予定
セルペルカチニブと過敏症
血液脳関門とがん薬物療法
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
脳転移を有する患者集団に対しても、免疫チェックポイント阻害薬は有効なのか
HER2エクソン20挿入変異陽性非小細胞肺がんに対するpoziotinib
セルペルカチニブの添付文書
第4世代ALK阻害薬・・・TPX-0131とNVL-655
セルペルカチニブ、製造販売承認
HER2遺伝子変異陽性肺がんに対するtrastuzumab deruxtecan
オシメルチニブ耐性化後は、耐性機序同定や分子標的治療は意味がないのか
EGFR/ALK陽性非小細胞肺がんに対するカルボプラチン+ペメトレキセド+ペンブロリズマブ併用療法
中国人患者におけるRET阻害薬(Selpercatinib, Pralsetinib)の有効性
オシメルチニブによる術前療法・・・NeoADAURAの前哨戦
病勢進行後の治療をどう考えるか
RET阻害薬、セルペルカチニブがやってくる








