2017年07月28日
KEYNOTE-024の日本人サブグループ解析
2017年7月28日 日本臨床腫瘍学会総会2日目(神戸市)
KEYNOTE-024の日本人サブグループ解析。
サブグループ解析なので人数は少ないけれど、確かに有望な結果。
Plenary session 3:
PD-L1高発現の見治療非小細胞肺がんに対するPembrolizumabの国際共同ランダム化第III相比較試験(KEYNOTE-024)の日本人集団解析
・PD-L1発現>50%の進行非小細胞肺癌患者を対象に、一次治療におけるPembrolizumabとプラチナ併用化学療法を比較する第III相試験
・主要評価項目は無増悪生存期間
・副次評価項目は全生存期間、奏効割合、安全性
・化学療法群が病勢進行に至った際、Pembrolizumabへのクロスオーバーを許容する
→全体では、化学療法群の50%がPembrolizumab療法に移行した

・化学療法群は全て病勢進行に至った
・アジアから参加したのは日本人のみ、n=40, PFSのHR 0.35 ( 0.14-0.91 )
アジア以外から参加したのはn=265、PFSのHR 0.52 ( 0.38-0.72 )
以下は、discussantからの意見。
・無増悪生存期間の生存曲線は、初期に大きく落ち込む:初期耐性
→機序を明らかにする必要あり
・Peters et al., AACR 2017, tumor mutational burdenはPD-L1発現と相関せず
・Joshua et al., ASCO 2017, MET増幅があると、PD-L1陽性でも免疫チェックポイント阻害薬は無効、PD-L1>50%が6人いたが、全てPD
・Hamanishi et al., Int J Clin Oncol. 2016 Jun;21(3):462-73
→https://www.ncbi.nlm.nih.gov/pubmed/26899259
免疫チェックポイント阻害薬開発に関するoverview
KEYNOTE-024の日本人サブグループ解析。
サブグループ解析なので人数は少ないけれど、確かに有望な結果。
Plenary session 3:
PD-L1高発現の見治療非小細胞肺がんに対するPembrolizumabの国際共同ランダム化第III相比較試験(KEYNOTE-024)の日本人集団解析
・PD-L1発現>50%の進行非小細胞肺癌患者を対象に、一次治療におけるPembrolizumabとプラチナ併用化学療法を比較する第III相試験
・主要評価項目は無増悪生存期間
・副次評価項目は全生存期間、奏効割合、安全性
・化学療法群が病勢進行に至った際、Pembrolizumabへのクロスオーバーを許容する
→全体では、化学療法群の50%がPembrolizumab療法に移行した

・化学療法群は全て病勢進行に至った
・アジアから参加したのは日本人のみ、n=40, PFSのHR 0.35 ( 0.14-0.91 )
アジア以外から参加したのはn=265、PFSのHR 0.52 ( 0.38-0.72 )
以下は、discussantからの意見。
・無増悪生存期間の生存曲線は、初期に大きく落ち込む:初期耐性
→機序を明らかにする必要あり
・Peters et al., AACR 2017, tumor mutational burdenはPD-L1発現と相関せず
・Joshua et al., ASCO 2017, MET増幅があると、PD-L1陽性でも免疫チェックポイント阻害薬は無効、PD-L1>50%が6人いたが、全てPD
・Hamanishi et al., Int J Clin Oncol. 2016 Jun;21(3):462-73
→https://www.ncbi.nlm.nih.gov/pubmed/26899259
免疫チェックポイント阻害薬開発に関するoverview
2017年07月28日
EGFR遺伝子変異陽性肺癌に対する治療戦略
2017年7月28日 日本臨床腫瘍学会2日目(神戸市)
昨日に続いて、スペインからお越しになった先生のご講演。
Medical Seminer (=Lanchon Seminer) 25
Grobal Strategies for the Treatment of EGFR Mutation Positive Patient
・1st lineとしてErlotinib, Afatinib, Gefitinibを使用可能
・治療中にほぼ例外なく耐性化し、治癒には至らない
・T790M陽性が確認できたら、Osimertinibを使用可能
・liquid biopsyも利用可能になった
・アジア人におけるEGFR遺伝子変異出現頻度
中国:50.2%
香港:47.2%
フィリピン:52.3%
台湾:62.1%
タイ:53.1%
・EURTAC study: Lancet Oncol 239-246, 2012
PFSはErlotinib群で9.7ヶ月、化学療法群で5.2ヶ月
Erlotinib群にも完全奏効の患者はおらず、みんな耐性化
・これまでのところ、一次治療としては、Afatinibは化学療法に対してOS延長効果を示した唯一のEGFR阻害薬(LUX-Lung 3 and 6 pooled analysis)
・Erlotinib 25mg is equivalent to gefitinib 250mg
→Yeo et al., J Thorac Oncol. 2010 Jul;5(7):1048-53
→https://www.ncbi.nlm.nih.gov/pubmed/20512075
・EGFR阻害薬同士のHead to Head studies
→CTONG0901: Yang et al., Br J Cancer. 2017 Feb 28;116(5):568-574
https://www.ncbi.nlm.nih.gov/pubmed/28103612
→WJOG5108L: Urata et al., J Clin Oncol. 2016 Sep 20;34(27):3248-57
https://www.ncbi.nlm.nih.gov/pubmed/27022112
→LUX-Lung 7: Paz-Ares et al., Ann Oncol. 2017 Feb 1;28(2):270-277, Corral et al., ELCC #93PD
Asian subgroupではHR 0.76, non-Asian subgroupではHR 0.72
https://www.ncbi.nlm.nih.gov/pubmed/28426106
→ARCHER 1050: Mok et al., ASCO 2017
→http://oitahaiganpractice.junglekouen.com/e900757.html
Asian subgroupではHR 0.51(0.39-0.66)
Non-Asian subgroupではHR 0.89(0.57-1.39)
・脳転移を有するEGFR遺伝子変異陽性患者の取り扱い
→Magnuson et al., J Clin Oncol. 2017 Apr 1;35(10):1070-1077
→https://www.ncbi.nlm.nih.gov/pubmed/28113019
EGFR阻害薬未治療で、脳転移を合併したEGFR遺伝子変異陽性の患者を後ろ向きに検討
定位照射の後にEGFR阻害薬を使った人、全脳照射の後にEGFR阻害薬を使った人、EGFR阻害薬を使った後に脳転移巣が悪化したら定位照射か全脳照射をした人の順に全生存期間が長く、それぞれの中央値は46ヶ月、30ヶ月、25ヶ月で、EGFR阻害薬を先に使ったほうが統計学的有意に予後不良だった
→中枢神経移行のよいOsimertinibが一次治療で使えるようになったら、前向きに検証すべきテーマだ
・minor mutationの患者にはafatinibがよい
・Hata et al., Nature Med 2016
Heterogeneity, early phase T790M evolution and late phase T790M evolution
・BELIEF trial: Erlotinib+Bevacizumabの治療効果はT790M statusによって異なる
OSはallで13.2ヶ月、T790M(+)群で16ヶ月、T790(-)群で10.5ヶ月
→https://www.ncbi.nlm.nih.gov/pubmed/28408243
・各種EGFR阻害薬の脳への集積:カニクイザルとPETを用いて可視化
→Ballard et al., Clin Cancer Res. 2016 Oct 15;22(20):5130-5140
→https://www.ncbi.nlm.nih.gov/pubmed/27435396
・EURTAXにおけるExon 21変異患者とctDNAの推移
→Karachaliou et al, Expert Opin Pharmacother. 2017 Feb;18(3):295-304
→https://www.ncbi.nlm.nih.gov/pubmed/28103738
・FLAURA studyがpositiveだったと2017/07/27にプレスリリース
→http://oitahaiganpractice.junglekouen.com/e906089.html
昨日に続いて、スペインからお越しになった先生のご講演。
Medical Seminer (=Lanchon Seminer) 25
Grobal Strategies for the Treatment of EGFR Mutation Positive Patient
・1st lineとしてErlotinib, Afatinib, Gefitinibを使用可能
・治療中にほぼ例外なく耐性化し、治癒には至らない
・T790M陽性が確認できたら、Osimertinibを使用可能
・liquid biopsyも利用可能になった
・アジア人におけるEGFR遺伝子変異出現頻度
中国:50.2%
香港:47.2%
フィリピン:52.3%
台湾:62.1%
タイ:53.1%
・EURTAC study: Lancet Oncol 239-246, 2012
PFSはErlotinib群で9.7ヶ月、化学療法群で5.2ヶ月
Erlotinib群にも完全奏効の患者はおらず、みんな耐性化
・これまでのところ、一次治療としては、Afatinibは化学療法に対してOS延長効果を示した唯一のEGFR阻害薬(LUX-Lung 3 and 6 pooled analysis)
・Erlotinib 25mg is equivalent to gefitinib 250mg
→Yeo et al., J Thorac Oncol. 2010 Jul;5(7):1048-53
→https://www.ncbi.nlm.nih.gov/pubmed/20512075
・EGFR阻害薬同士のHead to Head studies
→CTONG0901: Yang et al., Br J Cancer. 2017 Feb 28;116(5):568-574
https://www.ncbi.nlm.nih.gov/pubmed/28103612
→WJOG5108L: Urata et al., J Clin Oncol. 2016 Sep 20;34(27):3248-57
https://www.ncbi.nlm.nih.gov/pubmed/27022112
→LUX-Lung 7: Paz-Ares et al., Ann Oncol. 2017 Feb 1;28(2):270-277, Corral et al., ELCC #93PD
Asian subgroupではHR 0.76, non-Asian subgroupではHR 0.72
https://www.ncbi.nlm.nih.gov/pubmed/28426106
→ARCHER 1050: Mok et al., ASCO 2017
→http://oitahaiganpractice.junglekouen.com/e900757.html
Asian subgroupではHR 0.51(0.39-0.66)
Non-Asian subgroupではHR 0.89(0.57-1.39)
・脳転移を有するEGFR遺伝子変異陽性患者の取り扱い
→Magnuson et al., J Clin Oncol. 2017 Apr 1;35(10):1070-1077
→https://www.ncbi.nlm.nih.gov/pubmed/28113019
EGFR阻害薬未治療で、脳転移を合併したEGFR遺伝子変異陽性の患者を後ろ向きに検討
定位照射の後にEGFR阻害薬を使った人、全脳照射の後にEGFR阻害薬を使った人、EGFR阻害薬を使った後に脳転移巣が悪化したら定位照射か全脳照射をした人の順に全生存期間が長く、それぞれの中央値は46ヶ月、30ヶ月、25ヶ月で、EGFR阻害薬を先に使ったほうが統計学的有意に予後不良だった
→中枢神経移行のよいOsimertinibが一次治療で使えるようになったら、前向きに検証すべきテーマだ
・minor mutationの患者にはafatinibがよい
・Hata et al., Nature Med 2016
Heterogeneity, early phase T790M evolution and late phase T790M evolution
・BELIEF trial: Erlotinib+Bevacizumabの治療効果はT790M statusによって異なる
OSはallで13.2ヶ月、T790M(+)群で16ヶ月、T790(-)群で10.5ヶ月
→https://www.ncbi.nlm.nih.gov/pubmed/28408243
・各種EGFR阻害薬の脳への集積:カニクイザルとPETを用いて可視化
→Ballard et al., Clin Cancer Res. 2016 Oct 15;22(20):5130-5140
→https://www.ncbi.nlm.nih.gov/pubmed/27435396
・EURTAXにおけるExon 21変異患者とctDNAの推移
→Karachaliou et al, Expert Opin Pharmacother. 2017 Feb;18(3):295-304
→https://www.ncbi.nlm.nih.gov/pubmed/28103738
・FLAURA studyがpositiveだったと2017/07/27にプレスリリース
→http://oitahaiganpractice.junglekouen.com/e906089.html
2017年07月28日
周術期化学療法におけるがん薬物療法専門医の役割
2017年7月28日 日本臨床腫瘍学会総会2日目(神戸市)
会員委員会企画
周術期化学療法におけるがん薬物療法専門医の役割
・・・結局のところ、各病院でルールを決めて取り組むべきことだ。
呼吸器内科医と呼吸器外科医は同じ呼吸器センターで働いていることが多いが、腫瘍内科医と呼吸器外科医は必ずしもそうではない。
いつも近くにいるかいないかというのは、結構大きな違いだと思う。
多分、他の領域でもそうではないだろうか。
「いつでも、face to faceで気楽に相談できる」というのが何より大切なのだ。
MMP1-1
外科系薬物療法専門医の立場から
・大きな大学病院の消化器外科医の先生が発言
・消化器外科系の臨床試験は術式検討のたゆまぬ繰り返し
・より低侵襲に、より効果的に
・外科医の殆どは、切除範囲を広げても癌は取り除けないし、治療成績は高まらないと漠然と考えている
・消化器外科の術前・術後には、消化器外科医でないと対応できないようなさまざまな合併症が待ち受けている
・諸問題に対応しようと思ったら、消化器外科医が薬物療法に習熟して一貫した治療を行うのが理にかなっている
MMP1-2
内科系薬物療法専門医の立場から
・大きな大学病院の腫瘍内科主任教授、臨床腫瘍学会のone of the leaderが発言
・外科とか内科とかこだわらず、それぞれの得意分野を活かしてチームとして取り組みましょう
・臓器横断的に、幅広い知識を有する臨床腫瘍医が治療に携わることは、メリットが大きい
・日本と韓国が一緒にやった、肝細胞がんに対するsorafenib療法の検証的試験
→日本では標準治療と差が出ず、韓国では圧倒的な差がついた
→患者背景も治療法も差がなく、唯一差があったのは、日本では非腫瘍内科医が、韓国では腫瘍内科医が患者を担当した
→日本の方が累積投与量が少なく、治療期間も短かった・・・有害事象をうまくマネジメントできなかったことが原因では?
・がん薬物療法専門医はそれなりに増えてきた
総数:1229人
都道府県がん診療拠点病院に在籍:326人(26.5%)
地域がん診療連携拠点病院に在籍:527人(42.9%)
がんセンターに在籍:55人(4.5%)
その他の病院に在籍:288人(23.4%)
病院以外に在籍(政府機関、研究機関、海外留学中など):33人(2.7%)
・都道府県がん診療連携拠点病院全49施設の中で、
がん薬物療法専門医がいない病院:1施設(2%)
がん薬物療法専門医が1人しかいない病院:3施設(6%)
がん薬物療法専門医が2人しかいない病院:8施設(16%)
がん薬物療法専門医が3人しかいない病院:6施設(12%)
→全体の1/3では専門医が3人以下
・地域がん診療連携拠点病院全350病院中、がん薬物療法専門医がいない病院は151施設(43.1%)
MMP1-3
呼吸器内科系薬物療法専門医の立場から
・首都圏のがんセンターに勤める肺癌領域のone of opinion leaderが発現
・先にしゃべった二人の演者、どちらにも賛成できない
・薬物療法の実務は、各臓器専門の腫瘍内科医が担当すべきだろう
・そもそも肺癌は、全体の75%が治癒不能で、外科医の出る幕はない
・術後補助化学療法を内科に依頼するにあたり、術後の5年生存割合や術後補助化学療法に期待できる効果について説明していない外科医が結構いて、信用できない
・プラチナ併用化学療法やUFTの術後補助療法なら、マンパワーがある程度ある外科ならできなくはないだろう
・術前化学療法となると、許容できる毒性や手術のタイミングを測るために、内科医と外科医の密な連携が欠かせない
・術前治療にこだわりすぎて、手術が出来なかったらなんにもならない
・今後周術期に抗がん薬、分子標的薬、免疫チェックポイント阻害薬が導入されたら、多分外科医では管理できなくなる
MMP1-4
皮膚科の立場から
・中部地方のがんセンターに勤める皮膚科医が発言
・皮膚科医は、免疫チェックポイント阻害薬を扱うようになって、考え方も考えられ方も変わった
昔の皮膚科医:
独自性が高く、閉鎖的な考え方を持ち、チーム医療には消極的
今の皮膚科医:がん薬物療法専門医のサポートをすることが多くなった
チーム医療に組み入れられるようになった
いろんな治療を見て、薬物療法への理解が進んだ
悪性黒色腫の治療を介して、他の診療科との連携が進んだ
がん薬物療法に対しては、駆け出し者の立場
昔の腫瘍内科医:
皮膚領域に対する関心が少ない、皮膚合併症は見過ごしがち、チーム医療には積極的
今の腫瘍内科医:
皮膚科医の治療をサポートしてくれる(治療選択、用量設定、有害事象管理など)
悪性黒色腫の治療に免疫チェックポイント阻害薬が導入されたことで、皮膚科領域への注目度が高まった
悪性黒色腫の患者の管理を手伝って、経験をつんで、自分たちの治療に活かそうと目論んでいる
あわよくば、悪性黒色腫の治療も皮膚科医から奪おうとしているきらいがある、縄張り荒らし
・免疫チェックポイント阻害薬と併用することで、皮膚合併症を起こしやすいとされる薬がある
去痰薬、プロトンポンプ阻害薬、ST合剤、抗痙攣薬、ベムラフェニブ、アレクチニブ
会員委員会企画
周術期化学療法におけるがん薬物療法専門医の役割
・・・結局のところ、各病院でルールを決めて取り組むべきことだ。
呼吸器内科医と呼吸器外科医は同じ呼吸器センターで働いていることが多いが、腫瘍内科医と呼吸器外科医は必ずしもそうではない。
いつも近くにいるかいないかというのは、結構大きな違いだと思う。
多分、他の領域でもそうではないだろうか。
「いつでも、face to faceで気楽に相談できる」というのが何より大切なのだ。
MMP1-1
外科系薬物療法専門医の立場から
・大きな大学病院の消化器外科医の先生が発言
・消化器外科系の臨床試験は術式検討のたゆまぬ繰り返し
・より低侵襲に、より効果的に
・外科医の殆どは、切除範囲を広げても癌は取り除けないし、治療成績は高まらないと漠然と考えている
・消化器外科の術前・術後には、消化器外科医でないと対応できないようなさまざまな合併症が待ち受けている
・諸問題に対応しようと思ったら、消化器外科医が薬物療法に習熟して一貫した治療を行うのが理にかなっている
MMP1-2
内科系薬物療法専門医の立場から
・大きな大学病院の腫瘍内科主任教授、臨床腫瘍学会のone of the leaderが発言
・外科とか内科とかこだわらず、それぞれの得意分野を活かしてチームとして取り組みましょう
・臓器横断的に、幅広い知識を有する臨床腫瘍医が治療に携わることは、メリットが大きい
・日本と韓国が一緒にやった、肝細胞がんに対するsorafenib療法の検証的試験
→日本では標準治療と差が出ず、韓国では圧倒的な差がついた
→患者背景も治療法も差がなく、唯一差があったのは、日本では非腫瘍内科医が、韓国では腫瘍内科医が患者を担当した
→日本の方が累積投与量が少なく、治療期間も短かった・・・有害事象をうまくマネジメントできなかったことが原因では?
・がん薬物療法専門医はそれなりに増えてきた
総数:1229人
都道府県がん診療拠点病院に在籍:326人(26.5%)
地域がん診療連携拠点病院に在籍:527人(42.9%)
がんセンターに在籍:55人(4.5%)
その他の病院に在籍:288人(23.4%)
病院以外に在籍(政府機関、研究機関、海外留学中など):33人(2.7%)
・都道府県がん診療連携拠点病院全49施設の中で、
がん薬物療法専門医がいない病院:1施設(2%)
がん薬物療法専門医が1人しかいない病院:3施設(6%)
がん薬物療法専門医が2人しかいない病院:8施設(16%)
がん薬物療法専門医が3人しかいない病院:6施設(12%)
→全体の1/3では専門医が3人以下
・地域がん診療連携拠点病院全350病院中、がん薬物療法専門医がいない病院は151施設(43.1%)
MMP1-3
呼吸器内科系薬物療法専門医の立場から
・首都圏のがんセンターに勤める肺癌領域のone of opinion leaderが発現
・先にしゃべった二人の演者、どちらにも賛成できない
・薬物療法の実務は、各臓器専門の腫瘍内科医が担当すべきだろう
・そもそも肺癌は、全体の75%が治癒不能で、外科医の出る幕はない
・術後補助化学療法を内科に依頼するにあたり、術後の5年生存割合や術後補助化学療法に期待できる効果について説明していない外科医が結構いて、信用できない
・プラチナ併用化学療法やUFTの術後補助療法なら、マンパワーがある程度ある外科ならできなくはないだろう
・術前化学療法となると、許容できる毒性や手術のタイミングを測るために、内科医と外科医の密な連携が欠かせない
・術前治療にこだわりすぎて、手術が出来なかったらなんにもならない
・今後周術期に抗がん薬、分子標的薬、免疫チェックポイント阻害薬が導入されたら、多分外科医では管理できなくなる
MMP1-4
皮膚科の立場から
・中部地方のがんセンターに勤める皮膚科医が発言
・皮膚科医は、免疫チェックポイント阻害薬を扱うようになって、考え方も考えられ方も変わった
昔の皮膚科医:
独自性が高く、閉鎖的な考え方を持ち、チーム医療には消極的
今の皮膚科医:がん薬物療法専門医のサポートをすることが多くなった
チーム医療に組み入れられるようになった
いろんな治療を見て、薬物療法への理解が進んだ
悪性黒色腫の治療を介して、他の診療科との連携が進んだ
がん薬物療法に対しては、駆け出し者の立場
昔の腫瘍内科医:
皮膚領域に対する関心が少ない、皮膚合併症は見過ごしがち、チーム医療には積極的
今の腫瘍内科医:
皮膚科医の治療をサポートしてくれる(治療選択、用量設定、有害事象管理など)
悪性黒色腫の治療に免疫チェックポイント阻害薬が導入されたことで、皮膚科領域への注目度が高まった
悪性黒色腫の患者の管理を手伝って、経験をつんで、自分たちの治療に活かそうと目論んでいる
あわよくば、悪性黒色腫の治療も皮膚科医から奪おうとしているきらいがある、縄張り荒らし
・免疫チェックポイント阻害薬と併用することで、皮膚合併症を起こしやすいとされる薬がある
去痰薬、プロトンポンプ阻害薬、ST合剤、抗痙攣薬、ベムラフェニブ、アレクチニブ
2017年07月28日
FLAURA positive!
ギリシャで生まれ、スペインでキャリアを積んでいるきれいな先生の講演を伺っていたら、シンガポールからやってきた先生が、
「昨日のプレスリリースで、FLAURAがpositiveになったって聞いたけど、あんたならこれからどうする?」
と質問された。
暑い中、神戸までお越しいただいてありがとうございます。
とても勉強になります。
昨日の今頃は、広東からお越しになった先生が第1世代、第2世代、第3世代のEGFR阻害薬を整理してお話ししてくださったけれど、1日にして適応を考え直さねばならなくなった。
もっとも、薬事承認されるまではまだ時間があるけれど、心の準備を整えておかなければ。
これで、gefitinibとerlotinibの出番は少なくなりそうだ。
osimertinibとdacomitinibが一次治療から使えるようになったら、afatinibの立ち位置も難しくなるだろう。
Tagrisso significantly improves progression-free survival in the Phase III FLAURA trial for lung cancer
27 July 2017
→https://www.astrazeneca.com/media-centre/press-releases/2017/tagrisso-significantly-improves-progression-free-survival-in-the-phase-iii-flaura-trial-for-lung-cancer-27072017.html
タグリッソは、第III相試験であるFLAURA試験において、EGFR遺伝子変異陽性の局所進行・進行非小細胞肺癌に対する一次治療で、主要評価項目である無増悪生存期間について、標準治療(erlotinibまたはgefitinib)に対して統計学的に有意な、そして臨床的に意味のある延長を達成した。効果・安全性・忍容性についてのプロファイルは、タグリッソ、erlotinib、gefitinibともに既知の内容と変わりなかった。FLAURA試験の評価は現在も継続しており、今後の各種学会で詳細な結果が公表される予定だ。
FLAURA試験は、未治療のEGFR遺伝子変異陽性局所進行・進行非小細胞肺癌患者を対象に、タグリッソ療法と標準療法(erlotinibまたはgefitinib)の効果を比較する、二重盲検無作為化第III相試験であり、30ヶ国から556人の患者が参加した。主要評価項目は無増悪生存期間で、副次評価項目は全生存期間、奏効割合、奏効持続期間、病勢コントロール割合、安全性、健康関連QoLである。
「昨日のプレスリリースで、FLAURAがpositiveになったって聞いたけど、あんたならこれからどうする?」
と質問された。
暑い中、神戸までお越しいただいてありがとうございます。
とても勉強になります。
昨日の今頃は、広東からお越しになった先生が第1世代、第2世代、第3世代のEGFR阻害薬を整理してお話ししてくださったけれど、1日にして適応を考え直さねばならなくなった。
もっとも、薬事承認されるまではまだ時間があるけれど、心の準備を整えておかなければ。
これで、gefitinibとerlotinibの出番は少なくなりそうだ。
osimertinibとdacomitinibが一次治療から使えるようになったら、afatinibの立ち位置も難しくなるだろう。
Tagrisso significantly improves progression-free survival in the Phase III FLAURA trial for lung cancer
27 July 2017
→https://www.astrazeneca.com/media-centre/press-releases/2017/tagrisso-significantly-improves-progression-free-survival-in-the-phase-iii-flaura-trial-for-lung-cancer-27072017.html
タグリッソは、第III相試験であるFLAURA試験において、EGFR遺伝子変異陽性の局所進行・進行非小細胞肺癌に対する一次治療で、主要評価項目である無増悪生存期間について、標準治療(erlotinibまたはgefitinib)に対して統計学的に有意な、そして臨床的に意味のある延長を達成した。効果・安全性・忍容性についてのプロファイルは、タグリッソ、erlotinib、gefitinibともに既知の内容と変わりなかった。FLAURA試験の評価は現在も継続しており、今後の各種学会で詳細な結果が公表される予定だ。
FLAURA試験は、未治療のEGFR遺伝子変異陽性局所進行・進行非小細胞肺癌患者を対象に、タグリッソ療法と標準療法(erlotinibまたはgefitinib)の効果を比較する、二重盲検無作為化第III相試験であり、30ヶ国から556人の患者が参加した。主要評価項目は無増悪生存期間で、副次評価項目は全生存期間、奏効割合、奏効持続期間、病勢コントロール割合、安全性、健康関連QoLである。
2017年07月28日
ICIsのシンポジウム
2017年7月28日 日本臨床腫瘍学会2日目(神戸市)
肺癌と免疫チェックポイント阻害薬に関する国際シンポジウム。
遅刻したため、残念ながら最初の2演題は聞き逃してしまった。
ISY 8-3
Possible biomarker for immune checkpoint inhibitor
・CheckMate 071, 057とKEYNOTE 024のsurvival curveの供覧
・抗PD-1抗体の効果とPD-L1発現の関係に関する総説
→Grigg et al.,J Immunother Cancer. 2016 Aug 16;4:48
→https://www.ncbi.nlm.nih.gov/pubmed/27532023
・Rizvi et al., Science 2015, 124-128
・国立がん研究センター東病院と大阪大学病院外科で2014年から2016年に完全切除された肺癌患者のうち、49人について切除肺と血液サンプルを検証
・扁平上皮癌21人、非扁平上皮癌28人
・CD8陽性T細胞の浸潤、PD-L1の発現、tumor mutational burdenはいずれも扁平上皮癌の方で有意に高度だった
・biomarkerとして有用そうな"factor X"について研究を進めているとのこと
ISY 8-4
Management of adverse event due to ICIs - via clinical experiences -
・ICIs(almost Nivolumab)のadverse event
common: rash, arthralgia, thyroid dysfunction
uncommon, but severe: colitis, pneumonitis, hypophysitis, type I DM
・colitis
CT scan can detect early phase of colitis (if symptoms presented).
PSL 1mg/kg/day, infliximab
・pneumonitis
prevalence in Japan
all grade: 58/1005=5.8%
>Grade 3: 34/1005=3.4%
Grade 5: 7/1005=0.7%
PSL, CPA, CsA
→Kenmotsu et al., ASCO 2017 abst.#9078
→Kato et al., ASCO 2017 abst.#9077
・hepatitis
mycophenolate mophetil
・thyroiditis
Use βblocker if hyperthyroidism with aparent symptoms
・hypophysitis
evaluation for fT3 or fT4, cortisol, ACTH at pre- and inter-treatment
TSH high, fT3 or fT4 normal: hypothyroidism
TSH low, fT3 or fT4 normal: hyperthyroidism
TSH normal, fT3 or fT4 normal: euthyroid or hypophysitis
symptoms: malaise, myalgia(on limb), diarrhea, hypereosinophilia etc.
・early onset ir-AEs are refered to favorable effects
治療開始後早期に甲状腺機能異常があると、治療効果も高い
→Osorio et al., Ann Oncol. 2017 Mar 1;28(3):583-589
→https://www.ncbi.nlm.nih.gov/pubmed/27998967
肺癌と免疫チェックポイント阻害薬に関する国際シンポジウム。
遅刻したため、残念ながら最初の2演題は聞き逃してしまった。
ISY 8-3
Possible biomarker for immune checkpoint inhibitor
・CheckMate 071, 057とKEYNOTE 024のsurvival curveの供覧
・抗PD-1抗体の効果とPD-L1発現の関係に関する総説
→Grigg et al.,J Immunother Cancer. 2016 Aug 16;4:48
→https://www.ncbi.nlm.nih.gov/pubmed/27532023
・Rizvi et al., Science 2015, 124-128
・国立がん研究センター東病院と大阪大学病院外科で2014年から2016年に完全切除された肺癌患者のうち、49人について切除肺と血液サンプルを検証
・扁平上皮癌21人、非扁平上皮癌28人
・CD8陽性T細胞の浸潤、PD-L1の発現、tumor mutational burdenはいずれも扁平上皮癌の方で有意に高度だった
・biomarkerとして有用そうな"factor X"について研究を進めているとのこと
ISY 8-4
Management of adverse event due to ICIs - via clinical experiences -
・ICIs(almost Nivolumab)のadverse event
common: rash, arthralgia, thyroid dysfunction
uncommon, but severe: colitis, pneumonitis, hypophysitis, type I DM
・colitis
CT scan can detect early phase of colitis (if symptoms presented).
PSL 1mg/kg/day, infliximab
・pneumonitis
prevalence in Japan
all grade: 58/1005=5.8%
>Grade 3: 34/1005=3.4%
Grade 5: 7/1005=0.7%
PSL, CPA, CsA
→Kenmotsu et al., ASCO 2017 abst.#9078
→Kato et al., ASCO 2017 abst.#9077
・hepatitis
mycophenolate mophetil
・thyroiditis
Use βblocker if hyperthyroidism with aparent symptoms
・hypophysitis
evaluation for fT3 or fT4, cortisol, ACTH at pre- and inter-treatment
TSH high, fT3 or fT4 normal: hypothyroidism
TSH low, fT3 or fT4 normal: hyperthyroidism
TSH normal, fT3 or fT4 normal: euthyroid or hypophysitis
symptoms: malaise, myalgia(on limb), diarrhea, hypereosinophilia etc.
・early onset ir-AEs are refered to favorable effects
治療開始後早期に甲状腺機能異常があると、治療効果も高い
→Osorio et al., Ann Oncol. 2017 Mar 1;28(3):583-589
→https://www.ncbi.nlm.nih.gov/pubmed/27998967
2017年07月28日
T-DM1 for HER2 positive NSCLC
2017年7月27日 日本臨床腫瘍学会総会(神戸市)
O1-5-6:HER2陽性非小細胞肺癌に対するT-DM1の第2相試験
・HER2陽性の患者はIHC+++ or IHC++かつFISH+ or Exon 20 mutation+の患者
・主要評価項目は奏効割合
・副次評価項目は有害事象、全生存期間、無増悪生存期間など
・閾値奏効割合は10%、期待奏効割合は30%、α=0.05、β=0.20
・予定患者数は30人とし、15人を集積した段階で中間解析を実施
・年齢中央値は67歳(45歳から77歳)
・男性7人、女性8人
・15人すべてが腺癌
・IHC+++ / IHC++かつFISH+ / Exon 20 mutation = 5 / 3 / 7
・EGFR遺伝子変異陽性患者が2人含まれていた
・CR 0人、PR 1人、奏効割合 6.7%で無効中止となった
・PRの患者も、あまり長く効果は続かなかった
O1-5-6:HER2陽性非小細胞肺癌に対するT-DM1の第2相試験
・HER2陽性の患者はIHC+++ or IHC++かつFISH+ or Exon 20 mutation+の患者
・主要評価項目は奏効割合
・副次評価項目は有害事象、全生存期間、無増悪生存期間など
・閾値奏効割合は10%、期待奏効割合は30%、α=0.05、β=0.20
・予定患者数は30人とし、15人を集積した段階で中間解析を実施
・年齢中央値は67歳(45歳から77歳)
・男性7人、女性8人
・15人すべてが腺癌
・IHC+++ / IHC++かつFISH+ / Exon 20 mutation = 5 / 3 / 7
・EGFR遺伝子変異陽性患者が2人含まれていた
・CR 0人、PR 1人、奏効割合 6.7%で無効中止となった
・PRの患者も、あまり長く効果は続かなかった
2017年07月28日
再生検がらみのポスター発表まとめ
2017年7月27日 日本臨床腫瘍学会総会(神戸市)
P1-122:当院におけるRe-biopsyの現状と問題点
腫瘍検体を用いたcobas法での検索と、血漿検体を用いたMBP-QP法での検索の比較
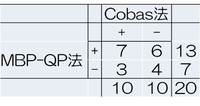
結果の一致率は11/20=55%
P1-123:EGFR遺伝子変異陽性非小細胞肺癌に対する再生検の後方視的検討
・56人を対象とした
・治療歴はgefitinib 18人、erlotinib 15人、afatinib 8人
・T790M陽性者は20人(36%)
・再生検の前後で組織型が変化したのは3人(5%)で、腺癌→小細胞癌が1人、腺癌→扁平上皮癌が1人、腺癌→大細胞神経内分泌癌が1人
P1-126:組織型転化を来たしたEGFR陽性肺癌症例の臨床的検討
・Ex.19 deletionの腺癌がEx.19 deletionの扁平上皮癌へ
・Ex.21+de novo T790Mの腺癌がEx.21+T790Mの扁平上皮癌へ
・Ex.19 deletionの腺癌がEx.19 deletionの小細胞癌へ(肝生検でも腰椎穿刺でも同じ結果だった)
・Ex.19 deletionの腺癌がEx.19 deletionの混合型小細胞癌(腺癌+小細胞癌)へ
P1-129:呼吸器内視鏡下再生検による耐性遺伝子T790Mの検出
・28人を対象とした
・腺癌26人、扁平上皮癌1人、小細胞癌1人
・再生検でT790M陽性と確認したのは10人(全体の38.5%)
・再々生検でT790M陽性と確認したのは3人、これを合わせると、T790M陽性患者は全体の48.1%)
P1-130:EGFR変異陽性非小細胞肺癌に対する、初回TKIとしてのアファチニブ投与例におけるT790M変異出現頻度の検討
・13施設での共同研究
・対象となった患者40人に再生検を行い、腫瘍細胞を採取できたのは37人
・Ex.19 deletion / Ex.21 point mutation / others = 21 / 13 / 3
・T790M陽性は16 / 37 = 43.2%
・Ex.19 deletionの患者でT790M陽性だったのは5人(23.8%)
・Ex.21 point mutationの患者でT790M陽性だったのは11人(84.6%)
・minor mutationの患者ではT790M検出されず
P1-166:非小細胞肺癌症例におけるEGFR遺伝子変異のモニタリング
・17人を対象とした
・腺癌15人、扁平上皮癌1人、NOS1人
・再生検時も組織型は変化なし
・T790Mは7人で陽性(41%)、そのうち、前治療がgefitinibだったのは6人、erlotinibだったのは1人
P1-122:当院におけるRe-biopsyの現状と問題点
腫瘍検体を用いたcobas法での検索と、血漿検体を用いたMBP-QP法での検索の比較

結果の一致率は11/20=55%
P1-123:EGFR遺伝子変異陽性非小細胞肺癌に対する再生検の後方視的検討
・56人を対象とした
・治療歴はgefitinib 18人、erlotinib 15人、afatinib 8人
・T790M陽性者は20人(36%)
・再生検の前後で組織型が変化したのは3人(5%)で、腺癌→小細胞癌が1人、腺癌→扁平上皮癌が1人、腺癌→大細胞神経内分泌癌が1人
P1-126:組織型転化を来たしたEGFR陽性肺癌症例の臨床的検討
・Ex.19 deletionの腺癌がEx.19 deletionの扁平上皮癌へ
・Ex.21+de novo T790Mの腺癌がEx.21+T790Mの扁平上皮癌へ
・Ex.19 deletionの腺癌がEx.19 deletionの小細胞癌へ(肝生検でも腰椎穿刺でも同じ結果だった)
・Ex.19 deletionの腺癌がEx.19 deletionの混合型小細胞癌(腺癌+小細胞癌)へ
P1-129:呼吸器内視鏡下再生検による耐性遺伝子T790Mの検出
・28人を対象とした
・腺癌26人、扁平上皮癌1人、小細胞癌1人
・再生検でT790M陽性と確認したのは10人(全体の38.5%)
・再々生検でT790M陽性と確認したのは3人、これを合わせると、T790M陽性患者は全体の48.1%)
P1-130:EGFR変異陽性非小細胞肺癌に対する、初回TKIとしてのアファチニブ投与例におけるT790M変異出現頻度の検討
・13施設での共同研究
・対象となった患者40人に再生検を行い、腫瘍細胞を採取できたのは37人
・Ex.19 deletion / Ex.21 point mutation / others = 21 / 13 / 3
・T790M陽性は16 / 37 = 43.2%
・Ex.19 deletionの患者でT790M陽性だったのは5人(23.8%)
・Ex.21 point mutationの患者でT790M陽性だったのは11人(84.6%)
・minor mutationの患者ではT790M検出されず
P1-166:非小細胞肺癌症例におけるEGFR遺伝子変異のモニタリング
・17人を対象とした
・腺癌15人、扁平上皮癌1人、NOS1人
・再生検時も組織型は変化なし
・T790Mは7人で陽性(41%)、そのうち、前治療がgefitinibだったのは6人、erlotinibだったのは1人



