2020年06月17日
ADAURA試験
ADAURA試験については、以前取り上げた。
http://oitahaiganpractice.junglekouen.com/e973395.html
無病生存期間の生存曲線を見ると、目を瞠る。
ハザード比0.17・・・。
そうそうお目にかかれない数字である。
本試験は、術後補助化学療法の標準治療であるプラチナ併用化学療法とオシメルチニブを比較したものではない。
EGFR遺伝子変異陽性の完全切除後非扁平上皮非小細胞肺がん患者を対象とし、適応のある患者には標準治療である術後補助化学療法を行い(詳しい治療レジメンの記載はないが)、その後にオシメルチニブを上乗せする意義があるかどうかを、プラセボ対照で検証した試験である。
実地臨床において、術後補助化学療法の適応はあるものの、年齢、背景疾患、患者の希望等々の理由で術後補助化学療法がおこなわれない患者は相当数いるため、こうした試験デザインでも一定の意義がある。
治療的にも医療経済的にも"toxic new"な治療だったわけだが、少なくともプラチナ併用術後補助化学療法の対象となるII期、IIIA期の患者に対しては、圧倒的な無病生存期間の延長効果を示している。
それも、「予定していなかった中間解析の結果を受けて、独立データモニタリング委員会が早期の非盲検化を勧告した」というほどの出来事であり、余程のことである。
多分、EGFRチロシンキナーゼ阻害薬関連試験の常で、全生存期間の延長は達成できないだろう。
それも、おそらくはオシメルチニブを術後補助療法として加えることにより再発を先延ばしにする効果が得られているだけで、オシメルチニブ群のプラセボ群の累積再発患者数は、おそらく有意差は出ないだろう。
そして、治癒を目指すべき患者を対象とした臨床試験で、全生存期間の延長が得られないときに、その治療に臨床的な意義があるのか、という議論が沸き起こるだろう。
しかし、再発なく過ごせる期間が圧倒的に長くなる、というのは、当然大きなアドバンテージだ。
また、本試験は、IB期とII / III期への対応を、明確に区別すべき世界的なきっかけになるかも知れない。
所属リンパ節転移を伴わないIB期と、伴う(ということは、既にリンパ路にのった腫瘍細胞が広い範囲に広がっている)II / III期では、おのずと異なる対応が必要となるだろう。
IB期に対する我が国の標準術後補助化学療法はUFT内服2年間だが、果たしてオシメルチニブは、この成績を凌駕できるだろうか。
http://oitahaiganpractice.junglekouen.com/e968113.html
また、II-IIIA期の患者で、術後補助化学療法が行われた患者と行われなかった患者で、無病生存期間や全生存期間に差が出るかどうかも見てみたいところである。
Osimertinib as adjuvant therapy in patients with stage IB-IIIA EGFR mutation positive NSCLC after complete tumor resection
Roy Herbst et al.
ASCO 2020 abst. #LBA5
背景:
オシメルチニブは第3世代の、中枢神経病変への活性を有するEGFRチロシンキナーゼ阻害薬で、EGFR遺伝子変異陽性の未治療進行非小細胞肺がんに対する治療において、ゲフィチニブやエルロチニブよりも効果が高いことが示されている。非小細胞肺がん患者の約30%はI-IIIA期の早期段階で診断され、この場合は外科手術が第一選択の治療である。II-III期、およびIB期の一部の患者では、切除後に術後補助化学療法を行うことが標準治療とされているが、いまだ術後再発率は高く、他の治療の必要性が叫ばれてきた。ADAURA試験は、完全切除後で、必要に応じて術後補助化学療法がおこなわれたIB-IIIA期のEGFR遺伝子変異陽性非小細胞肺がん患者を対象として、プラセボに対するオシメルチニブの有効性と安全性を評価することを目的とした第III相二重盲検ランダム化比較試験である。独立したデータモニタリング委員会の勧告に従い、本試験は有効性データをもとに早期の非盲検化を行うこととなった。そのため、今回は予定していなかった中間解析結果について報告する。
方法:
適格患者の条件は以下の通り。
・18歳以上(日本と台湾では20歳以上)
・WHO PS 0もしくは1
・IB, II, IIIA期の原発性非扁平上皮非小細胞肺がん
・EGFR遺伝子変異(エクソン19欠失変異 / エクソン21L858R点突然変異)が確認されている
・原発性非小細胞肺がん完全切除後で、術後状態から回復している
術後(補助)化学療法は許容された。対象患者はオシメルチニブ群(オシメルチニブ80mg/回を1日1回服用)とプラセボ群に1:1の割合で無作為に割り付けられ、3年間を上限としてプロトコール治療を受けた。病期(IB期 / II期 / IIIA期)、EGFR遺伝子変異のタイプ(エクソン19 / エクソン21)、人種(アジア人 / 非アジア人)を割り付け調整因子とした。主要評価項目はII-IIIA期の患者の無病生存期間とし、副次評価項目は全生存期間と安全性とした。データカットオフは2020年1月17日に設定された。
結果:
全体で、682人の患者が無作為割り付けされた。オシメルチニブ群は339人、プラセボ群は343人だった。背景因子は両群でバランスが取れていた。IB期患者はそれぞれ31%、II / IIIA期患者はそれぞれ69%、女性は68% / 72%、エクソン19変異は55% / 56%、エクソン21変異は45% / 44%だった。II-IIIA期の患者の無病生存期間に関するハザード比は0.17(95%信頼区間は0.12-0.23)で、p<0.0001(156 / 470イベント)と、オシメルチニブ群で有意に延長した。2年無病生存割合はオシメルチニブ群で90%、プラセボ群で44%だった。対象となった患者全体では、無病生存期間に関するハザード比は0.21(95%信頼区間は0.16-0.28)で、p<0.0001(196 / 682イベント)と、こちらもオシメルチニブ群で有意に延長した。2年無病生存割合はオシメルチニブ群で89%、プラセボ群で53%だった。データカットオフ時点での全生存期間データは未だ不十分で(データ確定は4%程度)、682人中29人が死亡していた(オシメルチニブ群で9人、プラセボ群で20人)。安全性については、オシメルチニブについて既に知られている内容と変わりはなかった。
結論:
オシメルチニブによる術後補助療法は、今回の対象集団に対して統計学的有意に、かつ臨床的にも意義のある無病生存期間の延長効果を示した。
・本試験のシェーマ

・患者背景

・試験結果概要

・無病生存期間生存曲線
II-IIIA期のみ(主要評価項目)

IB-IIIA期の全て
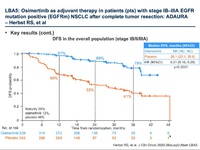
・各病期ごとの無病生存期間生存曲線

・サブグループ解析のフォレスト・プロット

・II期、IIIA期患者の全生存期間生存曲線

http://oitahaiganpractice.junglekouen.com/e973395.html
無病生存期間の生存曲線を見ると、目を瞠る。
ハザード比0.17・・・。
そうそうお目にかかれない数字である。
本試験は、術後補助化学療法の標準治療であるプラチナ併用化学療法とオシメルチニブを比較したものではない。
EGFR遺伝子変異陽性の完全切除後非扁平上皮非小細胞肺がん患者を対象とし、適応のある患者には標準治療である術後補助化学療法を行い(詳しい治療レジメンの記載はないが)、その後にオシメルチニブを上乗せする意義があるかどうかを、プラセボ対照で検証した試験である。
実地臨床において、術後補助化学療法の適応はあるものの、年齢、背景疾患、患者の希望等々の理由で術後補助化学療法がおこなわれない患者は相当数いるため、こうした試験デザインでも一定の意義がある。
治療的にも医療経済的にも"toxic new"な治療だったわけだが、少なくともプラチナ併用術後補助化学療法の対象となるII期、IIIA期の患者に対しては、圧倒的な無病生存期間の延長効果を示している。
それも、「予定していなかった中間解析の結果を受けて、独立データモニタリング委員会が早期の非盲検化を勧告した」というほどの出来事であり、余程のことである。
多分、EGFRチロシンキナーゼ阻害薬関連試験の常で、全生存期間の延長は達成できないだろう。
それも、おそらくはオシメルチニブを術後補助療法として加えることにより再発を先延ばしにする効果が得られているだけで、オシメルチニブ群のプラセボ群の累積再発患者数は、おそらく有意差は出ないだろう。
そして、治癒を目指すべき患者を対象とした臨床試験で、全生存期間の延長が得られないときに、その治療に臨床的な意義があるのか、という議論が沸き起こるだろう。
しかし、再発なく過ごせる期間が圧倒的に長くなる、というのは、当然大きなアドバンテージだ。
また、本試験は、IB期とII / III期への対応を、明確に区別すべき世界的なきっかけになるかも知れない。
所属リンパ節転移を伴わないIB期と、伴う(ということは、既にリンパ路にのった腫瘍細胞が広い範囲に広がっている)II / III期では、おのずと異なる対応が必要となるだろう。
IB期に対する我が国の標準術後補助化学療法はUFT内服2年間だが、果たしてオシメルチニブは、この成績を凌駕できるだろうか。
http://oitahaiganpractice.junglekouen.com/e968113.html
また、II-IIIA期の患者で、術後補助化学療法が行われた患者と行われなかった患者で、無病生存期間や全生存期間に差が出るかどうかも見てみたいところである。
Osimertinib as adjuvant therapy in patients with stage IB-IIIA EGFR mutation positive NSCLC after complete tumor resection
Roy Herbst et al.
ASCO 2020 abst. #LBA5
背景:
オシメルチニブは第3世代の、中枢神経病変への活性を有するEGFRチロシンキナーゼ阻害薬で、EGFR遺伝子変異陽性の未治療進行非小細胞肺がんに対する治療において、ゲフィチニブやエルロチニブよりも効果が高いことが示されている。非小細胞肺がん患者の約30%はI-IIIA期の早期段階で診断され、この場合は外科手術が第一選択の治療である。II-III期、およびIB期の一部の患者では、切除後に術後補助化学療法を行うことが標準治療とされているが、いまだ術後再発率は高く、他の治療の必要性が叫ばれてきた。ADAURA試験は、完全切除後で、必要に応じて術後補助化学療法がおこなわれたIB-IIIA期のEGFR遺伝子変異陽性非小細胞肺がん患者を対象として、プラセボに対するオシメルチニブの有効性と安全性を評価することを目的とした第III相二重盲検ランダム化比較試験である。独立したデータモニタリング委員会の勧告に従い、本試験は有効性データをもとに早期の非盲検化を行うこととなった。そのため、今回は予定していなかった中間解析結果について報告する。
方法:
適格患者の条件は以下の通り。
・18歳以上(日本と台湾では20歳以上)
・WHO PS 0もしくは1
・IB, II, IIIA期の原発性非扁平上皮非小細胞肺がん
・EGFR遺伝子変異(エクソン19欠失変異 / エクソン21L858R点突然変異)が確認されている
・原発性非小細胞肺がん完全切除後で、術後状態から回復している
術後(補助)化学療法は許容された。対象患者はオシメルチニブ群(オシメルチニブ80mg/回を1日1回服用)とプラセボ群に1:1の割合で無作為に割り付けられ、3年間を上限としてプロトコール治療を受けた。病期(IB期 / II期 / IIIA期)、EGFR遺伝子変異のタイプ(エクソン19 / エクソン21)、人種(アジア人 / 非アジア人)を割り付け調整因子とした。主要評価項目はII-IIIA期の患者の無病生存期間とし、副次評価項目は全生存期間と安全性とした。データカットオフは2020年1月17日に設定された。
結果:
全体で、682人の患者が無作為割り付けされた。オシメルチニブ群は339人、プラセボ群は343人だった。背景因子は両群でバランスが取れていた。IB期患者はそれぞれ31%、II / IIIA期患者はそれぞれ69%、女性は68% / 72%、エクソン19変異は55% / 56%、エクソン21変異は45% / 44%だった。II-IIIA期の患者の無病生存期間に関するハザード比は0.17(95%信頼区間は0.12-0.23)で、p<0.0001(156 / 470イベント)と、オシメルチニブ群で有意に延長した。2年無病生存割合はオシメルチニブ群で90%、プラセボ群で44%だった。対象となった患者全体では、無病生存期間に関するハザード比は0.21(95%信頼区間は0.16-0.28)で、p<0.0001(196 / 682イベント)と、こちらもオシメルチニブ群で有意に延長した。2年無病生存割合はオシメルチニブ群で89%、プラセボ群で53%だった。データカットオフ時点での全生存期間データは未だ不十分で(データ確定は4%程度)、682人中29人が死亡していた(オシメルチニブ群で9人、プラセボ群で20人)。安全性については、オシメルチニブについて既に知られている内容と変わりはなかった。
結論:
オシメルチニブによる術後補助療法は、今回の対象集団に対して統計学的有意に、かつ臨床的にも意義のある無病生存期間の延長効果を示した。
・本試験のシェーマ

・患者背景
・試験結果概要

・無病生存期間生存曲線
II-IIIA期のみ(主要評価項目)
IB-IIIA期の全て
・各病期ごとの無病生存期間生存曲線
・サブグループ解析のフォレスト・プロット
・II期、IIIA期患者の全生存期間生存曲線
セルペルカチニブ、上市
CLIP1-LTK融合遺伝子の発見・・・LC-SCRUM Asiaから
セルペルカチニブ、2021年12月13日発売予定
セルペルカチニブと過敏症
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
脳転移を有する患者集団に対しても、免疫チェックポイント阻害薬は有効なのか
第4世代ALK阻害薬・・・TPX-0131とNVL-655
セルペルカチニブ、製造販売承認
ドライバー遺伝子変異陽性患者におけるPACIFICレジメンの有効性
HER2遺伝子変異陽性肺がんに対するtrastuzumab deruxtecan
オシメルチニブ耐性化後は、耐性機序同定や分子標的治療は意味がないのか
EGFR/ALK陽性非小細胞肺がんに対するカルボプラチン+ペメトレキセド+ペンブロリズマブ併用療法
ドライバー遺伝子異常検出におけるジレンマとmultiplex PCR
中国人患者におけるRET阻害薬(Selpercatinib, Pralsetinib)の有効性
オシメルチニブによる術前療法・・・NeoADAURAの前哨戦
BRAF遺伝子変異と縁がない
RET阻害薬、セルペルカチニブがやってくる
進行が速い進行肺腺がんに遭遇したらどう振る舞うか
ARROW試験のupdated data...RET肺がんとpralsetinib
EGFRエクソン20挿入変異に対するAmivantamab
CLIP1-LTK融合遺伝子の発見・・・LC-SCRUM Asiaから
セルペルカチニブ、2021年12月13日発売予定
セルペルカチニブと過敏症
根治切除術直後の非小細胞肺がん患者に、バイオマーカー解析をするべきか
脳転移を有する患者集団に対しても、免疫チェックポイント阻害薬は有効なのか
第4世代ALK阻害薬・・・TPX-0131とNVL-655
セルペルカチニブ、製造販売承認
ドライバー遺伝子変異陽性患者におけるPACIFICレジメンの有効性
HER2遺伝子変異陽性肺がんに対するtrastuzumab deruxtecan
オシメルチニブ耐性化後は、耐性機序同定や分子標的治療は意味がないのか
EGFR/ALK陽性非小細胞肺がんに対するカルボプラチン+ペメトレキセド+ペンブロリズマブ併用療法
ドライバー遺伝子異常検出におけるジレンマとmultiplex PCR
中国人患者におけるRET阻害薬(Selpercatinib, Pralsetinib)の有効性
オシメルチニブによる術前療法・・・NeoADAURAの前哨戦
BRAF遺伝子変異と縁がない
RET阻害薬、セルペルカチニブがやってくる
進行が速い進行肺腺がんに遭遇したらどう振る舞うか
ARROW試験のupdated data...RET肺がんとpralsetinib
EGFRエクソン20挿入変異に対するAmivantamab








